Clear Sky Science · nl
Long tumouroiden als testplatform voor precieze CAR T-celtherapie
Waarom kleine longmodellen van belang zijn voor patiënten
Longkanker blijft wereldwijd de dodelijkste vorm van kanker, grotendeels omdat elke tumor anders is en vaak leert therapie te ontlopen. Deze studie introduceert een methode om miniatuur, patiëntspecifieke replica’s van longtumoren in het laboratorium te kweken en ze te gebruiken als testterrein voor geavanceerde immuuntherapieën, zogeheten CAR T‑cellen. Door deze tumor "mini‑organen" te vergelijken met overeenkomende gezonde longorganoïden uit dezelfde patiënt laten de onderzoekers zien hoe artsen mogelijk kunnen voorspellen welke behandelingen zullen werken, welke zullen falen en hoe gevaarlijke bijwerkingen voorkomen kunnen worden voordat de patiënt wordt behandeld.
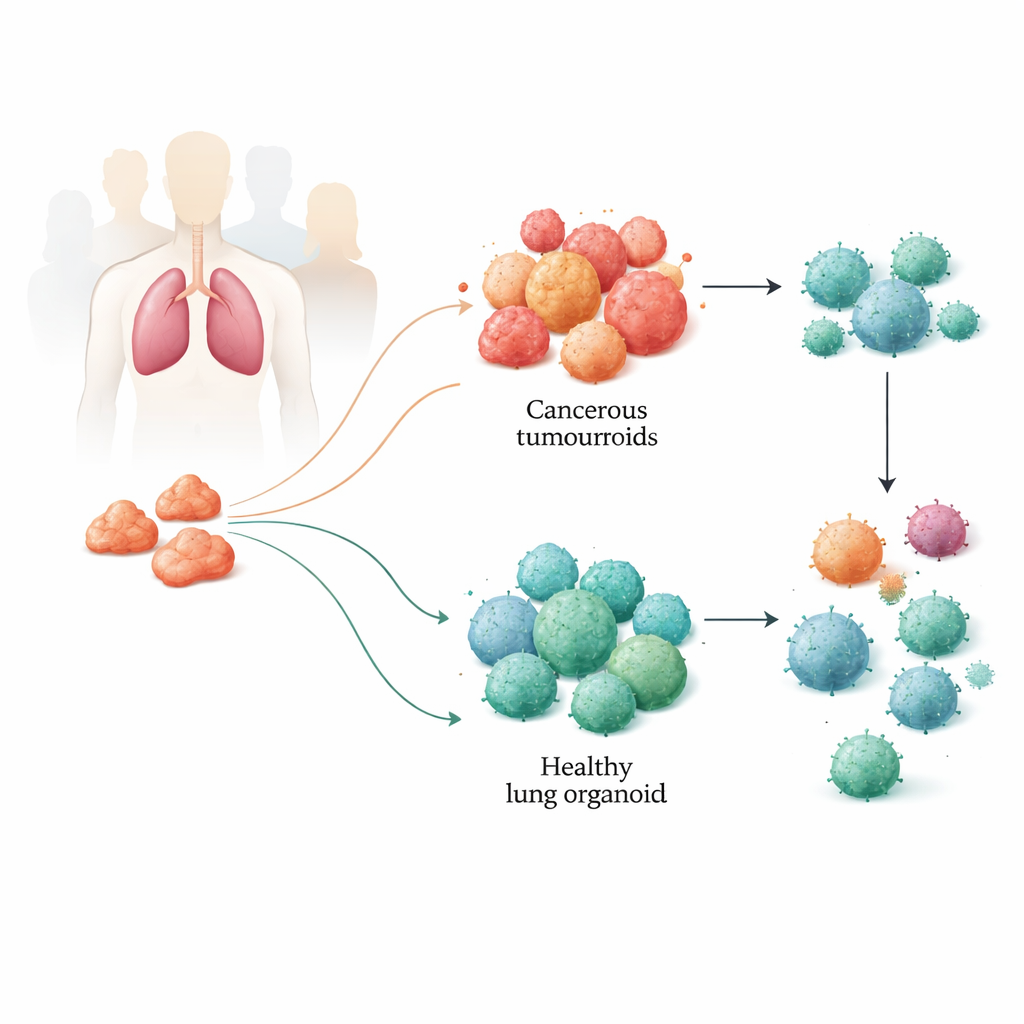
Miniatuurlongen opbouwen uit patiëntweefsel
Het team verzamelde tumormonsters en nabijgelegen gezond longweefsel van patiënten die longkankeroperaties ondergingen. Uit deze monsters kweekten ze driedimensionale structuren die bekendstaan als organoïden: tumouroiden uit kankergezwel en gezonde organoïden uit normaal longweefsel. Deze kleine bolletjes organiseren zichzelf en kunnen maandenlang in leven worden gehouden. Zorgvuldige genetische, epigenetische en proteïneniveau‑analyses toonden aan dat de tumouroiden de belangrijke moleculaire kenmerken van de oorspronkelijke tumoren behielden, inclusief veelvoorkomende longkankermutaties en hun complexe mengsel van celtypen. De gezonde organoïden behielden op hun beurt de kenmerken van niet‑kankerig longweefsel, waardoor de onderzoekers een betrouwbare zij‑aan‑zij‑model van de ziekte en het normale longweefsel van elke patiënt kregen.
De respons op geneesmiddelen nabootsen
Om te testen of deze mini‑organen werkelijk weerspiegelen wat er bij patiënten gebeurt, stelden de onderzoekers de tumouroiden bloot aan dezelfde chemotherapie en gerichte middelen die de patiënten al hadden gekregen. Met live‑cell‑imaging en levensvatbaarheidsassays ontdekten ze dat tumouroiden vaak gedroegen zoals de oorspronkelijke tumoren in de kliniek: monsters van patiënten waarvan de kanker resistent was tegen een middel waren vaak ook resistent in het schaaltje, terwijl tumouroiden van patiënten met gedeeltelijke respons gevoeliger waren. Proteomische profilering — het gelijktijdig meten van duizenden eiwitten — onthulde patronen die samenhingen met medicijnresistentie, zoals hoge niveaus van moleculen die eerder in verband werden gebracht met slechte respons op platinumchemotherapie. Deze bevindingen suggereren dat tumouroiden gebruikt zouden kunnen worden om te voorspellen of een bepaald middel waarschijnlijk zal helpen bij een individuele patiënt.
Maatwerktesten van immuuncellen van de volgende generatie
Het middelpunt van de studie is een workflow om CAR T‑celtherapie op maat te maken, een krachtige benadering waarbij de T‑cellen van een patiënt worden aangepast om specifieke merkers op kankercellen te herkennen. De wetenschappers screeneden eerst tumor- en gezond weefsel, evenals hun bijbehorende organoïden, op potentiële doelmoleculen aan het celoppervlak. Vervolgens genereerden ze panelen CAR T‑cellen — met een virusvrije genetische bewerkingsmethode — om veelbelovende doelen te herkennen zoals HER2 of PDL1, die op sommige longkankers aanwezig zijn. Door deze CAR T‑cellen samen te kweken met tumouroiden en gezonde organoïden konden ze gelijktijdig beoordelen hoe sterk de immuuncellen werden geactiveerd, hoeveel tumorschade ze veroorzaakten en of ze gezond‑achtig longweefsel schaadden.
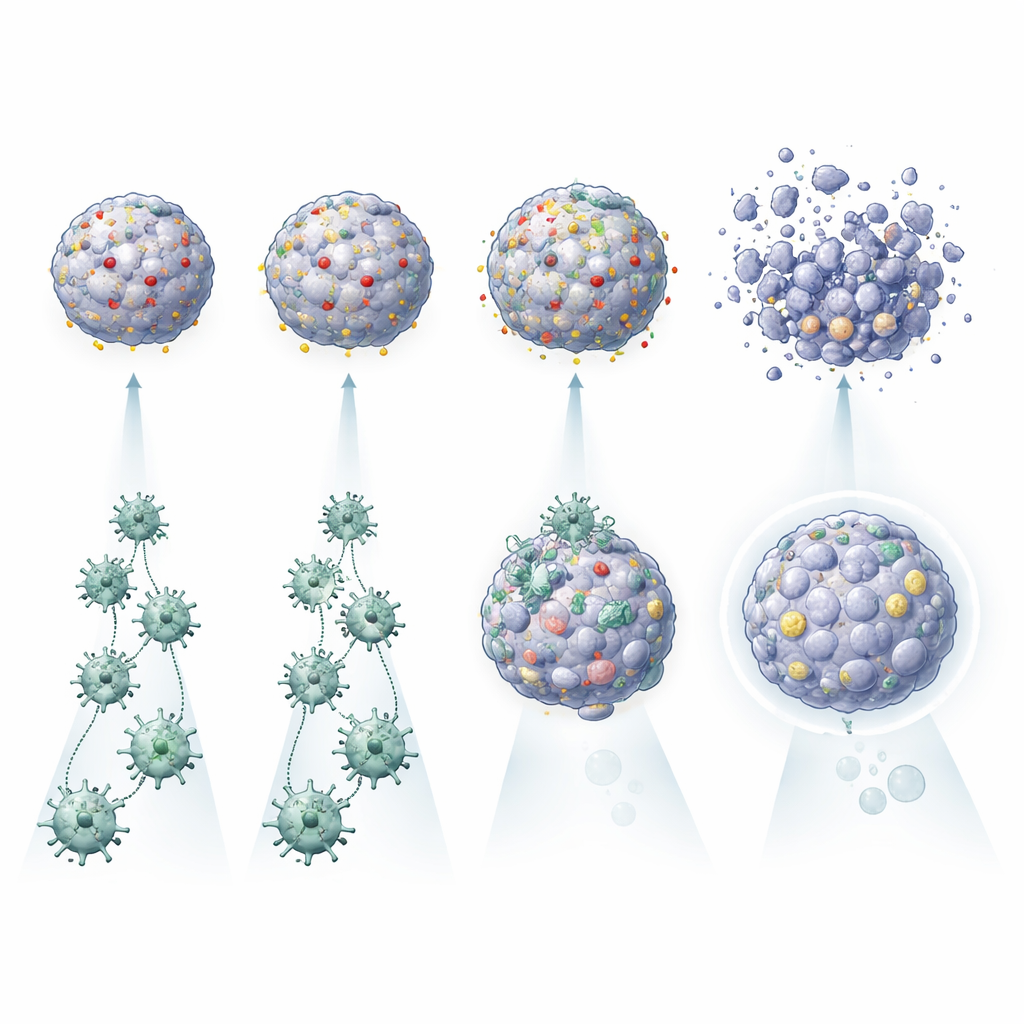
Ontdekken waarom sommige tumoren resistent zijn tegen CAR T‑cellen
Een opvallend resultaat was dat activatie van CAR T‑cellen op zichzelf geen effectieve tumordoding garandeerde. In de tumouroiden van sommige patiënten werden CAR T‑cellen geactiveerd en gaven ze ontstekingsmoleculen af, maar veroorzaakten ze slechts beperkte schade aan de kankermini‑organen. Bij anderen, met name die waarvan het tumoroppervlak veel kopieën van het doelmolecuul droeg, vernietigden dezelfde CAR T‑cellen de tumouroiden veel efficiënter. Het platform bracht ook subtielere invloeden aan het licht: tumouroiden die bepaalde cytokines afscheidden, zoals IL‑6, leken betere CAR T‑activiteit te ondersteunen, terwijl tumouroiden die rijk waren aan autophagie‑ en immuunontwijkingsproteïnen, of die onder ontstekingscondities scherp PDL1 konden verhogen, moeilijker te elimineren waren. Door elke tumor te vergelijken met zijn eigen gezonde organoïden kon het team ook patiënten identificeren voor wie een bepaald CAR‑ontwerp normaal longweefsel zou sparen — of onaanvaardbare risico’s zou vormen.
Wat dit kan betekenen voor toekomstige kankerzorg
In eenvoudige bewoordingen toont dit werk aan dat patiëntafgeleide long tumouroiden kunnen fungeren als realistische "crashtestpoppen" voor zowel standaardmedicatie als geavanceerde immuuntherapieën. Het model reproduceert echte patiëntreacties op behandeling, onthult waarom sommige tumoren bezwijken terwijl andere resistent blijven, en belicht wanneer een veelbelovende CAR T‑benadering ook gezonde longcellen kan beschadigen. Hoewel verdere verfijning nodig is, wijst dit platform naar een toekomst waarin oncologen de eigen mini‑tumoren van een patiënt gebruiken om therapieën te kiezen en fijn af te stemmen — inclusief op maat gemaakte CAR T‑cellen — voordat de patiënt aan de risico’s wordt blootgesteld.
Bronvermelding: Ehlen, L., Farrera-Sal, M., Szyska, M. et al. Lung tumouroids as a testing platform for precision CAR T cell therapy. Nat. Biomed. Eng 10, 815–831 (2026). https://doi.org/10.1038/s41551-025-01594-3
Trefwoorden: longkanker, organoïden, CAR T-celtherapie, precisiemedicine, immunotherapieresistentie