Clear Sky Science · tr
Yeni bir çok‑epitop aşı, Helicobacter pylori’ye karşı koruyucu ve terapötik bağışıklık sağlıyor
Günlük sağlık açısından neden önemli
Çoğu insan Helicobacter pylori adını hiç duymayacak, ancak bu spiral biçimli bakteri dünyanın yaklaşık yarısını sessizce enfekte eder ve mide ülserlerine, hatta mide kanserine yol açabilir. Bugün tek güvenilir tedavi bir antibiyotik karışımıdır, ancak artan ilaç direnci bu tedavilerin etkinliğini azaltıyor. Bu çalışma, yalnızca farelerde enfeksiyonu önlemekle kalmayan, aynı zamanda uzun süredir devam eden mide enfeksiyonlarını da ortadan kaldıran yeni tür deneysel bir aşıyı tanımlıyor; bu da gelecekte karmaşık ilaç rejimlerinin yerini basit bir enjeksiyonun alabileceğine işaret ediyor.
Sessiz bir mide istilacısı
H. pylori mide asidinin zorlu ortamında yaşamaya özgü şekilde uyum sağlar ve orada on yıllarca kalabilir. Pek çok kişi asla belirti geliştirmez, ancak bazıları için bakteri kronik iltihap, ağrılı ülserler ve önemli ölçüde artmış mide kanseri riski tetikler. Standart antibiyotik tedavileri, mikrop direnç geliştirdikçe etkisini kaybediyor ve önceki aşı girişimleri defalarca başarısız oldu. Daha önceki aşılar genellikle tek bakteri proteini kullanıyordu ve güçlü antikor yanıtı oluşturabilse de klinik deneylerde kalıcı koruma sağlayamadı. Araştırmacılar artık H. pylori’nin uzun vadeli başarılı kontrolünün hem antikor üreten hücrelerden hem de bağışıklık saldırılarını yönlendiren uzmanlaşmış T hücrelerinden oluşan koordineli bir yanıt gerektirdiğini düşünüyor.
Daha akıllı bir aşı inşa etmek
Tam bakteri proteinlerini enjekte etmek yerine ekip “çok‑epitop” bir aşı tasarladı. Epitoplar, bağışıklık sisteminin gerçekten tanıdığı protein parçacıklarıdır. Bilgisayar araçları kullanarak araştırmacılar altı önemli H. pylori virülans faktörü — bakterinin asitte hayatta kalmak, hareket etmek, mide hücrelerine tutunmak ve savunmalardan kaçmak için kullandığı moleküller — arasında tarama yaptı. Bunlardan B hücreleri (antikor üreten) ve T hücreleri (hücresel bağışıklığı yöneten) tarafından özellikle görünür olması öngörülen on altı kısa bölge seçildi. Bu parçalar, her bir parçanın net biçimde algılanmasına yardımcı olacak kısa bağlayıcılarla ayrılarak Tek Bir yapay antijen olan Çok‑Epitop Birimi (Multi‑Epitope Unit, MEU) adıyla birleştirildi; böylece bütün molekül kararlı, alerjen olmayan ve çözünebilir kaldı.
Yerleşik bir bağışıklık güçlendirici eklemek
Bu tasarlanmış antijenin bağışıklık sisteminin dikkatini çekmesini sağlamak için araştırmacılar onu doğal olarak TLR5 adlı alarm reseptörünü tetikleyen başka bir bakteriden alınan flagellin proteininin ana parçalarına füze ettiler. Ayrıca MEU talimatlarını, güçlü T hücre yanıtları uyandırma yeteneğiyle bilinen Zararsız Değiştirilmiş Vaccinia Ankara (MVA) adlı viral bir vektöre yerleştirerek aşıya ikinci bir versiyon da oluşturdular. Fare çalışmalarında MEU ya flagellin‑füzyonlu bir protein olarak, ya MVA‑tabanlı vektör olarak verildi ya da her iki formatı birleştiren “prime‑boost” (başlat‑güçlendir) düzeninde uygulandı. Laboratuvar testleri, füzyon proteininin amaçlandığı gibi TLR5 yolunu aktive ettiğini ve kendi adjuvanı gibi davrandığını; MVA vektörünün ise enfekte hücreler içinde MEU antijenini verimli şekilde ürettiğini doğruladı.
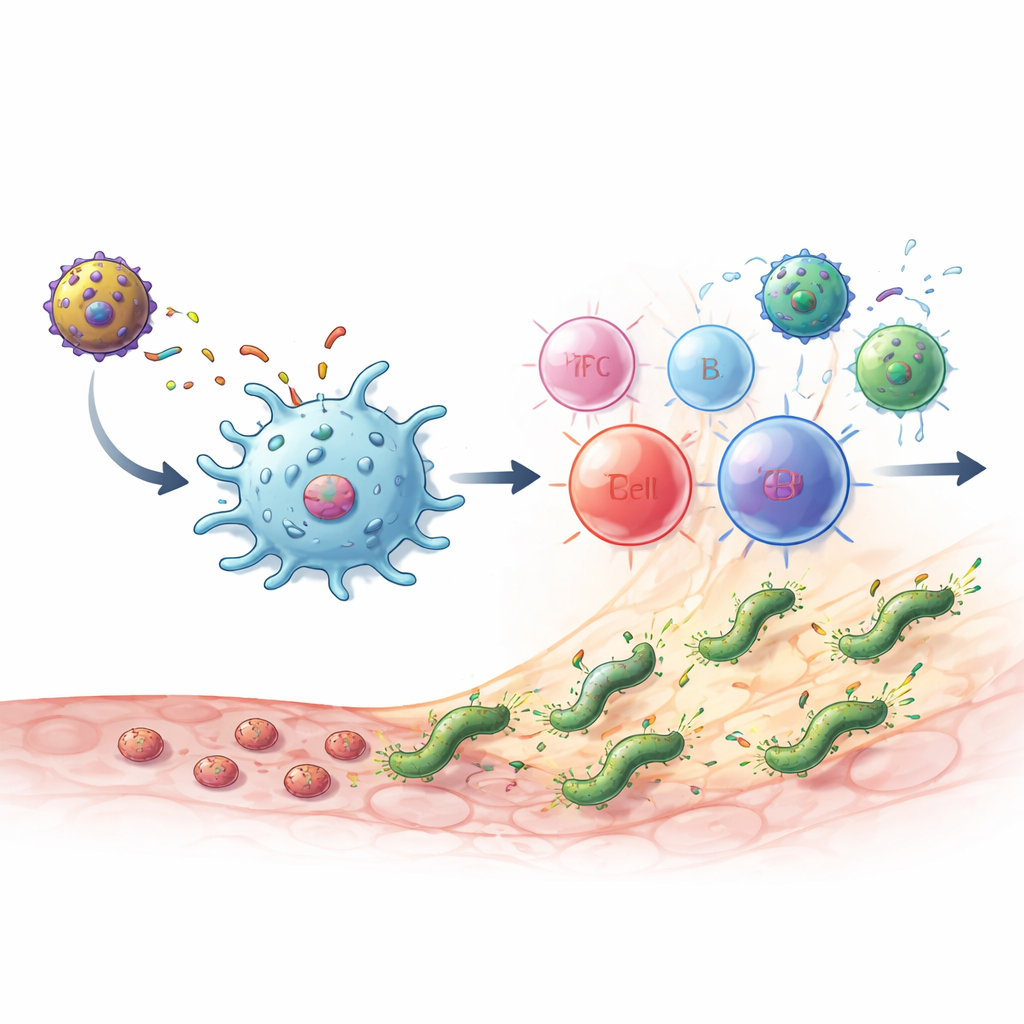
Enfekte farelerde ne oldu
Sağlıklı farelere aşı verildiğinde yüksek düzeyde MEU‑spesifik antikorlar ile IL‑2 ve interferon‑gamma gibi temel haberci moleküller üreten CD4 T hücreleri ortaya çıktı. Yanıt, mikrobu doğrudan öldürmeyle ilişkili bir yardımcı T hücre türü ile antikor üretimini destekleyen ve doku hasarını sınırlamaya yardımcı olan diğer ana yardımcı T hücre türü arasında sağlıklı bir denge gösterdi. Doğal ve edinilmiş bağışıklığı birbirine bağlayan NKT‑benzeri hücreler gibi önemli “köprü” hücreler de genişledi. En güçlü düzen, heterolog prime‑boost idi: önce MEU‑flagellin proteini, ardından MVA‑MEU vektörü. Hem koruyucu testlerde (maruziyetten önce aşılamak) hem de terapötik testlerde (kronik enfeksiyon yerleştikten sonra aşılamak) ya bu kombinasyon ya da iki doz MVA‑MEU, kültür ve genetik testlerle ölçüldüğünde midede tespit edilebilir H. pylori’yi tamamen temizledi.
Gelecekte bakım için ne anlama gelebilir
Bir uzman olmayan için sonuç çarpıcı: zorlu bir fare modelinde bu özenle tasarlanmış çok‑epitop aşı sadece H. pylori’nin yerleşmesini engellemekle kalmadı, aynı zamanda uzun süreli insan hastalığını taklit eden kökleşmiş enfeksiyonları da ortadan kaldırdı. Aynı anda birçok korunmuş bakteri parçasını hedefleyip bunları güçlü, yerleşik bir bağışıklık güçlendirici ve viral bir taşıyıcı sistemiyle eşleştirerek bu yaklaşım, önceki daha basit aşıların başarısız olmasına neden olan sınırlamaları aşıyor. Çalışma şimdi daha büyük hayvanlarda güvenlik çalışmalarına geçiyor. İnsanlarda benzer koruma sağlanabilirse, bu strateji bir gün ülserlere, mide kanserine ve bu olağanüstü dirençli mikroptan kaynaklanan antibiyotik direncine karşı çift yönlü bir darbe sunabilir.
Atıf: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Anahtar kelimeler: Helicobacter pylori, mide enfeksiyonu, çok‑epitop aşı, antibiyotik direnci, mide kanseri önleme