Clear Sky Science · sv
En ny multi-epitop-vaccin framkallar skyddande och terapeutiskt immunförsvar mot Helicobacter pylori
Varför detta betyder något för vardagshälsan
De flesta kommer aldrig höra namnet Helicobacter pylori, ändå infekterar denna spiralformade bakterie tyst omkring hälften av jordens befolkning och kan leda till magsår och till och med magsäckscancer. I dag är den enda pålitliga boten en blandning av antibiotika, men växande läkemedelsresistens gör dessa behandlingar mindre effektiva. Denna studie beskriver en ny typ av experimentellt vaccin som inte bara förhindrar infektion hos möss utan också rensar långvariga maginfektioner, vilket pekar mot en framtid där en enkel spruta kan ersätta komplexa läkemedelsregimer.
En tyst maginvasör
H. pylori är unikt anpassad för att leva i magsäckens hårda syra och kan dröja kvar där i årtionden. Många utvecklar aldrig symtom, men för andra utlöser bakterien kronisk inflammation, smärtsamma sår och en kraftigt ökad risk för magsäckscancer. Standardantibiotikabehandlingar förlorar mark när mikroben utvecklar resistens, och tidigare vaccinförsök har upprepade gånger misslyckats. Tidigare vacciner använde ofta enstaka bakteriella proteiner och kunde ge höga antikroppsnivåer, men de lyckades inte ge varaktigt skydd i kliniska prövningar. Forskare misstänker nu att framgångsrik, långsiktig kontroll av H. pylori kräver ett samordnat svar från både antikroppsproducerande celler och specialiserade T‑celler som dirigerar immunsvar.
Bygga ett smartare vaccin
I stället för att injicera hela bakteriella proteiner designade teamet ett "multi‑epitop"-vaccin. Epitoper är de nyckelavsnitt av ett protein som immunsystemet faktiskt känner igen. Med datorverktyg sållade forskarna igenom sex viktiga H. pylori-virulensfaktorer — molekyler som bakterien använder för att överleva i syra, röra sig, fästa vid magsäcksceller och undvika försvaret. Av dessa valde de sexton korta regioner som förutspåddes vara särskilt väl synliga för B‑celler (som bildar antikroppar) och T‑celler (som orkestrerar cellulärt immunförsvar). De satte ihop dessa bitar till ett enda konstgjort antigen kallat Multi‑Epitope Unit, eller MEU, åtskilda av korta länkar för att hjälpa immunsystemet att se varje del tydligt samtidigt som hela molekylen förblev stabil, icke‑allergen och löslig.
Lägga till en inbyggd immunstärkare
För att säkerställa att immunsystemet uppmärksammade detta konstruerade antigen sammanfogade forskarna det med viktiga delar av flagellin, ett protein från en annan bakterie som naturligt aktiverar en larmsensor känd som TLR5. De byggde också en andra version av vaccinet genom att infoga MEU‑instruktionerna i en ofarlig viral vektor kallad Modified Vaccinia Ankara (MVA), känd för att ge starka T‑cellsvar. I musstudier gavs MEU antingen som flagellin‑fuserat protein, som MVA‑baserad vektor eller i ett "prime‑boost"-schema som kombinerade båda formaten. Laboratorietester bekräftade att fusionsproteinet aktiverade TLR5‑vägen som avsett, fungerade som sin egen adjuvans, och att MVA‑vektorn effektivt producerade MEU‑antigenet inne i infekterade celler.
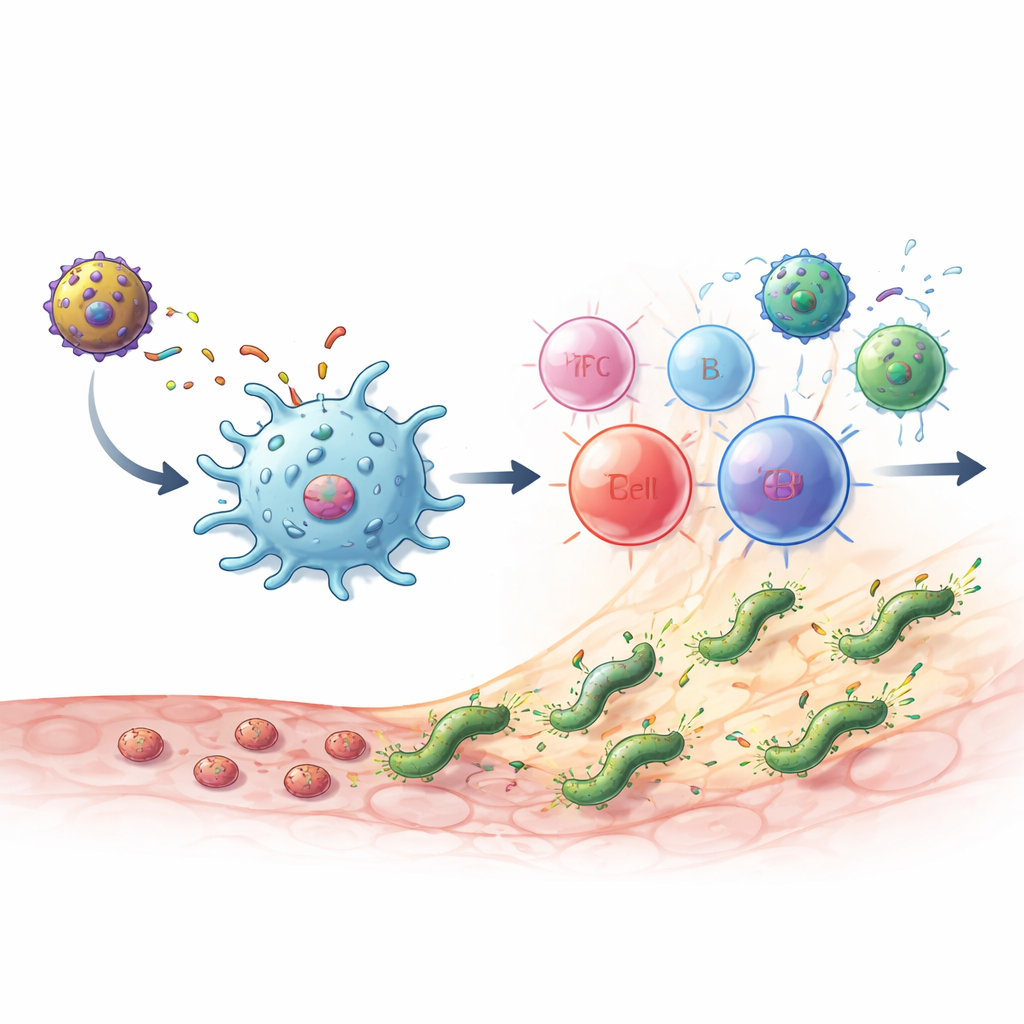
Vad som hände i infekterade möss
När friska möss fick vaccinerna frambringade de höga nivåer av MEU‑specifika antikroppar samt CD4‑T‑celler som producerade viktiga budbärarmolekyler som IL‑2 och interferon‑gamma. Svaret visade en sund balans mellan två stora hjälpar‑T‑cellstyper: en kopplad till direkt mikrobdödande och en annan som stöder antikroppsbildning och hjälper till att begränsa vävnadsskada. Viktiga "bro"‑celler som förbinder medfött och adaptivt immunförsvar, till exempel NKT‑liknande celler, expanderade också. Det mest kraftfulla schemat var en heterolog prime‑boost: först MEU‑flagellinproteinet, sedan MVA‑MEU‑vektorn. I både preventiva tester (vaccination före exponering) och terapeutiska tester (vaccination efter att kronisk infektion etablerats) rensade antingen denna kombination eller två doser av MVA‑MEU fullständigt detekterbar H. pylori från magen, mätt med odling och genetiska tester.
Vad detta kan betyda för framtida vård
För en icke‑specialist är slutsatsen slående: i en krävande musmodell blockerade detta omsorgsfullt konstruerade multi‑epitop‑vaccin inte bara att H. pylori etablerade sig utan eliminerade också inbitna infektioner som efterliknar långvarig mänsklig sjukdom. Genom att rikta in sig på många bevarade bakteriedelar på en gång och kombinera dem med en stark, inbyggd immunstärkare och ett virusbaserat leveranssystem övervinner metoden begränsningar som fällde tidigare, enklare vacciner. Arbetet går nu vidare till säkerhetsstudier i större djur. Om liknande skydd kan uppnås hos människor skulle denna strategi en dag kunna erbjuda ett tvåstegsangrepp mot sår, magsäckscancer och antibiotikaresistens drivet av denna anmärkningsvärt persistenta mikrob.
Citering: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Nyckelord: Helicobacter pylori, maginfektion, multi-epitop-vaccin, antibiotikaresistens, förebyggande av magsäckscancer