Clear Sky Science · pl
Nowa wieloekpitopowa szczepionka wywołuje odporność ochronną i terapeutyczną przeciw Helicobacter pylori
Dlaczego to ma znaczenie dla codziennego zdrowia
Większość ludzi nigdy nie usłyszy nazwy Helicobacter pylori, a jednak ta spiralna bakteria cicho zakaża około połowy światowej populacji i może prowadzić do wrzodów żołądka, a nawet raka żołądka. Obecnie jedynym niezawodnym leczeniem jest koktajl antybiotyków, lecz narastająca oporność lekowa osłabia skuteczność tych terapii. W badaniu opisano nowy typ eksperymentalnej szczepionki, która nie tylko zapobiega zakażeniu u myszy, lecz także usuwa długo utrzymujące się infekcje żołądka, wskazując na przyszłość, w której proste zastrzyki mogłyby zastąpić skomplikowane schematy leczenia.
Cichy intruz w żołądku
H. pylori jest wyjątkowo przystosowany do życia w silnie kwaśnym środowisku żołądka i może utrzymywać się tam przez dziesięciolecia. U wielu osób nie wywołuje objawów, ale u innych bakteria wywołuje przewlekłe zapalenie, bolesne wrzody i znacznie zwiększone ryzyko raka żołądka. Standardowe terapie antybiotykowe tracą skuteczność, gdy mikroorganizm rozwija oporność, a wcześniejsze próby szczepionek wielokrotnie nie przyniosły oczekiwanych rezultatów. Starsze szczepionki często wykorzystywały pojedyncze białka bakteryjne i potrafiły zwiększyć poziom przeciwciał, lecz nie zapewniały trwałej ochrony w badaniach klinicznych. Badacze podejrzewają obecnie, że skuteczne, długotrwałe kontrolowanie H. pylori wymaga skoordynowanej odpowiedzi zarówno komórek produkujących przeciwciała, jak i wyspecjalizowanych komórek T, które kierują komórkowym atakiem immunologicznym.
Budowa „mądrzejszej” szczepionki
Zamiast wstrzykiwać całe białka bakteryjne, zespół zaprojektował szczepionkę „wieloepitopową”. Epitopy to kluczowe fragmenty białka, które układ odpornościowy rzeczywiście rozpoznaje. Za pomocą narzędzi komputerowych badacze przeszukali sześć istotnych czynników wirulencji H. pylori — cząsteczek, których bakteria używa do przetrwania w kwaśnym środowisku, poruszania się, przylegania do komórek żołądka i unikania obrony. Z tych wybrali szesnaście krótkich odcinków przewidywanych jako szczególnie widoczne dla komórek B (wytwarzających przeciwciała) i komórek T (koordynujących odporność komórkową). Połączyli te fragmenty w pojedynczy sztuczny antygen nazwany Jednostką Wieloepitopową, czyli MEU, rozdzielając je krótkimi łącznikami, aby układ odpornościowy mógł wyraźnie widzieć każdy element, a jednocześnie utrzymać cząsteczkę stabilną, niealergiczną i rozpuszczalną.
Dodanie wbudowanego wzmacniacza odporności
Aby zapewnić, że układ odpornościowy zwróci uwagę na ten zaprojektowany antygen, badacze połączyli go z kluczowymi fragmentami flageliny — białka z innej bakterii, które naturalnie aktywuje receptor alarmowy znany jako TLR5. Stworzyli także drugą wersję szczepionki, umieszczając instrukcję MEU w nieszkodliwym wektorze wirusowym zwanym zmodyfikowaną szczepionką przeciwko ospie (Modified Vaccinia Ankara, MVA), znanym z silnego wywoływania odpowiedzi komórek T. W badaniach na myszach MEU podawano jako białko sprzężone z flageliną, jako wektor oparty na MVA lub w schemacie „prime‑boost”, łącząc oba formaty. Testy laboratoryjne potwierdziły, że białko sprzężone aktywowało ścieżkę TLR5 zgodnie z założeniem, działając jako własny adiuwant, oraz że wektor MVA efektywnie produkował antygen MEU wewnątrz zakażonych komórek.
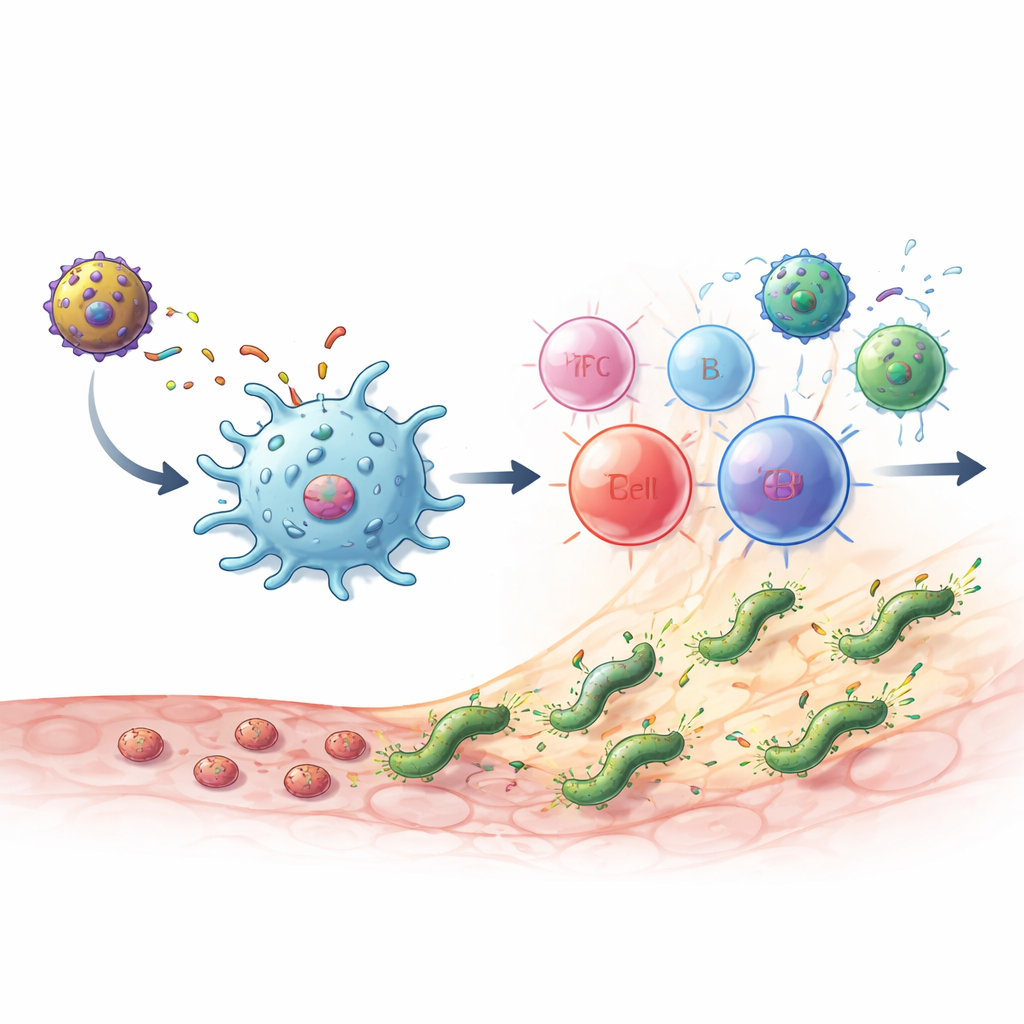
Co się stało u zakażonych myszy
Gdy zdrowe myszy otrzymały szczepionki, wytworzyły wysokie poziomy przeciwciał specyficznych dla MEU oraz komórek CD4 T produkujących kluczowe cząsteczki sygnalizacyjne, takie jak IL‑2 i interferon‑gamma. Odpowiedź wykazywała zdrową równowagę dwóch głównych typów pomocniczych komórek T: jednego związanego z bezpośrednim zabijaniem drobnoustrojów i drugiego wspierającego produkcję przeciwciał i pomagającego ograniczać uszkodzenia tkanki. Istotne komórki „mostowe”, łączące odporność wrodzoną i adaptacyjną, takie jak komórki podobne do NKT, również się rozrosły. Najskuteczniejszy schemat to heterologiczny prime‑boost: najpierw białko MEU‑flagelina, następnie wektor MVA‑MEU. Zarówno w testach zapobiegawczych (szczepienie przed ekspozycją), jak i terapeutycznych (szczepienie po ustaleniu przewlekłej infekcji), kombinacja ta lub dwie dawki MVA‑MEU całkowicie usunęły wykrywalne H. pylori z żołądka, mierzone hodowlą i badaniami genetycznymi.
Co to może znaczyć dla przyszłej opieki
Dla nietechnika wniosek jest uderzający: w wymagającym modelu mysiego ta starannie zaprojektowana wieloepitopowa szczepionka nie tylko uniemożliwiła zasiedlenie H. pylori, lecz także wyeliminowała utrwalone infekcje, które naśladują długotrwałą chorobę u ludzi. Dzięki jednoczesnemu ukierunkowaniu na wiele konserwowanych fragmentów bakteryjnych oraz sparowaniu ich z silnym, wbudowanym wzmacniaczem odporności i systemem dostarczania wirusowego, podejście to przezwycięża ograniczenia, które pogrzebały wcześniejsze, prostsze szczepionki. Prace są obecnie kontynuowane w badaniach bezpieczeństwa na większych zwierzętach. Jeśli podobna ochrona zostanie osiągnięta u ludzi, ta strategia mogłaby pewnego dnia zaoferować podwójny cios przeciw wrzodom, rakowi żołądka i oporności na antybiotyki napędzanej przez ten wyjątkowo trwały drobnoustrój.
Cytowanie: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Słowa kluczowe: Helicobacter pylori, zakażenie żołądka, wieloepitopowa szczepionka, oporność na antybiotyki, zapobieganie rakowi żołądka