Clear Sky Science · fr
Un nouveau vaccin multi-épitopes induit une immunité protectrice et thérapeutique contre Helicobacter pylori
Pourquoi cela compte pour la santé quotidienne
La plupart des gens n’entendront jamais le nom Helicobacter pylori, et pourtant cette bactérie en forme de spirale infecte discrètement environ la moitié de la population mondiale et peut provoquer des ulcères gastriques voire un cancer de l’estomac. Aujourd’hui, le seul traitement fiable est une combinaison d’antibiotiques, mais la résistance croissante aux médicaments rend ces traitements moins efficaces. Cette étude décrit un nouveau type de vaccin expérimental qui non seulement prévient l’infection chez la souris, mais élimine aussi des infections gastriques de longue date, ouvrant la voie à un avenir où une simple injection pourrait remplacer des schémas médicamenteux complexes.
Un envahisseur discret de l’estomac
H. pylori est particulièrement adapté pour vivre dans l’acidité sévère de l’estomac et peut y persister pendant des décennies. Nombre de personnes ne développent jamais de symptômes, mais chez d’autres la bactérie déclenche une inflammation chronique, des ulcères douloureux et un risque nettement accru de cancer gastrique. Les thérapies antibiotiques classiques perdent du terrain à mesure que le microbe développe des résistances, et les tentatives vaccinales antérieures ont échoué à plusieurs reprises. Les vaccins précédents utilisaient souvent une seule protéine bactérienne et pouvaient induire de forts taux d’anticorps, mais ils n’ont pas assuré une protection durable lors des essais cliniques. Les chercheurs soupçonnent désormais qu’un contrôle réussi et durable de H. pylori exige une réponse coordonnée à la fois des cellules productrices d’anticorps et des cellules T spécialisées qui dirigent les attaques immunitaires.
Concevoir un vaccin plus malin
Plutôt que d’injecter des protéines bactériennes entières, l’équipe a conçu un vaccin « multi‑épitopes ». Les épitopes sont les fragments clés d’une protéine que le système immunitaire reconnaît réellement. À l’aide d’outils informatiques, les chercheurs ont passé en revue six facteurs de virulence importants de H. pylori — des molécules que la bactérie utilise pour survivre dans l’acide, se déplacer, adhérer aux cellules gastriques et échapper aux défenses. Ils en ont extrait seize courtes régions prévues pour être particulièrement visibles par les cellules B (qui fabriquent les anticorps) et les cellules T (qui orchestrent l’immunité cellulaire). Ils ont assemblé ces morceaux en un seul antigène artificiel appelé Unité Multi‑Épitope, ou MEU, séparés par de courts liens pour aider le système immunitaire à reconnaître chaque élément distinct tout en maintenant la molécule globale stable, non allergène et soluble.
Ajouter un amplificateur immunitaire intégré
Pour s’assurer que le système immunitaire prête attention à cet antigène conçu, les chercheurs l’ont fusionné à des parties clés de la flagelline, une protéine d’une autre bactérie qui active naturellement un récepteur d’alerte nommé TLR5. Ils ont aussi construit une seconde version du vaccin en insérant les instructions du MEU dans un vecteur viral inoffensif appelé Modified Vaccinia Ankara (MVA), reconnu pour induire de fortes réponses des cellules T. Dans des études chez la souris, le MEU a été administré soit comme protéine fusionnée à la flagelline, soit sous forme du vecteur à base de MVA, soit selon un schéma « prime‑boost » combinant les deux formats. Des tests en laboratoire ont confirmé que la protéine de fusion activait la voie TLR5 comme prévu, agissant comme son propre adjuvant, et que le vecteur MVA produisait efficacement l’antigène MEU à l’intérieur des cellules infectées.
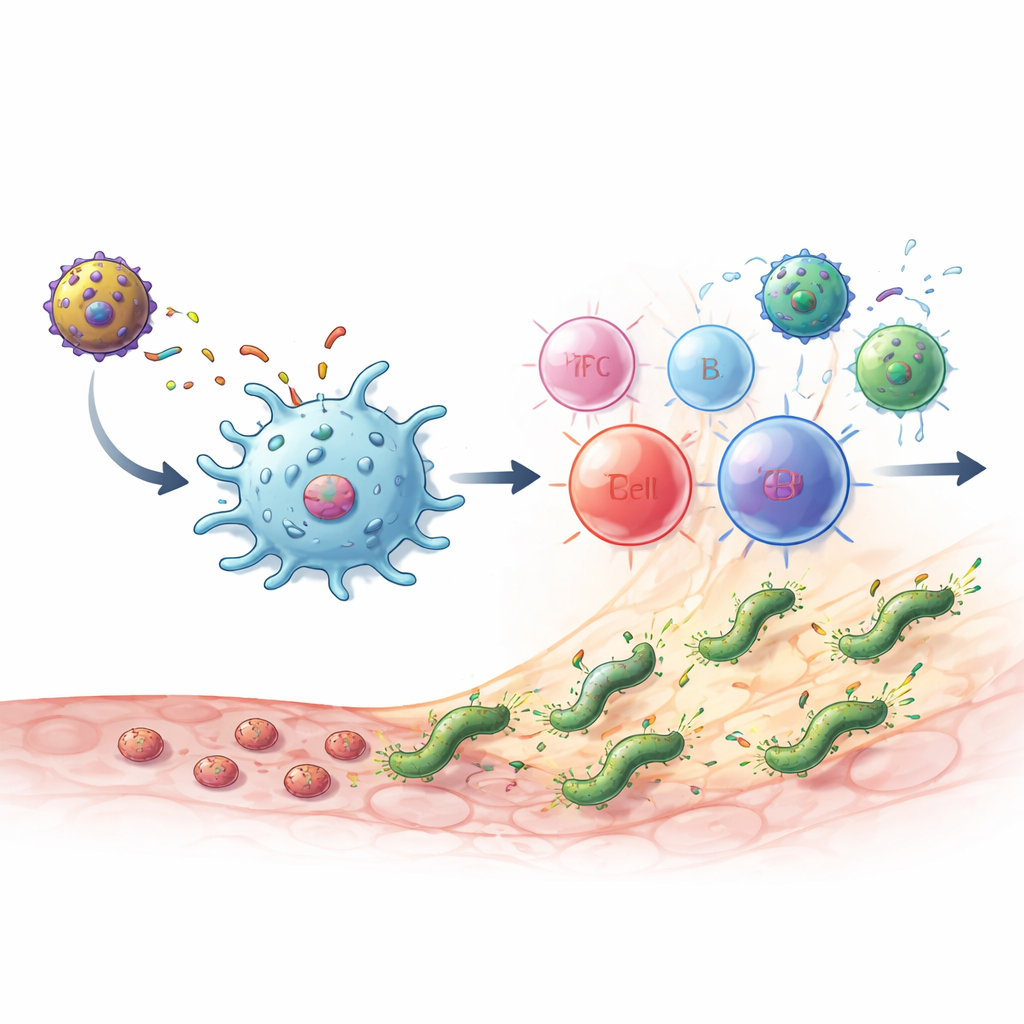
Ce qui s’est passé chez les souris infectées
Lorsque des souris saines ont reçu les vaccins, elles ont généré de forts niveaux d’anticorps spécifiques du MEU ainsi que des cellules T CD4 produisant des messagers clés comme l’IL‑2 et l’interféron‑gamma. La réponse montrait un équilibre sain entre deux grands types de cellules T auxiliaires : l’un associé à la destruction directe des microbes et l’autre soutenant la production d’anticorps et aidant à limiter les lésions tissulaires. Des cellules « relais » importantes reliant l’immunité innée et adaptative, comme des cellules de type NKT, se sont aussi développées. Le schéma le plus efficace était un prime‑boost hétérologue : d’abord la protéine MEU‑flagelline, puis le vecteur MVA‑MEU. Dans les tests préventifs (vaccination avant exposition) comme thérapeutiques (vaccination après établissement d’une infection chronique), soit cette combinaison, soit deux doses de MVA‑MEU ont complètement éliminé la présence détectable de H. pylori dans l’estomac, mesurée par culture et tests génétiques.
Ce que cela pourrait signifier pour les soins futurs
Pour un non‑spécialiste, la conclusion est frappante : dans un modèle murin exigeant, ce vaccin multi‑épitopes soigneusement conçu a non seulement empêché H. pylori de s’installer mais a aussi éliminé des infections enracinées qui imitent une maladie humaine de longue durée. En ciblant simultanément de nombreuses parties bactériennes conservées et en les associant à un puissant activateur immunitaire intégré et à un système d’administration viral, l’approche surmonte les limites qui ont fait échouer des vaccins antérieurs plus simples. Les travaux avancent maintenant vers des études de sécurité chez des animaux de plus grande taille. Si une protection similaire peut être obtenue chez l’humain, cette stratégie pourrait un jour offrir un double avantage contre les ulcères, le cancer gastrique et la résistance aux antibiotiques provoquée par ce germe remarquablement persistant.
Citation: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Mots-clés: Helicobacter pylori, infection gastrique, vaccin multi-épitopes, résistance aux antibiotiques, prévention du cancer gastrique