Clear Sky Science · it
Un nuovo vaccino multi-epitopo induce immunità protettiva e terapeutica contro Helicobacter pylori
Perché questo è importante per la salute quotidiana
La maggior parte delle persone non sentirà mai il nome Helicobacter pylori, eppure questo batterio a forma elicoidale infetta silenziosamente circa la metà della popolazione mondiale e può portare a ulcere gastriche e persino al cancro dello stomaco. Oggi l’unica cura affidabile è una combinazione di antibiotici, ma la crescente resistenza ai farmaci sta rendendo questi trattamenti meno efficaci. Questo studio descrive un nuovo tipo di vaccino sperimentale che non solo previene l’infezione nei topi, ma elimina anche infezioni gastriche di lunga durata, indicando un futuro in cui una semplice iniezione potrebbe sostituire regimi farmacologici complessi.
Un invasore silenzioso dello stomaco
H. pylori è adattato in modo unico a vivere nell’ambiente aspro dello stomaco e può persistere lì per decenni. Molte persone non sviluppano mai sintomi, ma per altre il batterio scatena infiammazione cronica, ulcere dolorose e un rischio notevolmente aumentato di cancro gastrico. Le terapie antibiotiche standard stanno perdendo efficacia man mano che il microbo evolve resistenza, e i tentativi vaccinali passati sono ripetutamente falliti. Vaccini precedenti spesso usavano proteine batteriche singole e potevano indurre forti livelli di anticorpi, ma non sono riusciti a conferire protezione duratura negli studi clinici. I ricercatori ora sospettano che il controllo efficace e a lungo termine di H. pylori richieda una risposta coordinata sia da parte delle cellule produttrici di anticorpi sia da parte di cellule T specializzate che dirigono gli attacchi immunitari.
Progettare un vaccino più intelligente
Invece di iniettare proteine batteriche intere, il team ha progettato un vaccino “multi-epitopo”. Gli epitopi sono i frammenti chiave di una proteina che il sistema immunitario riconosce effettivamente. Usando strumenti informatici, i ricercatori hanno setacciato sei importanti fattori di virulenza di H. pylori—molecole che il batterio utilizza per sopravvivere nell’acido, muoversi, aderire alle cellule gastriche e sfuggire alle difese. Da questi hanno selezionato sedici brevi regioni previste come particolarmente visibili alle cellule B (che producono anticorpi) e alle cellule T (che orchestrano l’immunità cellulare). Hanno concatenato questi pezzi in un unico antigene artificiale chiamato Unità Multi-Epitopo, o MEU, separandoli con brevi linker per aiutare il sistema immunitario a riconoscere ogni frammento chiaramente mantenendo la molecola complessiva stabile, non allergenica e solubile.
Aggiungere un potenziatore immunitario incorporato
Per fare in modo che il sistema immunitario prestasse attenzione a questo antigene ingegnerizzato, i ricercatori lo hanno fuso con parti chiave della flagellina, una proteina di un altro batterio che attiva naturalmente un recettore d’allarme noto come TLR5. Hanno inoltre costruito una seconda versione del vaccino inserendo le istruzioni del MEU in un vettore virale innocuo chiamato Modified Vaccinia Ankara (MVA), noto per indurre forti risposte delle cellule T. Negli studi sui topi, il MEU è stato somministrato come proteina fusa con la flagellina, come vettore a base di MVA, o con uno schema "prime-boost" che combinava entrambi i formati. I test di laboratorio hanno confermato che la proteina di fusione attivava la via TLR5 come previsto, funzionando come suo proprio adiuvante, e che il vettore MVA produceva efficientemente l’antigene MEU all’interno delle cellule infettate.
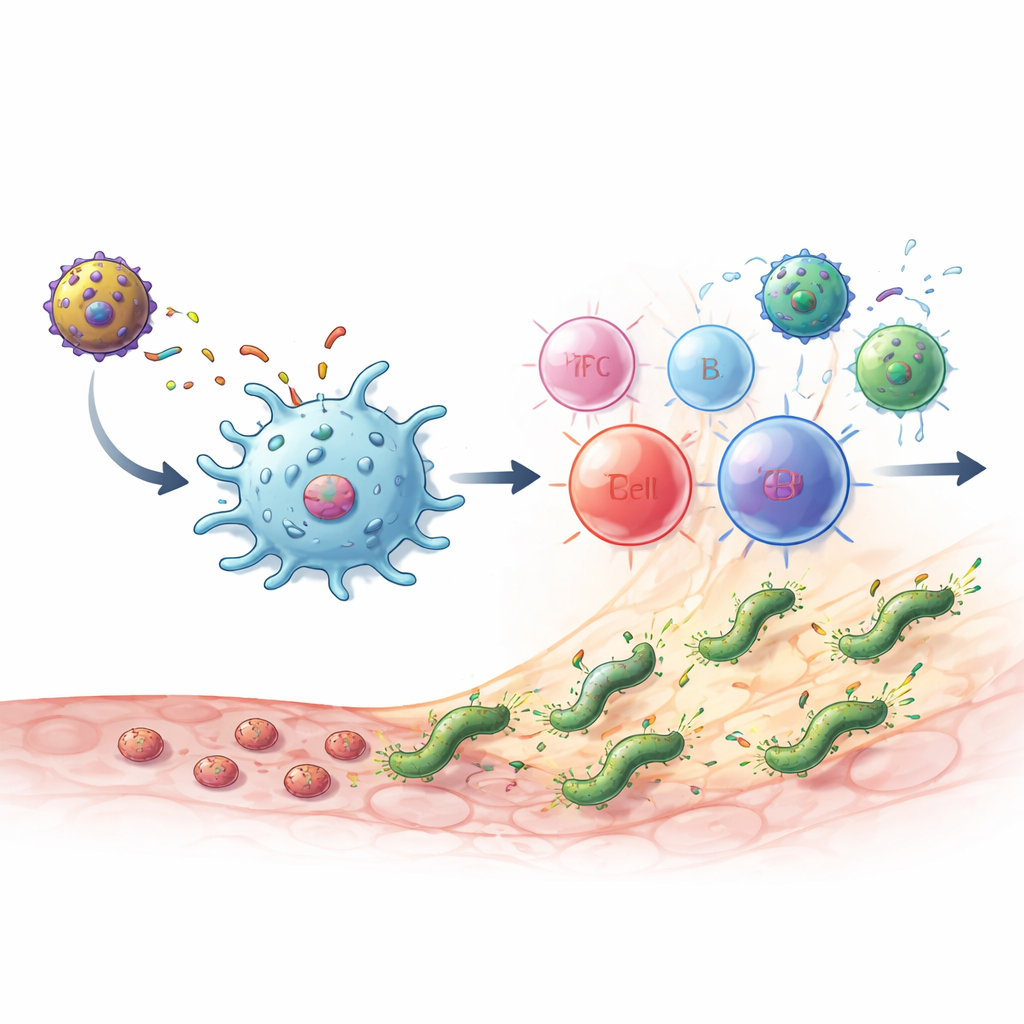
Cosa è successo nei topi infettati
Quando topi sani hanno ricevuto i vaccini, hanno generato alti livelli di anticorpi specifici per il MEU oltre a cellule T CD4 che producevano molecole chiave come IL-2 e interferone-gamma. La risposta ha mostrato un equilibrio sano di due principali tipi di cellule T helper: una legata all’uccisione diretta del microbo e l’altra che sostiene la produzione di anticorpi e aiuta a limitare il danno tissutale. Anche cellule “ponte” importanti che connettono l’immunità innata e adattativa, come le cellule simili alle NKT, sono state ampliate. Lo schema più potente è risultato essere un prime-boost eterologo: prima la proteina MEU-flagellina, poi il vettore MVA-MEU. Sia nei test preventivi (vaccinazione prima dell’esposizione) sia in quelli terapeutici (vaccinazione dopo l’instaurarsi di un’infezione cronica), questa combinazione o due dosi di MVA-MEU hanno eliminato completamente H. pylori rilevabile dallo stomaco, come misurato col colturale e con test genetici.
Cosa potrebbe significare per le cure future
Per un non specialista, la conclusione è notevole: in un modello murino impegnativo, questo vaccino multi-epitopo progettato con cura non solo ha impedito a H. pylori di stabilirsi, ma ha anche eliminato infezioni radicate che imitano la malattia umana a lungo termine. Mirando contemporaneamente a molte parti batteriche conservate e abbinandole a un forte potenziatore immunitario incorporato e a un sistema di veicolazione virale, l’approccio supera i limiti che hanno condannato i vaccini precedenti, più semplici. Il lavoro sta ora passando a studi di sicurezza in animali di taglia maggiore. Se una protezione simile potrà essere ottenuta nelle persone, questa strategia potrebbe un giorno offrire un doppio colpo contro le ulcere, il cancro gastrico e la resistenza agli antibiotici favorita da questo germe straordinariamente persistente.
Citazione: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Parole chiave: Helicobacter pylori, infezione gastrica, vaccino multi-epitopo, resistenza agli antibiotici, prevenzione del cancro gastrico