Clear Sky Science · es
Una vacuna multiepítopo novedosa induce inmunidad protectora y terapéutica contra Helicobacter pylori
Por qué esto importa para la salud cotidiana
La mayoría de las personas nunca escuchará el nombre Helicobacter pylori, y sin embargo esta bacteria en forma de espiral infecta silenciosamente a aproximadamente la mitad de la población mundial y puede causar úlceras gástricas e incluso cáncer de estómago. Hoy en día, la única cura fiable es un cóctel de antibióticos, pero la creciente resistencia a los medicamentos está haciendo que estos tratamientos sean menos eficaces. Este estudio describe un nuevo tipo de vacuna experimental que no solo previene la infección en ratones, sino que también elimina infecciones estomacales de larga duración, lo que apunta a un futuro en el que una simple inyección podría reemplazar regímenes farmacológicos complejos.
Un invasor silencioso del estómago
H. pylori está adaptado de forma única para vivir en el ambiente ácido y hostil del estómago y puede persistir allí durante décadas. Muchas personas nunca desarrollan síntomas, pero en otras la bacteria desencadena inflamación crónica, úlceras dolorosas y un riesgo muy aumentado de cáncer gástrico. Las terapias antibióticas estándar van perdiendo eficacia a medida que el microbio evoluciona resistencia, y los intentos previos de desarrollar vacunas han fracasado repetidamente. Las vacunas anteriores a menudo usaban proteínas bacterianas únicas y podían inducir altos niveles de anticuerpos, pero no lograban protección duradera en ensayos clínicos. Los investigadores sospechan ahora que el control exitoso y a largo plazo de H. pylori requiere una respuesta coordinada de células productoras de anticuerpos y de células T especializadas que dirigen los ataques inmunitarios.
Construyendo una vacuna más inteligente
En vez de inyectar proteínas bacterianas completas, el equipo diseñó una vacuna “multiepítopo”. Los epítopos son los fragmentos clave de una proteína que el sistema inmune reconoce realmente. Usando herramientas informáticas, los investigadores revisaron seis factores de virulencia importantes de H. pylori, moléculas que la bacteria emplea para sobrevivir en el ácido, moverse, adherirse a las células gástricas y evadir las defensas. De estas seleccionaron dieciséis regiones cortas predichas como especialmente visibles para las células B (que producen anticuerpos) y las células T (que orquestan la inmunidad celular). Unieron estas piezas en un único antígeno artificial llamado Unidad Multiepítopo, o MEU, separadas por pequeños conectores para ayudar al sistema inmune a reconocer cada fragmento claramente manteniendo la molécula estable, no alergénica y soluble.
Sumando un potenciador inmune incorporado
Para asegurarse de que el sistema inmune prestara atención a este antígeno diseñado, los investigadores lo fusionaron con partes clave de la flagelina, una proteína de otra bacteria que activa de forma natural un receptor de alarma conocido como TLR5. También construyeron una segunda versión de la vacuna insertando las instrucciones del MEU en un vector viral inofensivo llamado Modified Vaccinia Ankara (MVA), conocido por inducir fuertes respuestas de células T. En estudios en ratones, el MEU se administró bien como proteína fusionada con flagelina, como vector basado en MVA, o en un programa de “prime‑boost” que combinó ambos formatos. Pruebas de laboratorio confirmaron que la proteína de fusión activó la vía TLR5 como se pretendía, actuando como su propio adyuvante, y que el vector MVA produjo eficientemente el antígeno MEU dentro de las células infectadas.
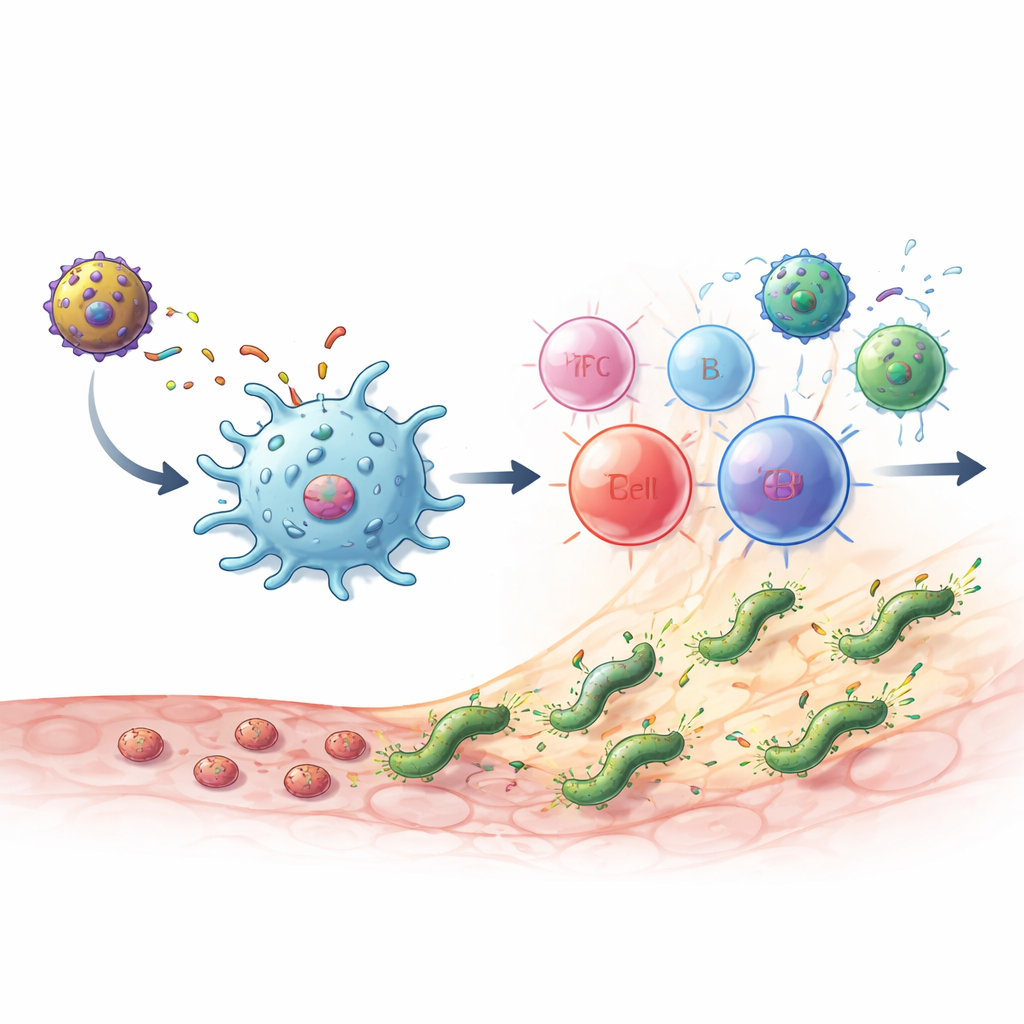
Qué ocurrió en los ratones infectados
Cuando ratones sanos recibieron las vacunas, generaron altos niveles de anticuerpos específicos contra el MEU así como células T CD4 que producían mensajeros clave como IL‑2 e interferón‑gamma. La respuesta mostró un equilibrio sano de dos tipos principales de células T auxiliares: una vinculada a la eliminación directa del microbio y otra que apoya la producción de anticuerpos y ayuda a limitar el daño tisular. También se expandieron células “puente” importantes que conectan la inmunidad innata y adaptativa, como células tipo NKT. El esquema más eficaz fue un prime‑boost heterólogo: primero la proteína MEU‑flagelina y luego el vector MVA‑MEU. En pruebas tanto preventivas (vacunación antes de la exposición) como terapéuticas (vacunación tras establecerse la infección crónica), tanto esta combinación como dos dosis de MVA‑MEU eliminaron por completo la detección de H. pylori en el estómago, según cultivo y pruebas genéticas.
Qué podría significar para la atención futura
Para un no especialista, la conclusión es llamativa: en un modelo de ratón exigente, esta vacuna multiepítopo cuidadosamente diseñada no solo impidió que H. pylori se estableciera, sino que también eliminó infecciones arraigadas que imitan la enfermedad humana de larga duración. Al apuntar simultáneamente a muchas partes bacterianas conservadas y combinarlas con un potente potenciador inmune incorporado y un sistema de administración viral, el enfoque supera limitaciones que hundieron vacunas anteriores, más simples. El trabajo avanza ahora hacia estudios de seguridad en animales de mayor tamaño. Si se logra una protección similar en humanos, esta estrategia podría algún día ofrecer un doble golpe contra las úlceras, el cáncer gástrico y la resistencia a antibióticos impulsada por este germen notablemente persistente.
Cita: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Palabras clave: Helicobacter pylori, infección de estómago, vacuna multiepítopo, resistencia a antibióticos, prevención del cáncer gástrico