Clear Sky Science · ru
Новая многоэпитопная вакцина вызывает защитный и терапевтический иммунитет против Helicobacter pylori
Почему это важно для повседневного здоровья
Большинство людей никогда не слышали название Helicobacter pylori, однако эта спиральная бактерия тихо инфицирует около половины населения Земли и может вызывать язвы желудка и даже рак желудка. В настоящее время единственным надежным лечением является комбинация антибиотиков, но растущая устойчивость к лекарствам снижает их эффективность. В этом исследовании описана новая экспериментальная вакцина, которая не только предотвращает инфицирование у мышей, но и очищает длительно существующие желудочные инфекции, что указывает на будущее, в котором простая прививка может заменить сложные схемы лечения.
Тихий захватчик желудка
H. pylori уникально приспособлен к жизни в агрессивной среде желудочной кислоты и может сохраняться там десятилетиями. У многих людей симптомы не развиваются, но у других бактерия вызывает хроническое воспаление, болезненные язвы и значительно увеличивает риск рака желудка. Стандартные антибиотикотерапии теряют эффективность по мере того, как микроорганизм накапливает устойчивость, а предыдущие попытки создания вакцины неоднократно не давали должного результата. Ранее вакцины часто использовали одиночные бактериальные белки и могли вызывать высокий уровень антител, но не обеспечивали длительной защиты в клинических испытаниях. Исследователи теперь полагают, что успешный долгосрочный контроль H. pylori требует скоординированного ответа как со стороны клеток, продуцирующих антитела, так и специализированных Т-клеток, направляющих иммунные атаки.
Создание более умной вакцины
Вместо введения целых бактериальных белков команда разработала «многоэпитопную» вакцину. Эпитопы — это ключевые фрагменты белка, которые иммунная система действительно распознаёт. С помощью компьютерных инструментов исследователи отобрали шесть важных вирулентных факторов H. pylori — молекул, которые бактерия использует для выживания в кислоте, движения, прикрепления к клеткам желудка и уклонения от защитных механизмов. Из них они выбрали шестнадцать коротких участков, предсказанных как особенно заметные для В-клеток (производящих антитела) и Т-клеток (координирующих клеточный иммунитет). Эти фрагменты были соединены в единый искусственный антиген, названный Многоэпитопной единицей, или MEU, разделённый короткими линкерами, чтобы помочь иммунной системе чётко распознавать каждый кусочек при сохранении общей молекулы стабильной, неаллергенной и растворимой.
Добавление встроенного усилителя иммунного ответа
Чтобы привлечь внимание иммунной системы к этому сконструированному антигену, исследователи слили его с ключевыми участками флагеллина — белка другой бактерии, который естественно активирует рецептор тревоги, известный как TLR5. Они также создали вторую версию вакцины, вставив инструкции MEU в безвредный вирусный вектор Modified Vaccinia Ankara (MVA), известный способностью вызывать сильный Т‑клеточный ответ. В исследованиях на мышах MEU вводили либо как белок, слитый с флагеллином, либо как вектор на основе MVA, либо по схеме «prime‑boost», комбинируя оба формата. Лабораторные тесты подтвердили, что белковый конструкт активирует путь TLR5 как задумано, действуя как собственный адъювант, а вектор MVA эффективно синтезирует антиген MEU внутри инфицированных клеток.
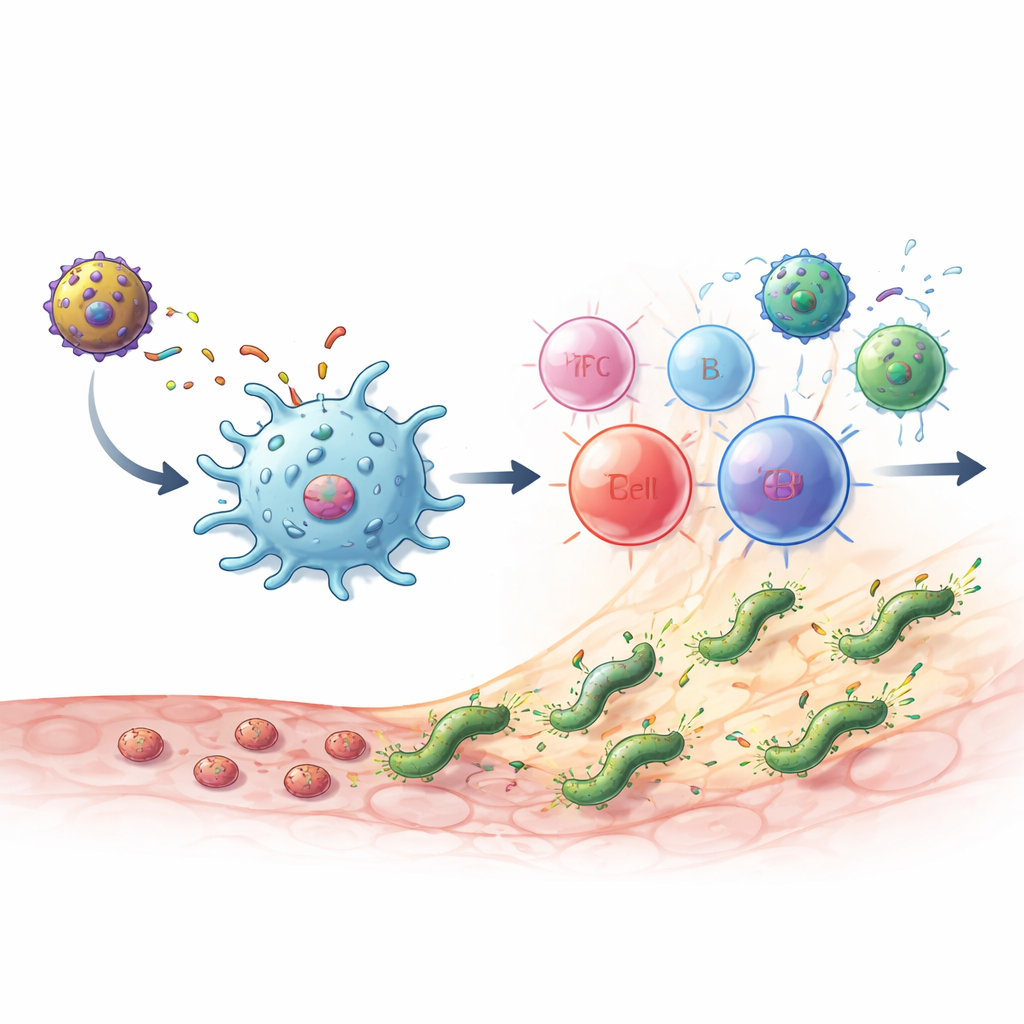
Что произошло у инфицированных мышей
У здоровых мышей, получавших вакцины, формировались высокие уровни антител, специфичных к MEU, а также CD4 Т‑клеток, производивших ключевые мессенджерные молекулы, такие как IL‑2 и интерферон‑гамма. Ответ отличался сбалансированностью двух основных типов помощников Т‑клеток: одного, связанного с прямым уничтожением микроорганизмов, и другого, поддерживающего выработку антител и помогающего ограничивать повреждение тканей. Важные «мостовые» клетки, связывающие врождённый и адаптивный иммунитет, такие как NKT‑похожие клетки, также расширялись. Наиболее эффективной оказалась гетерологичная схема prime‑boost: сначала белок MEU‑флагеллин, затем вектор MVA‑MEU. В профилактических испытаниях (вакцинация до заражения) и в терапевтических тестах (вакцинация после установления хронической инфекции) либо эта комбинация, либо две дозы MVA‑MEU полностью устраняли обнаруживаемый H. pylori из желудка по данным культивирования и генетических тестов.
Что это может означать для будущей медицины
Для неспециалиста главный вывод впечатляет: в требовательной модельной системе на мышах эта тщательно разработанная многоэпитопная вакцина не только препятствовала закреплению H. pylori, но и устраняла укоренившиеся инфекции, имитирующие длительное заболевание у людей. За счёт нацеливания сразу на многие консервативные участки бактерии и сочетания их с мощным встроенным усилителем иммунитета и вирусной системой доставки подход преодолевает ограничения, которыми грешили более ранние, простые вакцины. Работа сейчас переходит к исследованиям безопасности на крупных животных. Если аналогичная защита будет достигнута у людей, эта стратегия однажды может предложить двойной удар против язв, рака желудка и антибиотикорезистентности, вызванной этим поразительно устойчивым микроорганизмом.
Цитирование: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Ключевые слова: Helicobacter pylori, инфекция желудка, многоэпитопная вакцина, антибиотикорезистентность, профилактика рака желудка