Clear Sky Science · pt
Uma nova vacina multiepítopo induz imunidade protetora e terapêutica contra Helicobacter pylori
Por que isso importa para a saúde cotidiana
A maioria das pessoas nunca ouvirá o nome Helicobacter pylori, e ainda assim essa bactéria em forma de espiral infecta discretamente cerca de metade da população mundial e pode levar a úlceras estomacais e até câncer gástrico. Hoje, a única cura confiável é um coquetel de antibióticos, mas a crescente resistência aos medicamentos vem tornando esses tratamentos menos eficazes. Este estudo descreve um novo tipo de vacina experimental que não só previne a infecção em camundongos, como também elimina infecções estomacais de longa duração, apontando para um futuro em que uma simples injeção poderia substituir regimes complexos de medicamentos.
Um invasor silencioso do estômago
H. pylori é singularmente adaptado para viver no ambiente ácido e agressivo do estômago e pode persistir ali por décadas. Muitas pessoas nunca desenvolvem sintomas, mas para outras a bactéria desencadeia inflamação crônica, úlceras dolorosas e um risco muito maior de câncer gástrico. Terapias antibióticas padrão estão perdendo eficácia à medida que o microrganismo evolui resistência, e tentativas anteriores de vacinas repetidamente fracassaram. Vacinas anteriores frequentemente usavam proteínas bacterianas isoladas e podiam elevar fortemente os níveis de anticorpos, porém falharam em proporcionar proteção duradoura em ensaios clínicos. Pesquisadores agora suspeitam que o controle bem‑sucedido e de longo prazo de H. pylori requer uma resposta coordenada tanto de células produtoras de anticorpos quanto de células T especializadas que dirigem ataques imunológicos.
Construindo uma vacina mais inteligente
Em vez de injetar proteínas bacterianas inteiras, a equipe projetou uma vacina “multiepítopo”. Epítopos são os fragmentos chave de uma proteína que o sistema imunológico realmente reconhece. Usando ferramentas computacionais, os pesquisadores vasculharam seis fatores de virulência importantes de H. pylori — moléculas que a bactéria usa para sobreviver ao ácido, mover‑se, aderir às células do estômago e escapar das defesas. Desses, selecionaram dezesseis regiões curtas previstas como especialmente visíveis para células B (que produzem anticorpos) e células T (que orquestram a imunidade celular). Eles uniram essas peças em um único antígeno artificial chamado Unidade Multi‑Epítopo, ou MEU, separados por pequenos conectores para ajudar o sistema imunológico a reconhecer cada pedaço claramente, mantendo a molécula global estável, não alergênica e solúvel.
Adicionando um potenciador imune embutido
Para garantir que o sistema imunológico prestasse atenção a esse antígeno projetado, os pesquisadores o fundiram com partes-chave da flagelina, uma proteína de outra bactéria que naturalmente ativa um receptor de alarme conhecido como TLR5. Eles também construíram uma segunda versão da vacina inserindo as instruções do MEU em um vetor viral inofensivo chamado Modified Vaccinia Ankara (MVA), reconhecido por induzir fortes respostas de células T. Em estudos com camundongos, o MEU foi administrado ora como proteína fundida à flagelina, ora como vetor baseado em MVA, ou em um cronograma “prime‑boost” que combinou ambos os formatos. Testes laboratoriais confirmaram que a proteína de fusão ativou a via TLR5 conforme esperado, atuando como seu próprio adjuvante, e que o vetor MVA produziu eficientemente o antígeno MEU dentro das células infectadas.
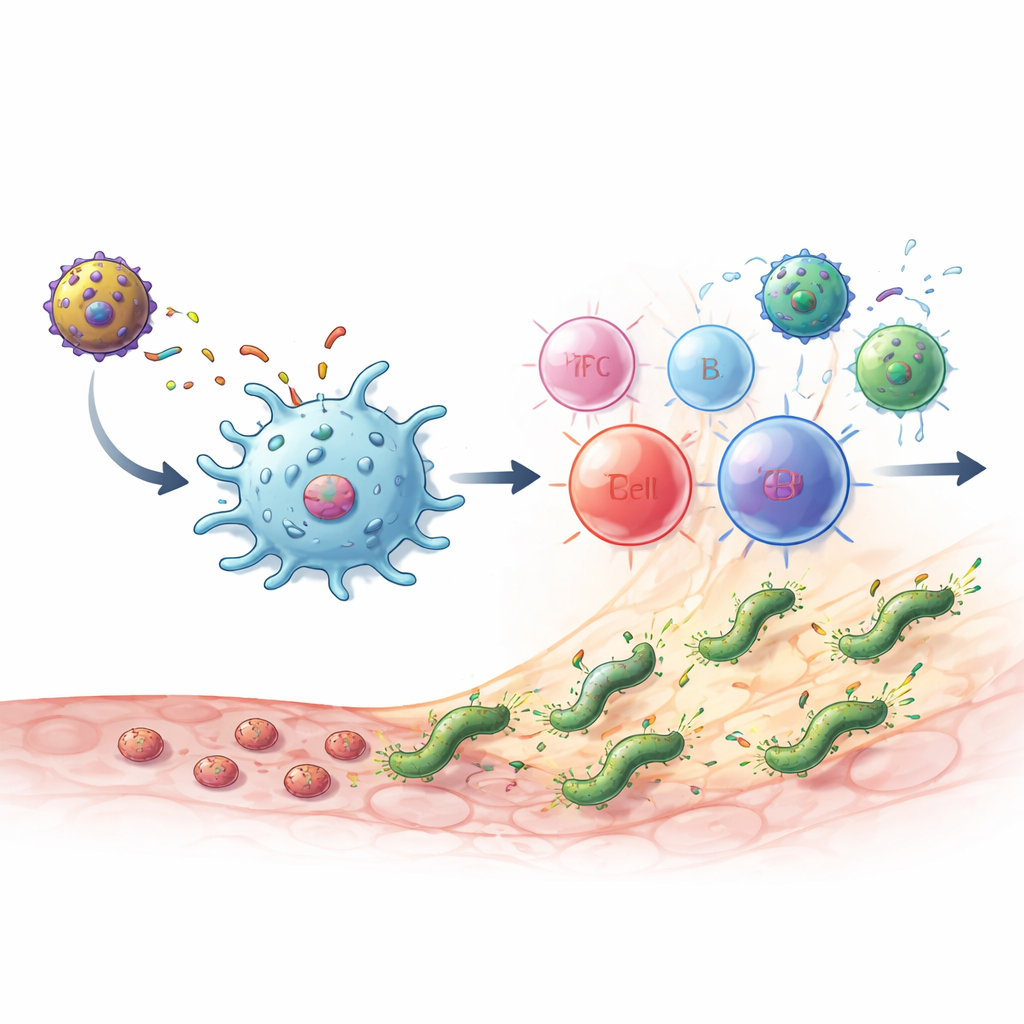
O que ocorreu em camundongos infectados
Quando camundongos saudáveis receberam as vacinas, eles geraram altos níveis de anticorpos específicos para o MEU, bem como células T CD4 que produziram moléculas mensageiras chave como IL‑2 e interferon‑gama. A resposta mostrou um equilíbrio saudável entre dois grandes tipos de células T helper: uma associada à destruição direta do microrganismo e outra que sustenta a produção de anticorpos e ajuda a limitar o dano tecidual. Células importantes de “ponte” que conectam a imunidade inata e adaptativa, como células do tipo NKT, também foram expandidas. O esquema mais potente foi o prime‑boost heterólogo: primeiro a proteína MEU‑flagelina, depois o vetor MVA‑MEU. Tanto em testes preventivos (vacinação antes da exposição) quanto em testes terapêuticos (vacinação após estabelecimento de infecção crônica), essa combinação ou duas doses de MVA‑MEU eliminaram completamente a detecção de H. pylori do estômago, conforme medido por cultura e testes genéticos.
O que isso pode significar para os cuidados futuros
Para um não especialista, a conclusão é marcante: em um modelo exigente em camundongos, essa vacina multiepítopo cuidadosamente projetada não apenas impediu que H. pylori se estabelecesse, mas também eliminou infecções entrincheiradas que imitam a doença humana de longa duração. Ao mirar muitas partes bacterianas conservadas simultaneamente e combiná‑las com um potente potenciador imune embutido e um sistema de entrega viral, a abordagem supera limitações que derrubaram vacinas anteriores e mais simples. O trabalho agora avança para estudos de segurança em animais maiores. Se proteção similar puder ser alcançada em pessoas, essa estratégia pode um dia oferecer um golpe duplo contra úlceras, câncer gástrico e a resistência a antibióticos impulsionada por esse germe notavelmente persistente.
Citação: Moeini, H., Mostafazadeh, A., Schoenemann, L. et al. A novel multi-epitope vaccine induces protective and therapeutic immunity against Helicobacter pylori. npj Vaccines 11, 69 (2026). https://doi.org/10.1038/s41541-026-01409-9
Palavras-chave: Helicobacter pylori, infecção estomacal, vacina multiepítopo, resistência a antibióticos, prevenção do câncer gástrico