Clear Sky Science · tr
Kortikal ve bazal gangliyon beta osilasyonları ile frekans-bağımlı DBS etkileri: A53T Parkinson hastalığı sıçan modelinde
Bu beyin ritmi çalışması neden önemli
Parkinson hastalığı titreme ve hareketlerde yavaşlama ile bilinir; ancak beynin derinliklerinde anormal “beta” ritimleri, bir tür elektriksel arka plan vuruşu olarak da öne çıkar. Cerrahlar belirli beyin bölgelerine atımlar gönderen, bir nevi pil benzeri terapi olan derin beyin stimülasyonu ile semptomları hafifletebiliyor. Yine de bu faydanın ne ölçüde beta ritimlerinin susturulmasından kaynaklandığı ve hangi stimülasyon desenlerinin en etkili olduğu belirsiz kaldı. Bu çalışma, insan Parkinson’una yakın bir sıçan modeli kullanarak bu ritimlerin nasıl ortaya çıktığını izliyor ve farklı stimülasyon türlerinin bunları nasıl şekillendirdiğini test ederek gelecekteki beyin terapilerinin rafine edilmesine yönelik ipuçları sunuyor.
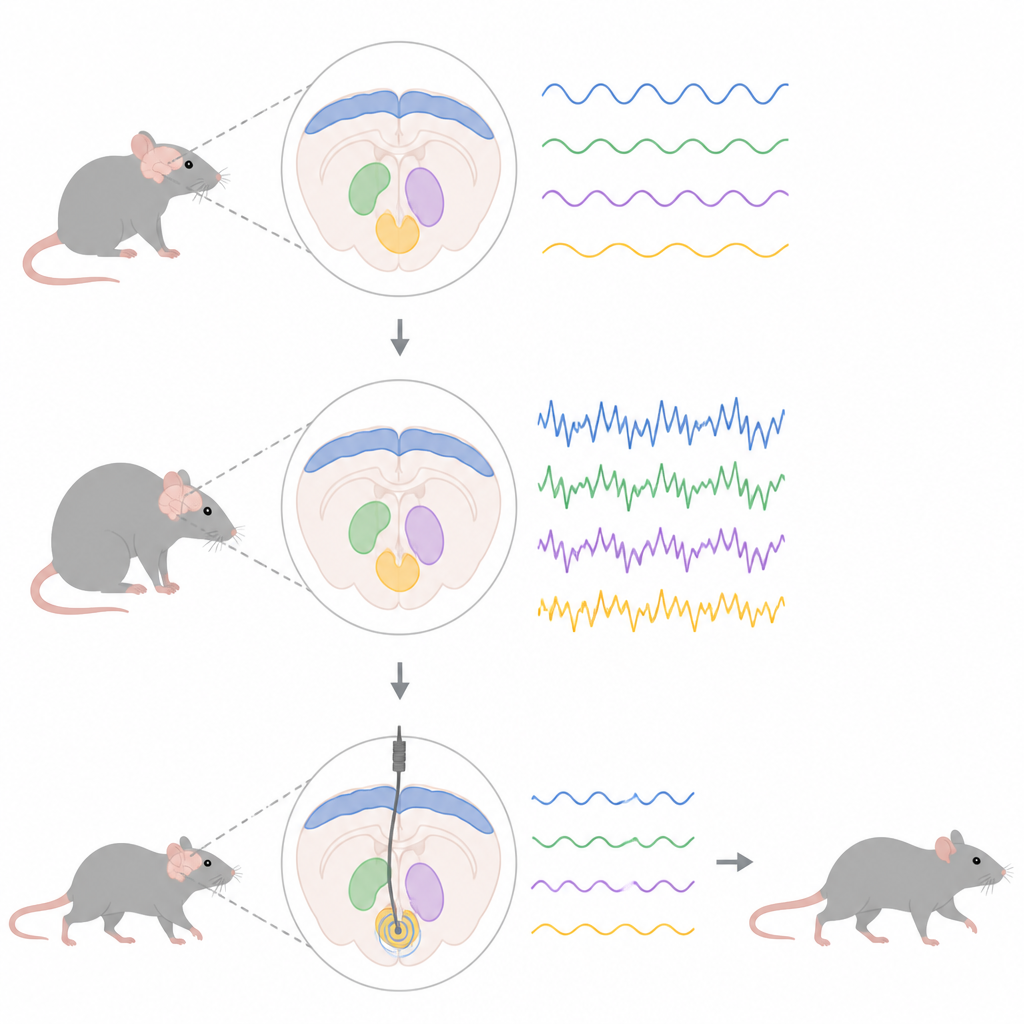
Görünmeyen beynin vuruşunu izlemek
Araştırmacılar, sıçanlarda alfa-sinüklein proteininin mutasyona uğramış bir formunun aşırı üretilmesini sağlayan genetik bir yöntem kullandı; aynı protein Parkinson hastalarında birikiyor. Bu süreç orta beyinlerde dopamin üreten hücrelerin zamanla yok olmasına yol açtı ve korteksten subthalamik çekirdek ile entopedunküler çekirdeğe kadar uzanan daha geniş bir hareket ağında değişiklikleri tetikledi; entopedunküler çekirdek sıçanda insanlardaki önemli bir çıkış merkezinin eşdeğeridir. Bu bölgelere ince elektrotlar yerleştirerek ekip, çok sayıda sinir hücresinin birleşik elektriksel aktivitesini yansıtan lokal saha potansiyellerini izledi ve özellikle 13–30 döngü/saniye arasındaki beta aralığına odaklandı.
Sistematik olarak yayılan sağlıksız ritimler
Hafif anestezi altında yapılan kayıtlar, anormal beta aktivitesinin her yerde aynı anda ortaya çıkmadığını gösterdi. Hastalık sürecinin erken döneminde, dopamin kaybı hâlâ sınırlıyken bile motor kortekste ekstra beta gücü zaten görünüyordu; motor korteks hareketleri planlamaya ve başlatmaya yardımcı olan dış tabakadır. Daha sonra, daha fazla dopamin hücresi öldüğünde güçlü beta ritimleri subthalamik ve entopedunküler çekirdeklerde ortaya çıktı. Hastalık proteini bulunan sıçanlarda, bu derin bölgelerdeki sinir hücrelerinin ateşleme biçimleri de değişti: entopedunküler çekirdek hücreleri daha hızlı ve patlamalı (burst) ateşlemeye başladı; subthalamik hücreler ise ilerleyen aşamalarda ortalama ateşleme hızlarında büyük bir değişim olmasa bile daha düzensiz, patlamalı desenler geliştirdi.
Düzgün hareketi engelleyen patlamalar
Bu sinyallerin doğal davranış sırasında nasıl davrandığını görmek için ekip kayıtları uyanık ve serbestçe hareket eden sıçanlarda tekrarladı. Sürekli bir uğultu yerine beta aktivitesi kısa patlamalar (burst) halinde ortaya çıktı. Parkinson benzeri değişiklikleri olan sıçanlarda patlamalar daha uzun sürdü, daha sık meydana geldi ve kontrol hayvanlarına göre toplam zamanda daha fazla yer kapladı. Subthalamik çekirdekte daha güçlü beta aktivitesi daha az hareketle ilişkiliydi; bu, beta patlamalarının eylemleri başlatma ve kontrol etmede zorlukla bağlantılı olduğu Parkinson’lu insanlara ait gözlemlerle örtüşüyor. Bu desenler, hastalığın hareketleri nasıl bozduğunda sadece genel beta gücünden ziyade patlamaların zamanlaması ve şeklinin önemli olduğunu öne sürüyor.
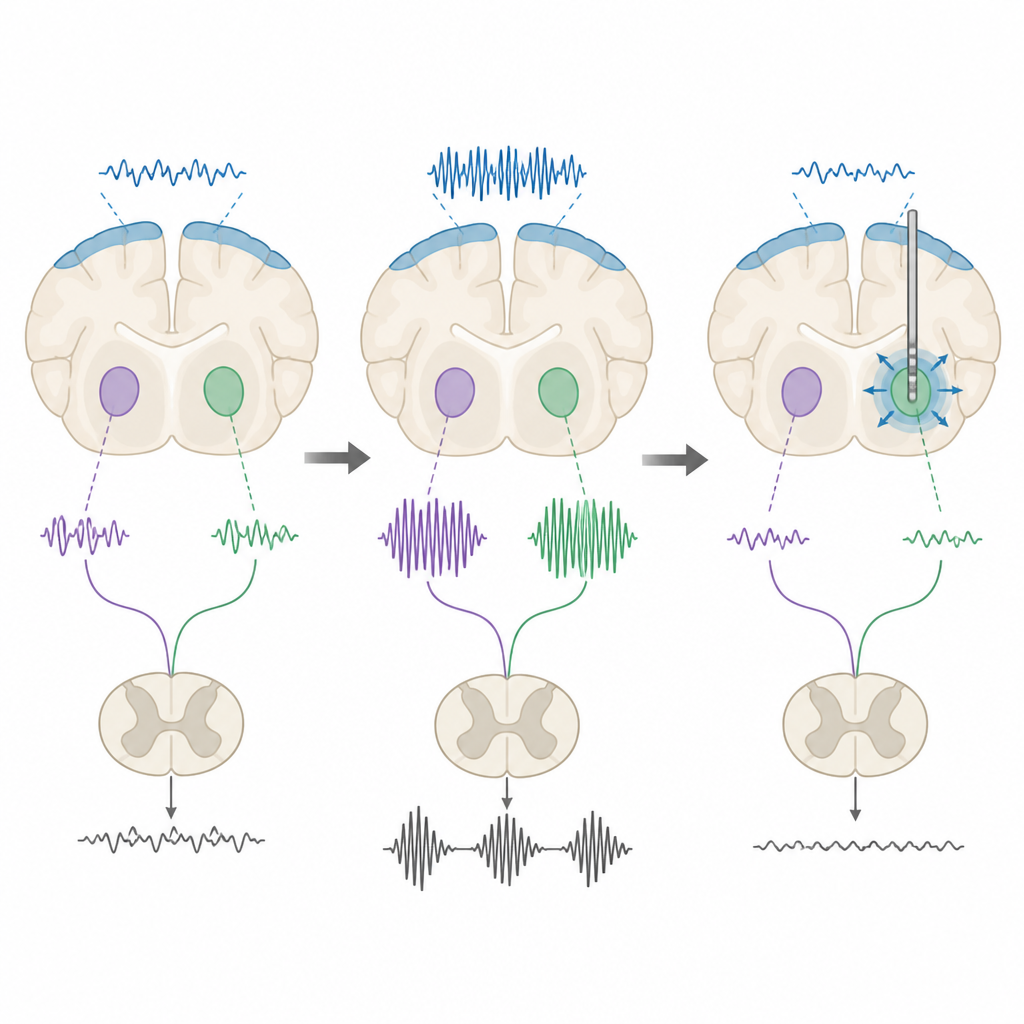
Beyin stimülasyonu desenlerinin test edilmesi
Araştırmacılar daha sonra derin beyin stimülasyonunun bu ritimleri ayarlayıp ayarlayamayacağını sınadı. Subthalamik ve entopedunküler çekirdeklere hem düşük frekanslı hem de yüksek frekanslı elektriksel atımlar uyguladılar. Anestezi altında, her iki tür stimülasyon da hastalıklı değişiklikleri olan sıçanlarda genel beta gücünü azalttı; sağlıklı kontrollerde ise bu etki görülmedi; bu da anormal ritimlerin stimülasyona özellikle duyarlı olduğunu gösteriyor. Uyanık sıçanlarda daha nüanslı bir tablo ortaya çıktı. Yüksek frekanslı stimülasyon genellikle beta patlamalarını kısalttı veya sinyalin yüksek-beta durumunda geçirdiği zamanı azalttı; düşük frekanslı stimülasyon ise çoğu zaman ters etki yaparak patlamaları uzattı veya toplam sürelerini artırdı. Ekip bir ızgara-yürüme testinde hareketi ölçtüğünde, yalnızca entopedunküler çekirdeğin yüksek frekanslı stimülasyonu sıçanların adım doğruluğunu iyileştirdi.
Gelecekteki tedavi için ne anlama geliyor
Birlikte ele alındığında bulgular, bu sıçan modelinin Parkinson hastalarında görülen aynı tür beta patlamalarını ve ateşleme düzensizliklerini güvenilir şekilde geliştirdiğini ve derin beyin stimülasyonuna frekans-bağımlı olarak yanıt verdiğini gösteriyor. Uzun, bozucu beta patlamalarını parçalamak ve daha düzgün hareketi desteklemek için yüksek frekanslı atımlar düşük frekanslılara göre daha uygun görünüyor. Anormal ritimlerin hareket ağı boyunca nasıl ortaya çıktığını ve farklı stimülasyon ayarlarının bunları nasıl yeniden biçimlendirdiğini haritalayarak bu çalışma, beyin bölgelerini sadece susturmaktan öte elektriksel zamanlamalarını yeniden ayarlamayı amaçlayan gelecekteki stratejiler için güçlü bir test ortamı sağlıyor.
Atıf: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Anahtar kelimeler: Parkinson hastalığı, beta osilasyonları, derin beyin stimülasyonu, bazal gangliyon, sıçan modeli