Clear Sky Science · de
Kortikale und Basalganglien-Beta-Oszillationen und frequenzabhängige DBS-Effekte im A53T-Parkinson-Rattenmodell
Warum diese Studie zu Gehirnrhythmen wichtig ist
Parkinson-Krankheit ist vor allem für Tremor und verlangsamte Bewegung bekannt, doch tief im Gehirn zeichnet sie sich auch durch abnorme „Beta“-Rhythmen aus, eine Art elektrischer Hintergrundtakt. Chirurgen können Symptome mit tiefer Hirnstimulation lindern, einer pacemakerähnlichen Therapie, die Impulse an bestimmte Hirnregionen liefert. Unklar blieb jedoch, wie stark dieser Nutzen darauf zurückzuführen ist, jene Beta-Rhythmen zu dämpfen, und welche Stimulationsmuster am besten wirken. Diese Studie nutzt ein Rattenmodell, das die menschliche Parkinson-Krankheit eng nachbildet, um das Auftreten dieser Rhythmen zu beobachten und zu testen, wie verschiedene Stimulationsarten sie formen — Hinweise, die künftige Hirntherapien verfeinern könnten.
Dem verborgenen Takt des Gehirns folgen
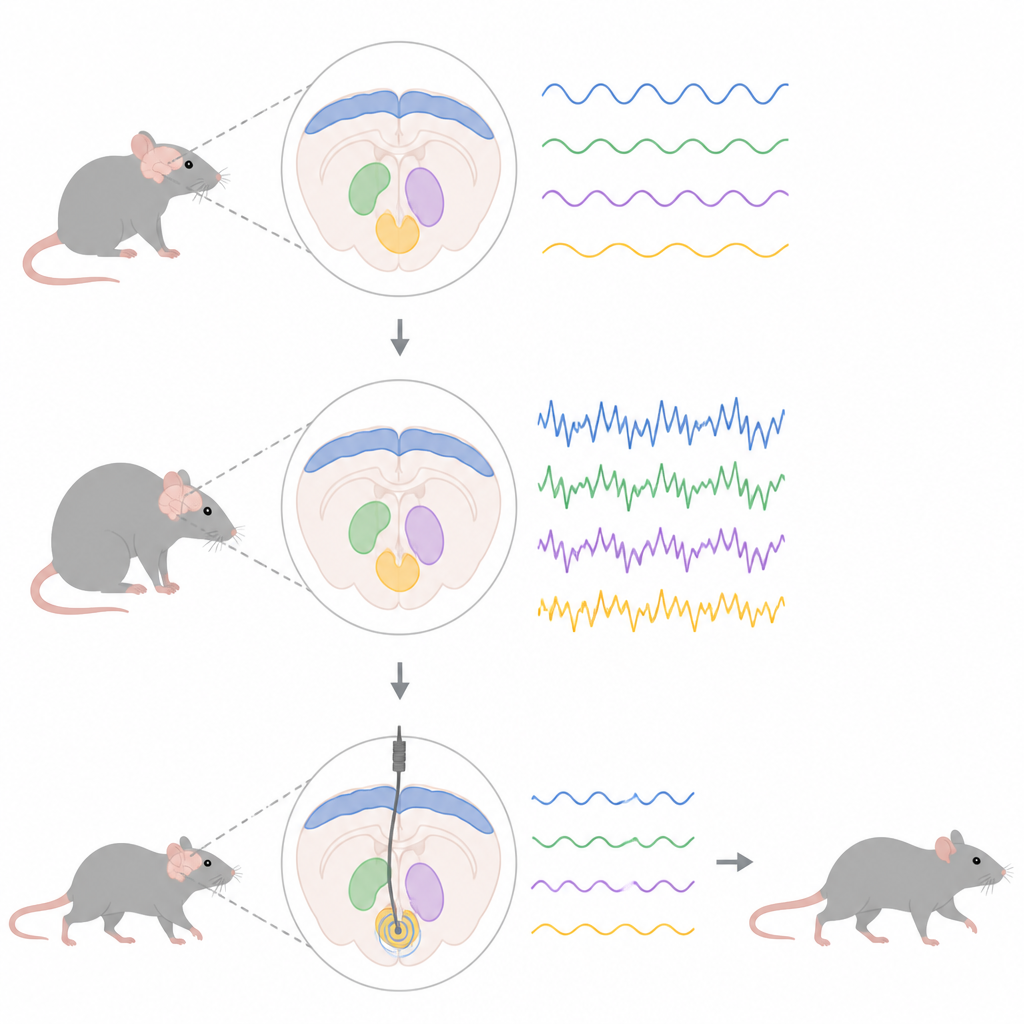
Die Forschenden nutzten einen genetischen Trick, um Ratten die Produktion einer mutierten Form von Alpha-Synuklein zu erhöhen, desselben Proteins, das sich bei vielen Menschen mit Parkinson anreichert. Dies führte allmählich zum Absterben dopaminproduzierender Zellen im Mittelhirn und löste Veränderungen in einem größeren Bewegungsnetzwerk aus, das die äußere Hirnrinde mit tiefen Strukturen verbindet, den subthalamischen und dem entopedunkulären Nukleus, dem Rattengegenstück zu einem wichtigen humanen Ausgangsknoten. Durch das Einsetzen feiner Elektroden in diese Bereiche verfolgte das Team lokale Feldpotenziale, die kombinierte elektrische Aktivität vieler Nervenzellen, mit Fokus auf Aktivität im Beta-Bereich zwischen 13 und 30 Zyklen pro Sekunde.
Stufenweiser Ausbreitung ungesunder Rhythmen
Aufnahmen unter leichter Anästhesie zeigten, dass abnorme Beta-Aktivität nicht überall gleichzeitig auftrat. Früh im Krankheitsverlauf, als der Dopaminverlust noch moderat war, war erhöhte Beta-Leistung bereits im motorischen Kortex sichtbar, der äußeren Schicht, die bei der Planung und Initiierung von Bewegungen hilft. Erst später, als mehr Dopaminzellen zugrunde gingen, traten starke Beta-Rhythmen im subthalamischen und entopedunkulären Nukleus auf. In Ratten mit dem Krankheitsprotein veränderten sich zudem die Feuermuster der Nervenzellen in diesen tiefen Regionen: Zellen im entopedunkulären Nukleus begannen schneller und in Bursts zu feuern, während subthalamische Zellen später unregelmäßigere, burstartige Muster entwickelten, selbst ohne große Veränderung ihrer durchschnittlichen Feuerrate.
Bursts, die flüssige Bewegung blockieren
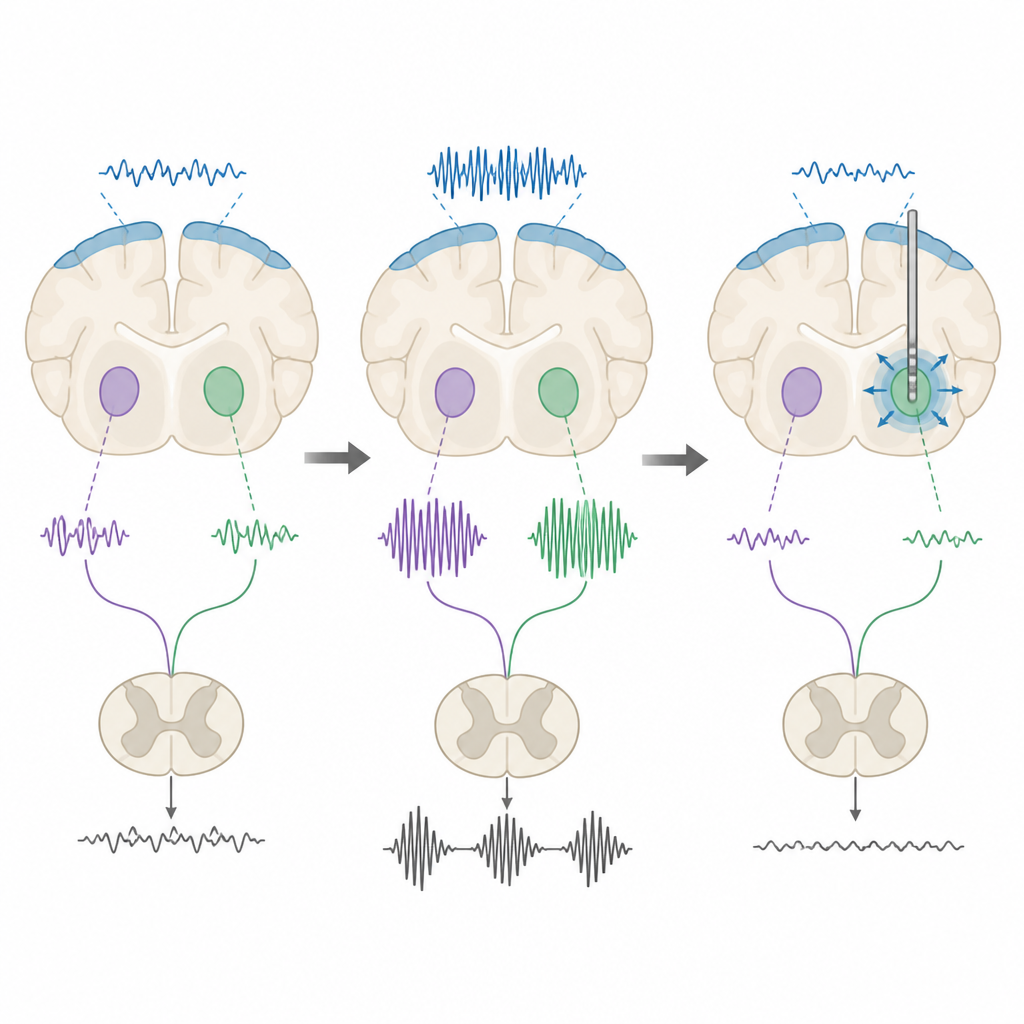
Um zu sehen, wie sich diese Signale bei natürlichem Verhalten verhalten, wiederholte das Team die Aufnahmen bei wachen, sich frei bewegenden Ratten. Statt eines gleichmäßigen Summens trat Beta-Aktivität als kurze Bursts auf. Ratten mit den Parkinson-ähnlichen Veränderungen zeigten Bursts, die länger dauerten, häufiger auftraten und insgesamt mehr Zeit einnahmen als bei Kontrolltieren. Im subthalamischen Nukleus ging stärkere Beta-Aktivität mit weniger Bewegung einher, was Beobachtungen beim Menschen mit Parkinson widerspiegelt, bei denen Beta-Bursts mit Schwierigkeiten beim Initiieren und Kontrollieren von Aktionen verbunden sind. Diese Muster deuten darauf hin, dass Zeitpunkt und Form der Bursts — nicht nur die Gesamtstärke des Beta-Signals — entscheidend dafür sind, wie die Krankheit die Bewegung stört.
Testen von Stimulationsmustern
Die Forschenden testeten anschließend, ob tiefe Hirnstimulation diese Rhythmen abstimmen kann. Sie setzten sowohl niederfrequente als auch hochfrequente elektrische Pulse an den subthalamischen und den entopedunkulären Nukleus. Unter Anästhesie reduzierten beide Stimulationsarten die gesamte Beta-Leistung bei Ratten mit den Krankheitsveränderungen, nicht jedoch bei gesunden Kontrollen, was zeigt, dass die abnormen Rhythmen besonders empfindlich gegenüber Stimulation sind. Bei wachen Ratten ergab sich ein nuancierteres Bild. Hochfrequente Stimulation verkürzte tendenziell Beta-Bursts oder verringerte die Zeit, die das Signal in einem Hoch-Beta-Zustand verbrachte, während niederfrequente Stimulation häufig das Gegenteil bewirkte, Bursts verlängerte oder ihre Gesamtdauer erhöhte. In einem Gitterlauf-Test verbesserte nur die hochfrequente Stimulation des entopedunkulären Nukleus die Schrittkontrolle der Ratten.
Was das für künftige Behandlungen bedeutet
Zusammen genommen zeigen die Ergebnisse, dass dieses Rattenmodell zuverlässig die gleichen Arten von Beta-Bursts und Feuerrhythmusstörungen entwickelt, die beim Menschen mit Parkinson beobachtet werden, und dass es frequenzabhängig auf tiefe Hirnstimulation reagiert. Hochfrequente Pulse scheinen besser geeignet zu sein, lange, störende Beta-Bursts aufzubrechen und flüssigere Bewegung zu unterstützen als niederfrequente. Indem beschrieben wird, wie abnorme Rhythmen im Bewegungsnetzwerk entstehen und wie verschiedene Stimulationsparameter sie umformen, bietet diese Arbeit ein leistungsfähiges Testfeld für künftige Strategien, die nicht nur Hirnregionen „abschalten“, sondern deren elektrische Zeitstruktur neu abstimmen wollen, um Parkinson-Symptome besser zu kontrollieren.
Zitation: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Schlüsselwörter: Parkinson-Krankheit, Beta-Oszillationen, Tiefe Hirnstimulation, Basalganglien, Rattenmodell