Clear Sky Science · ru
Бета-осцилляции коры и базальных ганглиев и частотно‑зависимые эффекты ГМСТ в модели болезни Паркинсона A53T у крыс
Почему это исследование ритмов мозга важно
Болезнь Паркинсона прежде всего известна тремором и замедлением движений, но глубоко в мозге она также характеризуется аномальными «бета» ритмами — электрическим фоном с определённым ритмом. Хирурги могут смягчать симптомы с помощью глубокой стимуляции мозга, терапии-пейсмейкера, посылающей импульсы в определённые области. Тем не менее было не до конца ясно, насколько польза связана с подавлением этих бета‑ритмов и какие режимы стимуляции работают лучше. В этом исследовании использована крысиная модель, тесно имитирующая человеческий Паркинсон, чтобы наблюдать возникновение этих ритмов и проверить, как разные типы стимуляции их меняют — давая подсказки, которые могут помочь уточнить будущие мозговые терапии.
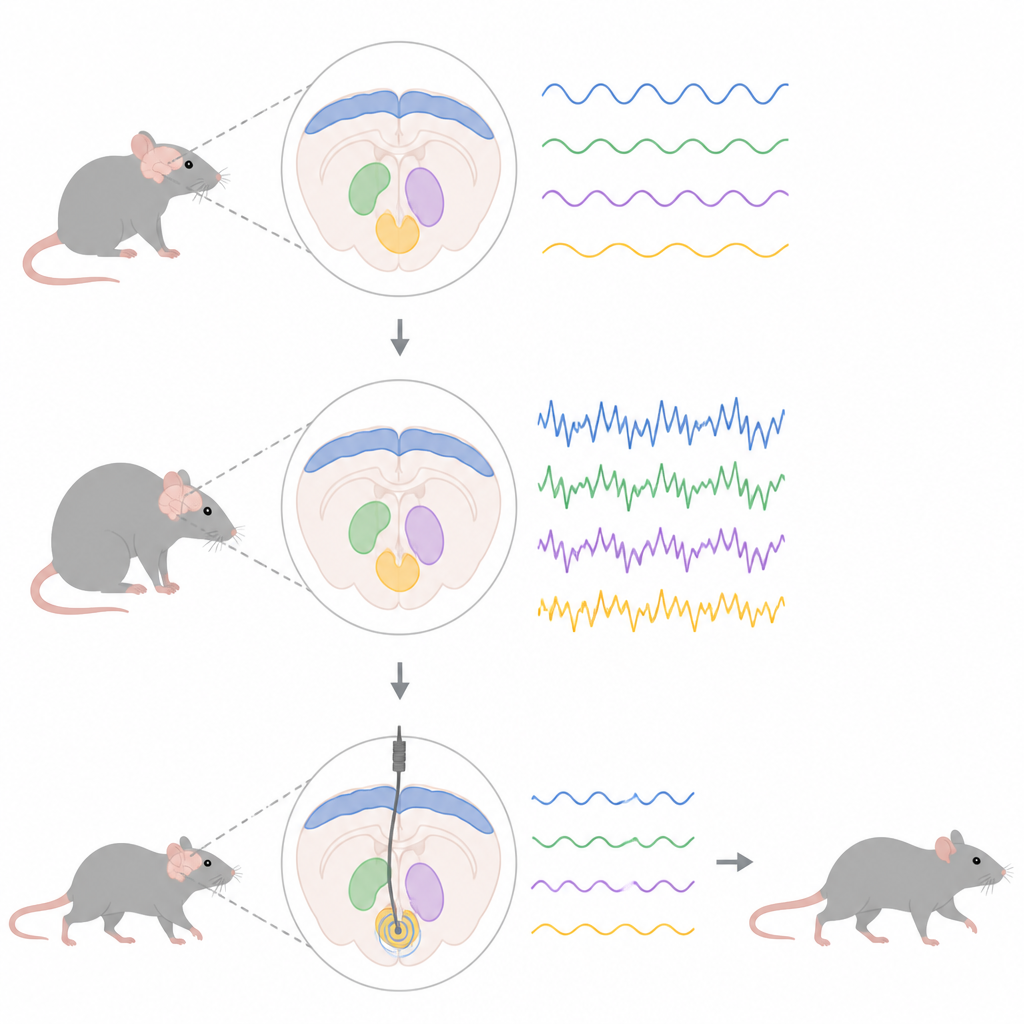
Отслеживание скрытого ритма мозга
Исследователи использовали генетический приём, чтобы заставить крыс перепроизводить мутантную форму альфа‑синуклеина — тот же белок, который накапливается у многих людей с болезнью Паркинсона. Это постепенно уничтожало клетки, продуцирующие дофамин в среднем мозге, вызывая изменения в более широкой моторной сети, соединяющей кору с глубокими структурами: субталамическим и энтопедунклярным ядрами, которые у крыс эквивалентны ключевому выходному узлу у человека. Поместив тонкие электроды в эти области, команда регистрировала локальные поле‑потенциалы — суммарную электрическую активность множества нервных клеток, — сосредоточившись на активности в бета‑диапазоне от 13 до 30 циклов в секунду.
Пошаговое распространение нездоровых ритмов
Записи под лёгким наркозом показали, что аномальная бета‑активность появлялась не везде одновременно. Ранней в процессе болезни, когда потеря дофамина была ещё небольшой, повышенная бета‑мощность уже наблюдалась в моторной коре — внешнем слое, который помогает планировать и запускать движения. Лишь позднее, по мере гибели большего числа дофаминовых клеток, в субталамическом и энтопедунклярном ядрах сформировались выраженные бета‑ритмы. У крыс с патологическим белком нервные клетки в этих глубоких областях также изменили свои свойства спайкинга: клетки в энтопедунклярном ядре начали чаще и пачками стрелять, тогда как субталамические клетки на более поздних стадиях приобрели более нерегулярные, всплескообразные паттерны, даже без большой смены их средней частоты разрядов.
Всплески, мешающие плавному движению
Чтобы посмотреть, как эти сигналы ведут себя при естественном поведении, команда повторила записи у бодрствующих крыс, свободно двигающихся по клетчатой площадке. Вместо ровного фона бета‑активность проявлялась в виде коротких всплесков. У крыс с паркинсоническими изменениями всплески были длиннее, случались чаще и в сумме занимали больше времени, чем у контрольных животных. В субталамическом ядре усиление бета‑активности шло вразрез с движением: чем сильнее бета, тем меньше движение — что созвучно наблюдениям у людей с Паркинсоном, где бета‑всплески связаны с трудностями в запуске и контроле действий. Эти паттерны указывают, что важна не только общая сила бета‑активности, но и временная структура и форма всплесков для того, как болезнь нарушает движение.
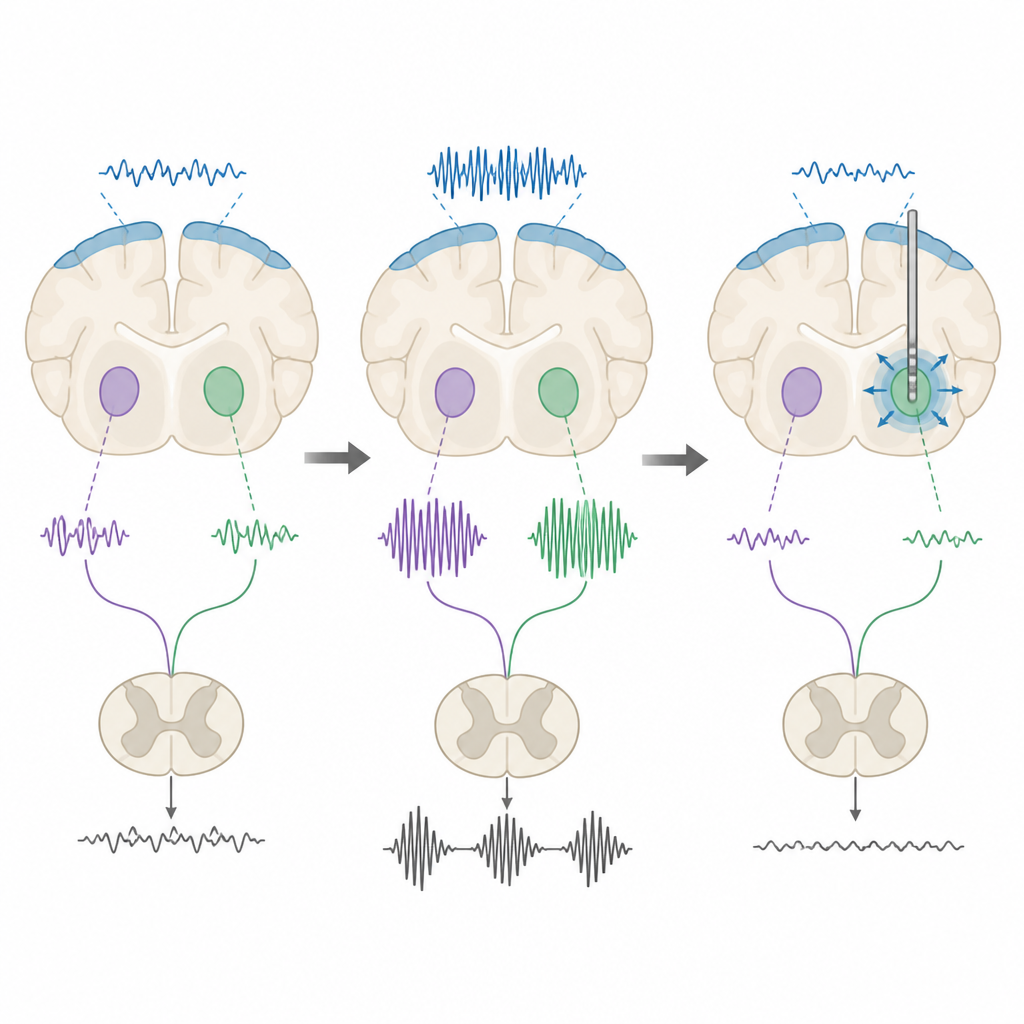
Тестирование режимов мозговой стимуляции
Затем исследователи проверили, может ли глубокая стимуляция мозга «настроить» эти ритмы. Они применяли как низкочастотные, так и высокочастотные электрические импульсы к субталамическому и энтопедунклярному ядрам. Под наркозом оба типа стимуляции снижали общую бета‑мощность у крыс с патологией, но не у здоровых животных, что показывает особую чувствительность аномальных ритмов к стимуляции. У бодрствующих крыс картина оказалась более тонкой. Высокочастотная стимуляция чаще укоротила бета‑всплески или уменьшала долю времени, проведённого в состоянии высокого бета, тогда как низкочастотная часто действовала противоположно — удлиняла всплески или увеличивала их суммарную продолжительность. При измерении походки на тесте ходьбы по решётке лишь высокочастотная стимуляция энтопедунклярного ядра улучшала точность постановки ступней у крыс.
Что это значит для будущего лечения
В целом результаты показывают, что эта крысиная модель достоверно развивает те же типы бета‑всплесков и нерегулярности разрядов, что и у людей с болезнью Паркинсона, и реагирует на глубокую стимуляцию мозга в зависимоти от частоты. Высокочастотные импульсы кажутся лучше приспособленными для разрыва длинных, нарушающих бета‑всплесков и для содействия более плавному движению по сравнению с низкочастотными. Карта возникновения аномальных ритмов по моторной сети и того, как разные настройки стимуляции их перестраивают, даёт мощную испытательную площадку для будущих стратегий, нацеленных не просто на «заглушение» областей мозга, а на перенастройку их электрического ритма для лучшего контроля симптомов Паркинсона.
Цитирование: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Ключевые слова: болезнь Паркинсона, бета‑осцилляции, глубокая стимуляция мозга, базальные ганглии, крысиная модель