Clear Sky Science · ar
تذبذبات بيتا في القشرة والعقد القاعدية وتأثيرات التحفيز العميق للمخ المعتمدة على التردد في نموذج فأري لمرض باركنسون A53T
لماذا تهم هذه الدراسة لإيقاعات الدماغ
يشتهر مرض باركنسون بالرجفان وبطء الحركة، لكن داخل الدماغ يميّزه أيضاً إيقاعات «بيتا» شاذة، وهي نوع من النبض الكهربائي الخلفي. يمكن للجراحين تخفيف الأعراض عبر التحفيز العميق للمخ، وهو علاج يشبه منظم ضربات القلب يرسل نبضات إلى مناطق دماغية محددة. ومع ذلك ظل من غير الواضح إلى أي مدى يعود هذا الفائدة لكبح هذه الإيقاعات البيتية وأي أنماط تحفيز هي الأفضل. تستخدم هذه الدراسة نموذج فأري يحاكي مرض باركنسون البشري لمراقبة بروز هذه الإيقاعات واختبار كيف تشكّلها أنواع مختلفة من التحفيز، مما يقدم دلائل قد تساعد على تحسين علاجات دماغية مستقبلية.
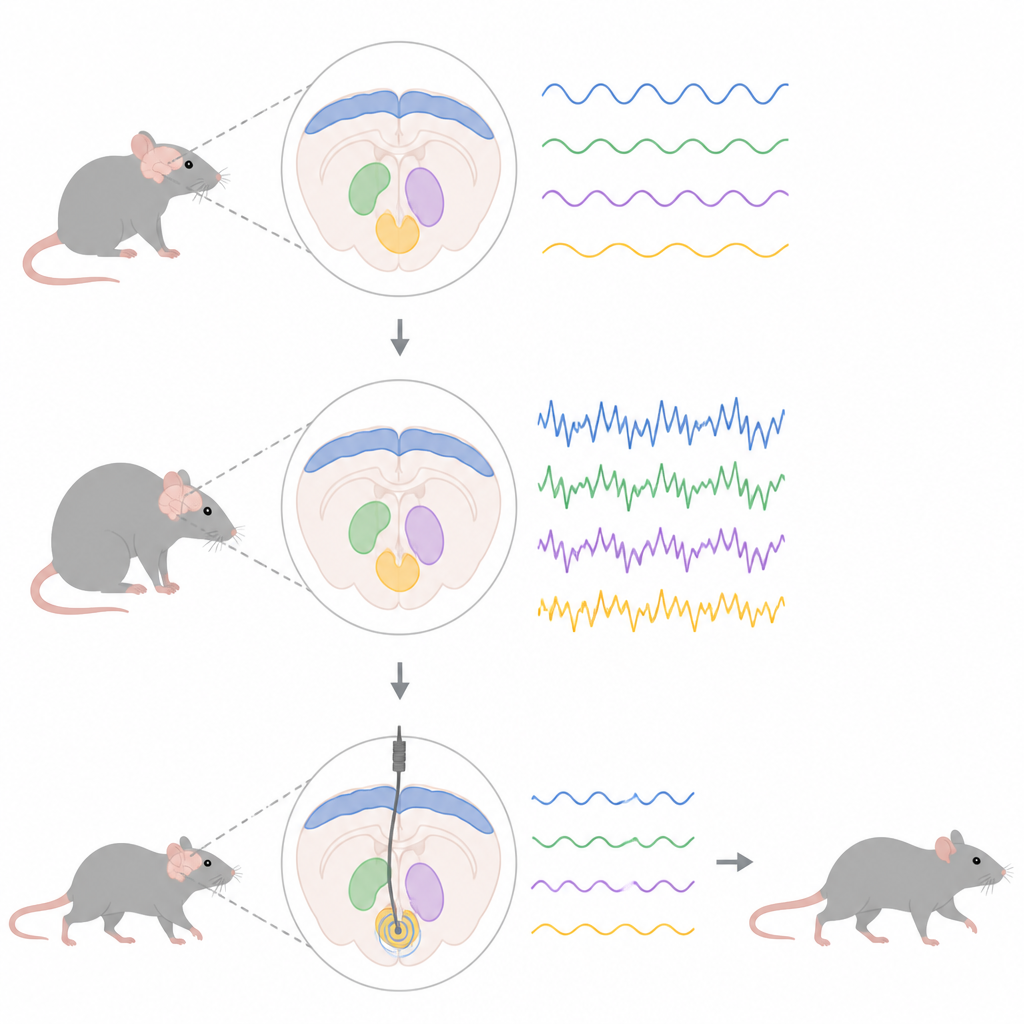
متابعة النبض الخفي للدماغ
استخدم الباحثون حيلة جينية لجعل الفئران تفرط في إنتاج شكل طفري من بروتين الألفا-سينوكلين، نفس البروتين الذي يتراكم لدى كثير من المصابين بمرض باركنسون. هذا تسبب تدريجياً في موت الخلايا المنتجة للدوبامين في منتصف الدماغ، مما أحدث تغييرات في شبكة حركة أوسع تربط القشرة الخارجية ببُنى عميقة تسمى النواة تحت المهادية والنواة الانتوبِندونكيولار، وهي المعادل الفأري لمركز إخراج رئيسي في البشر. بوضع أقطاب دقيقة في هذه المناطق، تتبّع الفريق الإمكانات الميدانية المحلية، أي النشاط الكهربائي المجمّع لكثير من الخلايا العصبية، مع التركيز على النشاط في نطاق بيتا بين 13 و30 دورة في الثانية.
انتشار تدريجي لإيقاعات مريضة
أظهرت التسجيلات تحت تخدير خفيف أن النشاط البيتائي الشاذ لم يظهر في كل مكان دفعة واحدة. في بدايات المرض، عندما كان فقدان الدوبامين لا يزال طفيفاً، بدا أن القوة البيتائية الزائدة كانت مرئية بالفعل في قشرة الحركة، الطبقة الخارجية التي تساعد في تخطيط وبدء الحركات. لم تظهر الإيقاعات البيتائية القوية في النواتين تحت المهادية والانتوبندونكيولار إلا لاحقاً، مع ازدياد موت خلايا الدوبامين. في الفئران الحاملة للبروتين المرضي، تغيّرت أيضاً طريقة إطلاق الخلايا العصبية في هذه المناطق العميقة: بدأت خلايا النواة الانتوبندونكيولارية بإطلاق النبضات بوتيرة أسرع وبشكل اندفاعي، بينما طوّرت خلايا النواة تحت المهادية أنماطاً أكثر عدم انتظام واندفاعية في المراحل المتأخرة، حتى من دون تغيير كبير في معدل إطلاقها المتوسط.
اندفاعات تعرقل الحركة السلسة
لمعرفة كيف تتصرف هذه الإشارات أثناء السلوك الطبيعي، كرر الفريق التسجيلات في فئران يقظة تتحرك بحرية. بدلاً من همهمة ثابتة، ظهر نشاط بيتا على شكل اندفاعات قصيرة. أظهرت الفئران ذات التغيرات الشبيهة بالباركنسون اندفاعات أطول، وحدثت بتواتر أكبر، وشغلت معاً وقتاً أكثر مقارنة بالحيوانات الضابطة. في النواة تحت المهادية ارتبط النشاط البيتائي الأقوى بتناقص الحركة، مما يعكس ملاحظات لدى البشر المصابين بباركنسون حيث ترتبط اندفاعات بيتا بالصعوبة في بدء والتحكم في الحركات. وتقترح هذه الأنماط أن توقيت وشكل الاندفاعات، وليس فقط القوة البيتائية الإجمالية، هما المهمان في كيفية تعطيل المرض للحركة.
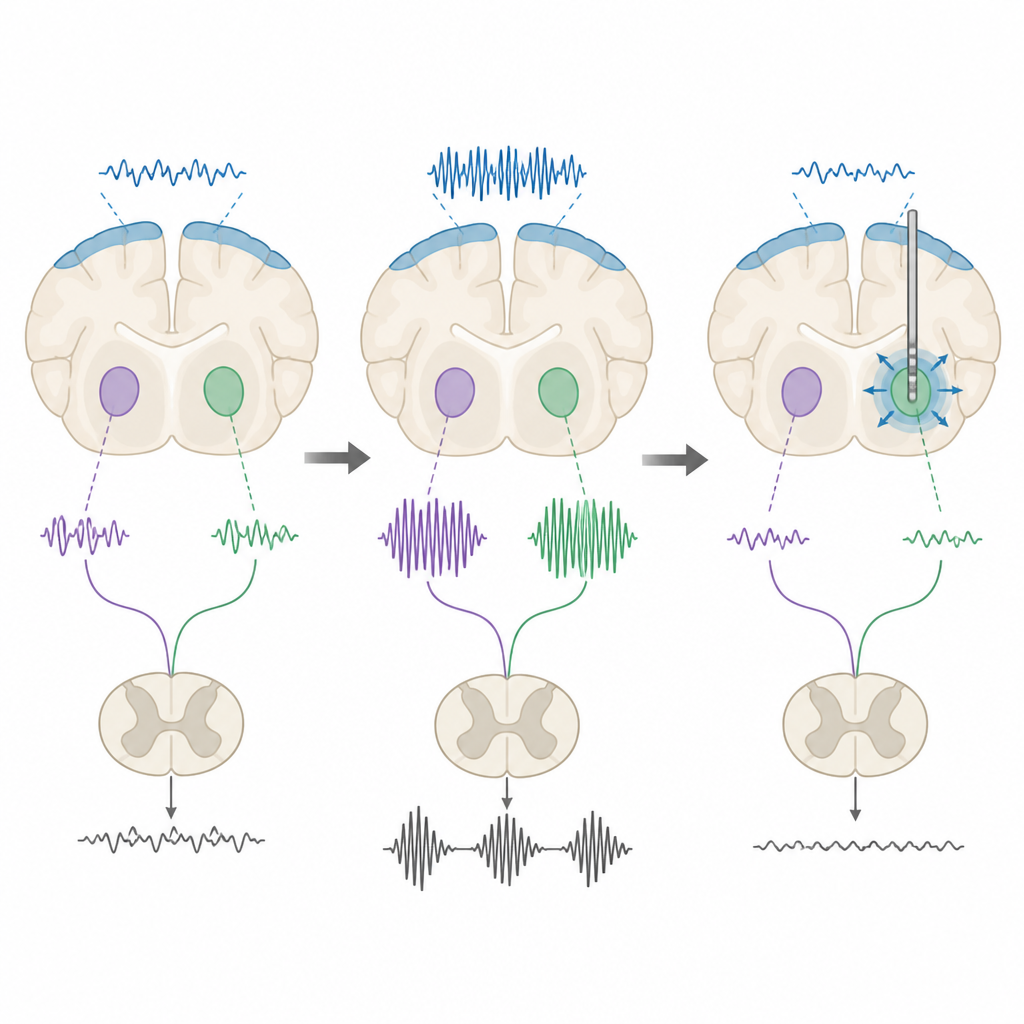
اختبار أنماط التحفيز الدماغي
اختبر الباحثون بعد ذلك ما إذا كان التحفيز العميق للمخ يمكنه ضبط هذه الإيقاعات. طبقوا نبضات كهربائية منخفضة التردد وعالية التردد على النواتين تحت المهادية والانتوبندونكيولار. تحت التخدير قلّلت كلا طرقا التحفيز من القدرة البيتائية الإجمالية في الفئران الحاملة للتغيرات المرضية، لكن ليس في الحيوانات السليمة، ما يدل على أن الإيقاعات الشاذة حساسة بشكل خاص للتحفيز. وفي الفئران اليقظة ظهر مشهد أكثر دقة. ميّلت التحفيزات عالية التردد إلى تقصير اندفاعات بيتا أو تقليل الوقت الذي يقضيه الإشارة في حالة بيتا مرتفعة، بينما غالباً ما كان للتحفيز منخفض التردد التأثير المعاكس، متمثلاً في إطالة الاندفاعات أو زيادة مدتها الإجمالية. وعند قياس الحركة في اختبار المشي على شبكة، تحسنت دقة خطوة الفئران فقط عند التحفيز عالي التردد للنواة الانتوبندونكيولار.
ماذا يعني هذا للعلاج المستقبلي
بإجمالها، تُظهر النتائج أن هذا النموذج الفأري يطوّر بصورة موثوقة نفس نوع اندفاعات بيتا وعدم انتظام الإطلاق الذي يُرى لدى مرضى باركنسون ويستجيب للتحفيز العميق للمخ بطريقة تعتمد على التردد. تبدو النبضات عالية التردد أكثر ملاءمة من منخفضة التردد لتفكيك اندفاعات بيتا الطويلة والمضطربة ودعم حركة أكثر سلاسة. من خلال رسم خريطة كيفية نشوء الإيقاعات الشاذة عبر شبكة الحركة وكيف تعيدها إعدادات التحفيز المختلفة، يوفر هذا العمل أرضية اختبار قوية لاستراتيجيات مستقبلية تهدف ليس فقط إلى إسكات مناطق الدماغ، بل إلى إعادة ضبط توقيتها الكهربائي للتحكم الأفضل في أعراض باركنسون.
الاستشهاد: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
الكلمات المفتاحية: مرض باركنسون, تذبذبات بيتا, التحفيز العميق للمخ, العقد القاعدية, نموذج فأري