Clear Sky Science · nl
Corticale en basale ganglia beta-oscillaties en frequentie-afhankelijke DBS-effecten in het A53T-parkinsonratmodel
Waarom dit onderzoek naar hersenritmes ertoe doet
De ziekte van Parkinson staat vooral bekend om tremoren en vertraagde beweging, maar diep in de hersenen wordt ze ook gekenmerkt door abnormale “beta”-ritmes, een soort elektrische achtergrondslag. Chirurgen kunnen de symptomen verlichten met diepe hersenstimulatie, een pacemakerachtige therapie die pulsen naar specifieke hersengebieden stuurt. Toch was het onduidelijk hoeveel van dit voordeel voortkomt uit het dempen van die beta-ritmes en welke stimulatiepatronen het meest effectief zijn. Deze studie gebruikt een rattenmodel dat nauw aansluit bij menselijke Parkinson om die ritmes te volgen en te testen hoe verschillende vormen van stimulatie ze beïnvloeden, wat aanwijzingen kan geven om toekomstige hersentherapieën te verfijnen.
Het verborgen ritme van de hersenen volgen
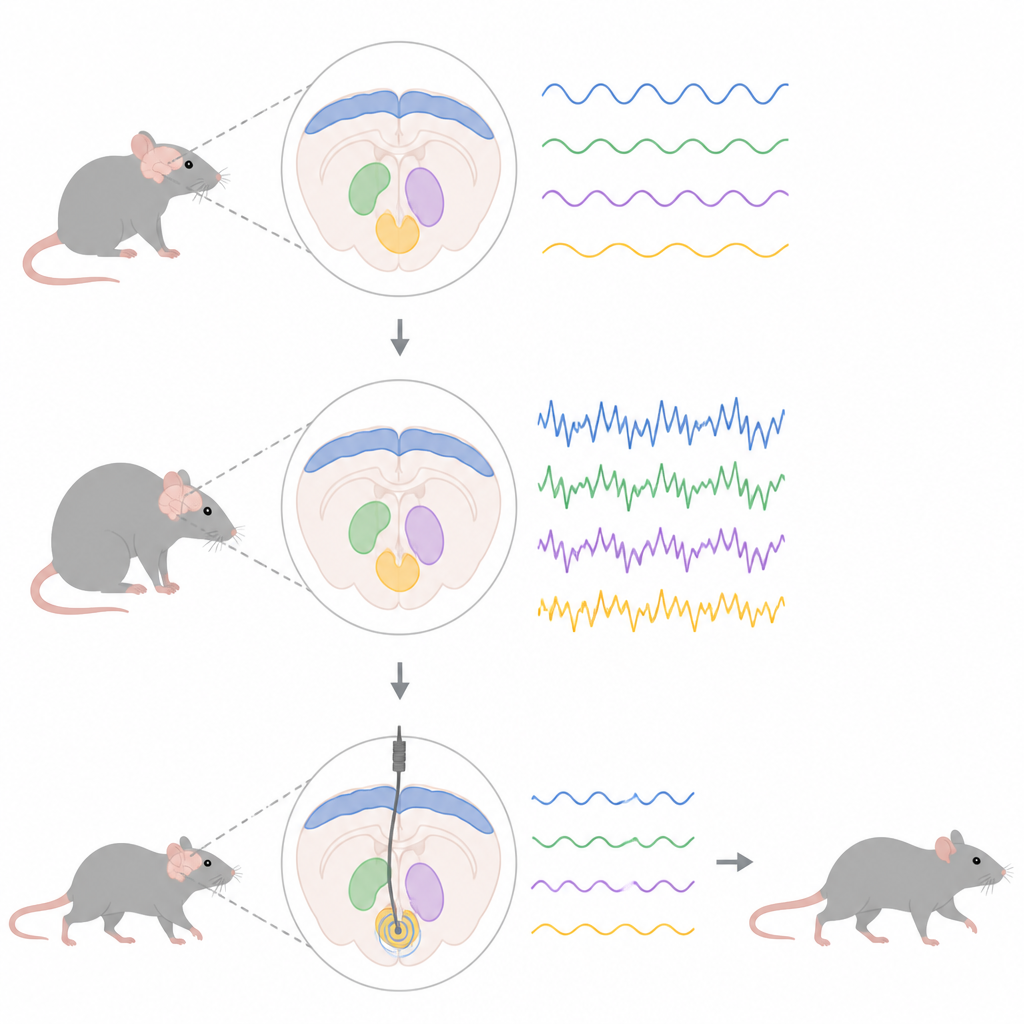
De onderzoekers gebruikten een genetische truc om ratten te laten te veel produceren van een gemuteerde vorm van alfa-synucleïne, hetzelfde eiwit dat zich ophoopt bij veel mensen met de ziekte van Parkinson. Dit zorgde er geleidelijk voor dat dopamine-producerende cellen in de middenhersenen afstierven, wat veranderingen in een groter bewegingsnetwerk in gang zette dat de cortex verbindt met diepe structuren zoals de subthalamische nucleus en de entopedunculaire nucleus, het rattenequivalent van een belangrijk menselijk uitvoercentrum. Door fijne elektroden in deze gebieden te plaatsen, volgde het team lokale veldpotentialen, de gecombineerde elektrische activiteit van veel zenuwcellen, met de focus op activiteit in het beta-bereik tussen 13 en 30 cycli per seconde.
Stapsgewijze verspreiding van ongezonde ritmes
Opnames onder lichte anesthesie lieten zien dat abnormale beta-activiteit niet overal tegelijk verscheen. Vroeg in het ziekteproces, toen het dopamineverlies nog bescheiden was, was extra beta-vermogen al zichtbaar in de motorische cortex, de buitenste laag die helpt bij het plannen en starten van bewegingen. Pas later, naarmate meer dopaminerge cellen stierven, ontstonden sterke beta-ritmes in de subthalamische en entopedunculaire nuclei. In ratten met het ziekte-eiwit veranderden de zenuwcellen in deze diepe regio’s ook hun vuurmotoriek: cellen in de entopedunculaire nucleus begonnen sneller en in bursts te vuren, terwijl subthalamische cellen in latere stadia onregelmatiger en meer in bursts gingen vuren, zelfs zonder een grote verandering in hun gemiddelde vuursnelheid.
Bursts die vloeiende beweging blokkeren
Om te zien hoe deze signalen zich gedragen tijdens natuurlijk gedrag herhaalde het team de opnames in wakker bewegende ratten. In plaats van een constante toon trad beta-activiteit op als korte bursts. Ratten met de Parkinson-achtige veranderingen vertoonden bursts die langer duurden, vaker voorkwamen en samen meer tijd in beslag namen dan bij controledieren. In de subthalamische nucleus ging sterkere beta-activiteit gepaard met minder beweging, wat echo’s van waarnemingen bij mensen met Parkinson weerspiegelt, waar beta-bursts gekoppeld zijn aan moeite met het starten en beheersen van acties. Deze patronen suggereren dat het de timing en vorm van de bursts is, en niet alleen de algehele beta-sterkte, die van belang is voor hoe de ziekte beweging verstoort.
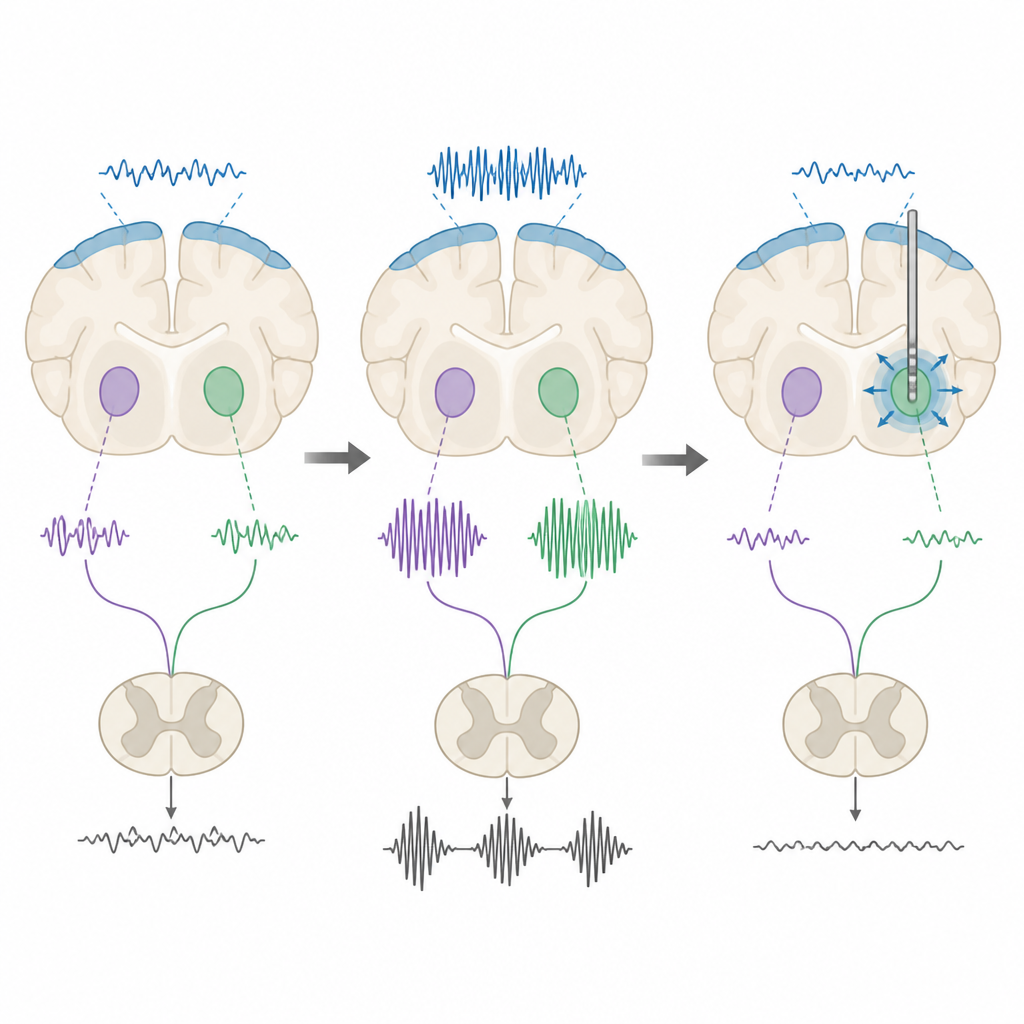
Testen van stimulatiepatronen in de hersenen
De onderzoekers testten vervolgens of diepe hersenstimulatie deze ritmes kon bijsturen. Ze pasten zowel laagfrequente als hoogfrequente elektrische pulsen toe op de subthalamische en entopedunculaire nuclei. Onder anesthesie verminderden beide vormen van stimulatie het algehele beta-vermogen bij ratten met de ziekteveranderingen, maar niet bij gezonde controles, wat laat zien dat de abnormale ritmes bijzonder gevoelig zijn voor stimulatie. Bij wakker bewegende ratten ontstond een genuanceerder beeld. Hoogfrequente stimulatie had de neiging beta-bursts te verkorten of de tijd dat het signaal zich in een hoog-beta-toestand bevond te verminderen, terwijl laagfrequente stimulatie vaak het tegenovergestelde effect had, bursts verlengde of hun totale duur vergrootte. Toen het team de beweging mat in een rasterlooptest, verbeterde alleen hoogfrequente stimulatie van de entopedunculaire nucleus de stapnauwkeurigheid van de ratten.
Wat dit betekent voor toekomstige behandeling
Gezamenlijk tonen de bevindingen aan dat dit rattenmodel op betrouwbare wijze het type beta-bursts en vuurionregelmatigheden ontwikkelt dat ook bij mensen met de ziekte van Parkinson wordt gezien, en dat het frequentie-afhankelijk reageert op diepe hersenstimulatie. Hoogfrequente pulsen lijken beter geschikt dan laagfrequente om lange, verstorende beta-bursts te doorbreken en vloeiender bewegen te ondersteunen. Door in kaart te brengen hoe abnormale ritmes ontstaan in het bewegingsnetwerk en hoe verschillende stimulatie-instellingen ze hervormen, biedt dit werk een krachtig testveld voor toekomstige strategieën die niet alleen gericht zijn op het dempen van hersengebieden, maar op het opnieuw afstemmen van hun elektrische timing om de controle over Parkinson-symptomen te verbeteren.
Bronvermelding: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Trefwoorden: Ziekte van Parkinson, beta-oscillaties, deep brain stimulation, basale ganglia, rattenmodel