Clear Sky Science · sv
Kortikala och basala gangliernas betaoscillationer och frekvensberoende DBS‑effekter i A53T‑parkinsonråttmodellen
Varför denna studie om hjärnrytmer är viktig
Parkinsons sjukdom är mest känd för tremor och fördröjd rörelse, men djupt i hjärnan kännetecknas den också av onormala “beta”‑rytmer, en sorts elektrisk bakgrundspuls. Kirurger kan lindra symtomen med djup hjärnstimulering, en pacemakerliknande behandling som skickar pulser till specifika hjärnregioner. Det har emellertid varit oklart i vilken utsträckning denna nytta beror på att dämpa beta‑rytmerna och vilka stimulationsmönster som fungerar bäst. Denna studie använder en råttmodell som nära efterliknar mänsklig Parkinsons sjukdom för att iaktta hur dessa rytmer uppträder och testa hur olika typer av stimulering formar dem, och ger ledtrådar som kan hjälpa att förfina framtida hjärnterapier.
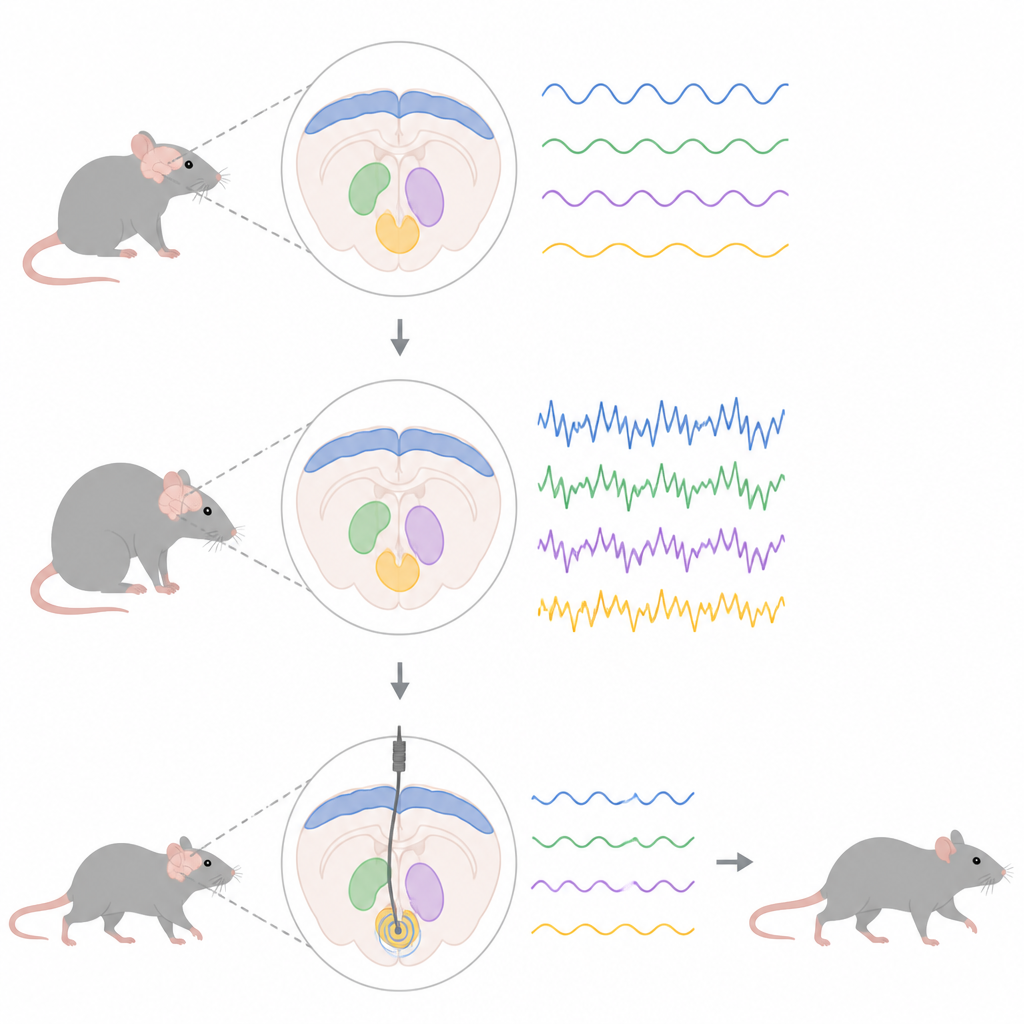
Att följa hjärnans dolda puls
Forskarlaget använde ett genetiskt knep för att få råttor att överproducera en muterad form av alfa‑synuklein, samma protein som ackumuleras hos många personer med Parkinsons sjukdom. Detta dödade gradvis ner dopaminproducerande celler i mitthjärnan och satte igång förändringar i ett större rörelsenätverk som förbinder cortex med djupa strukturer som subthalamiska kärnan och entopedunculära kärnan, råttans motsvarighet till en viktig mänsklig utgångscentral. Genom att placera fina elektroder i dessa områden följde teamet lokala fältpotentialer, den sammanlagda elektriska aktiviteten hos många nervceller, med fokus på aktivitet i betaområdet mellan 13 och 30 cykler per sekund.
Stegvis spridning av osunda rytmer
Inspelningar under lätt anestesi visade att onormal betaaktivitet inte dök upp överallt samtidigt. Tidigt i sjukdomsförloppet, när dopaminförlusten fortfarande var måttlig, syntes redan ökad betaeffekt i motorcortex, det yttre lagret som hjälper till att planera och initiera rörelser. Först senare, när fler dopaminceller hade gått förlorade, uppstod starka beta‑rytmer i subthalamiska och entopedunculära kärnorna. I råttor med sjukdomsproteinet förändrade även nervcellerna i dessa djupa regioner sina fyrningsmönster: celler i entopedunculära kärnan började fyras snabbare och i burstar, medan subthalamiska celler utvecklade mer oregelbundna, burstlika mönster i senare stadier, även utan stor förändring i deras genomsnittliga fyrningsfrekvens.
Burstar som blockerar jämn rörelse
För att se hur dessa signaler beter sig under naturligt beteende upprepade forskarna inspelningarna i vakna råttor som rörde sig fritt. Istället för ett stadigt brus framträdde betaaktiviteten som korta burstar. Råttor med Parkinsonlika förändringar visade burstar som var längre, uppträdde oftare och tillsammans upptog mer tid än hos kontrollråttor. I subthalamiska kärnan gick starkare betaaktivitet hand i hand med mindre rörelse, vilket speglar observationer hos människor med Parkinsons där beta‑burstar kopplas till svårigheter att starta och kontrollera handlingar. Dessa mönster tyder på att burstarnas timing och form, inte bara den totala betastyrkan, är avgörande för hur sjukdomen stör rörelse.
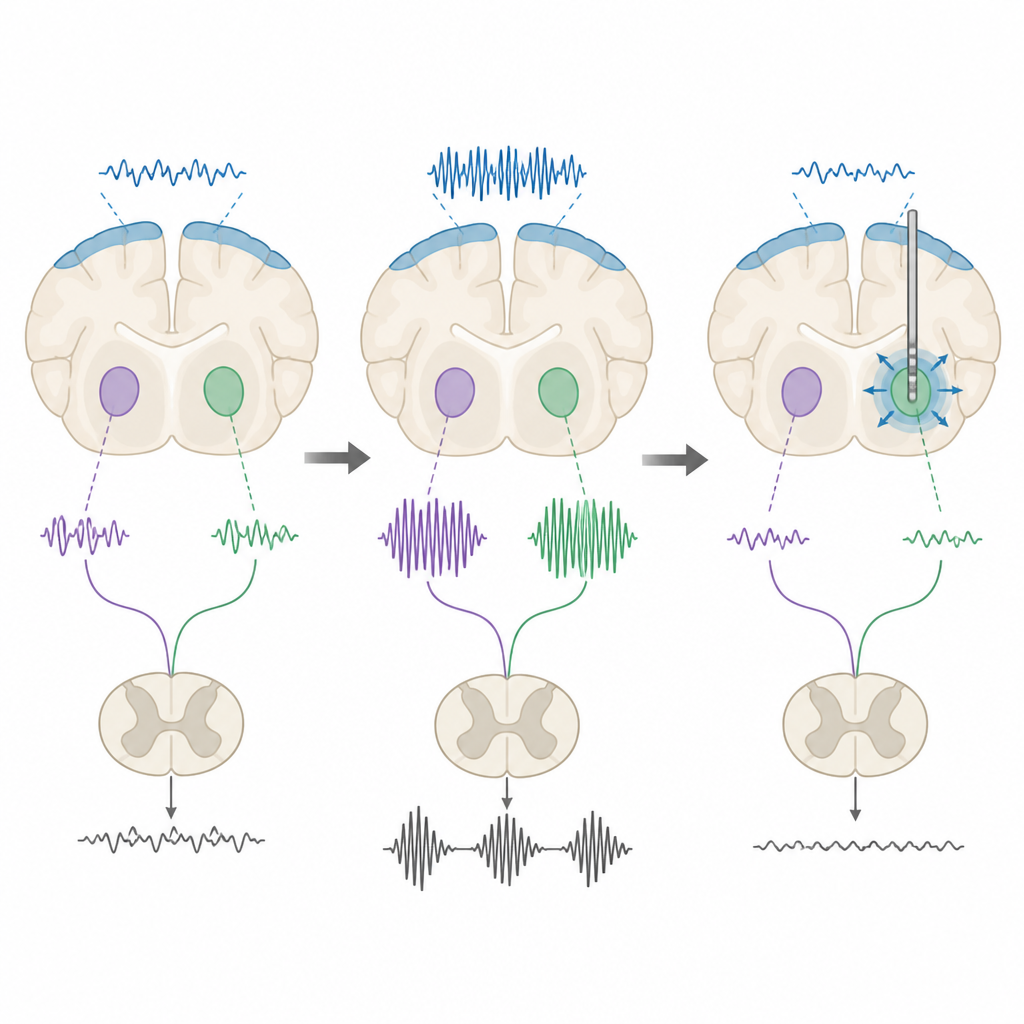
Test av stimulationsmönster
Forskarna testade sedan om djup hjärnstimulering kunde stämma av dessa rytmer. De applicerade både låg‑ och högfrekventa elektriska pulser på subthalamiska och entopedunculära kärnorna. Under anestesi minskade båda typerna av stimulering den totala betaeffekten hos råttor med sjukdomsförändringar, men inte hos friska kontroller, vilket visar att de onormala rytmerna är särskilt känsliga för stimulering. I vakna råttor framträdde en mer nyanserad bild. Högfrekvent stimulering tenderade att förkorta beta‑burstar eller reducera tiden signalen spenderade i ett högbeta‑tillstånd, medan låg‑frekvent stimulering ofta hade motsatt effekt och förlängde burstarna eller ökade deras totala varaktighet. När teamet mätte rörelse i ett rutnätstest förbättrade endast högfrekvent stimulering av den entopedunculära kärnan råttornas stegprecision.
Vad detta innebär för framtida behandling
Tillsammans visar resultaten att denna råttmodell pålitligt utvecklar samma slags beta‑burstar och oregelbunden fyrning som ses hos människor med Parkinsons sjukdom och svarar på djup hjärnstimulering på ett frekvensberoende sätt. Högfrekventa pulser verkar bättre lämpade än lågfrekventa för att bryta upp långa, störande beta‑burstar och stödja jämnare rörelse. Genom att kartlägga hur onormala rytmer uppstår i rörelsenätverket och hur olika stimulationsinställningar omformar dem erbjuder detta arbete en kraftfull testbädd för framtida strategier som inte bara syftar till att tysta hjärnregioner, utan att stämma om deras elektriska timing för bättre kontroll av Parkinsonsymtom.
Citering: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Nyckelord: Parkinsons sjukdom, betaoscillationer, djup hjärnstimulering, basala ganglier, råttmodell