Clear Sky Science · pl
Oscylacje beta w korze i prążkowiu i zależne od częstotliwości efekty DBS w szczurzym modelu choroby Parkinsona A53T
Dlaczego to badanie rytmów mózgowych ma znaczenie
Choroba Parkinsona jest najbardziej znana z drżeń i spowolnienia ruchów, ale głęboko w mózgu przejawia się też nieprawidłowymi rytmami „beta” — rodzajem elektrycznego tła. Chirurdzy mogą łagodzić objawy za pomocą stymulacji głębokiej mózgu, terapii przypominającej rozrusznik, która dostarcza impulsy do określonych regionów mózgu. Nie było jednak jasne, na ile korzyści wynikają z tłumienia tych rytmów beta i które wzory stymulacji działają najlepiej. To badanie wykorzystuje szczurzy model, który wiernie odzwierciedla ludzką chorobę Parkinsona, aby obserwować pojawianie się tych rytmów i testować, jak różne rodzaje stymulacji je kształtują, dostarczając wskazówek, które mogą pomóc dopracować przyszłe terapie mózgowe.
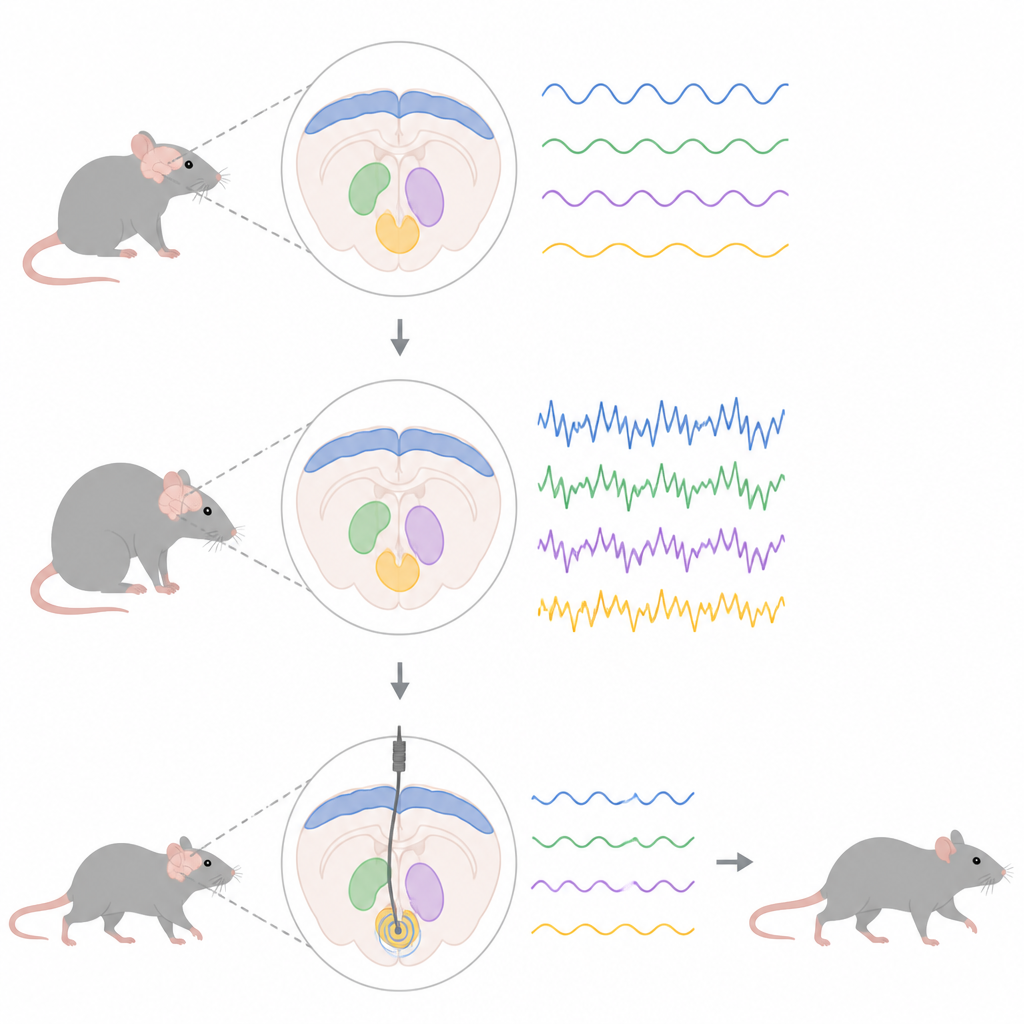
Śledzenie ukrytego rytmu mózgu
Naukowcy zastosowali genetyczny zabieg, by szczury nadmiernie produkowały zmutowaną formę alfa-synukleiny, tej samej białkowej cząsteczki, która gromadzi się u wielu osób z chorobą Parkinsona. To stopniowo niszczyło komórki produkujące dopaminę w śródmózgowiu, wywołując zmiany w szerszej sieci ruchowej, łączącej korę z głębokimi strukturami takimi jak jądro niskowzgórzowe (subthalamiczne) i jądro entopeduncularne, odpowiadającym u szczura ważnemu wyjściowemu ośrodkowi u ludzi. Umieszczając cienkie elektrody w tych obszarach, badacze rejestrowali potencjały polowe — skumulowaną aktywność elektryczną wielu komórek nerwowych — koncentrując się na aktywności w paśmie beta między 13 a 30 cykli na sekundę.
Krokowe szerzenie się niezdrowych rytmów
Nagrania wykonane pod lekkim znieczuleniem wykazały, że nieprawidłowa aktywność beta nie pojawiała się wszędzie jednocześnie. Wczesnie w przebiegu choroby, gdy utrata dopaminy była wciąż umiarkowana, dodatkowa moc w paśmie beta była już widoczna w korze ruchowej, zewnętrznej warstwie pomagającej planować i inicjować ruchy. Dopiero później, gdy więcej komórek dopaminowych zginęło, silne rytmy beta pojawiły się w jądrach niskowzgórzowym i entopeduncularnym. U szczurów z białkiem chorobowym komórki nerwowe w tych głębokich regionach także zmieniły sposób wyładowywania: komórki w jądrze entopeduncularnym zaczęły wyładowywać szybciej i w seriach, podczas gdy komórki jądra niskowzgórzowego rozwinęły bardziej nieregularne, skokowe wzorce w późniejszych stadiach, nawet bez dużej zmiany średniej częstości wyładowań.
Wybuchy, które hamują płynność ruchu
Aby sprawdzić, jak te sygnały zachowują się podczas naturalnego zachowania, zespół powtórzył nagrania u świadomych szczurów poruszających się swobodnie. Zamiast stałego szumu, aktywność beta pojawiała się jako krótkie wybuchy. Szczury z Parkinsonopodobnymi zmianami wykazywały wybuchy dłuższe, występujące częściej i zajmujące łącznie więcej czasu niż u zwierząt kontrolnych. W jądrze niskowzgórzowym silniejsza aktywność beta szła w parze z mniejszą ruchliwością, co odzwierciedla obserwacje u ludzi z chorobą Parkinsona, gdzie wybuchy beta wiążą się z trudnościami w inicjowaniu i kontrolowaniu ruchów. Te wzorce sugerują, że to timing i kształt wybuchów, a nie tylko ogólna moc beta, mają znaczenie dla tego, jak choroba zaburza ruch.
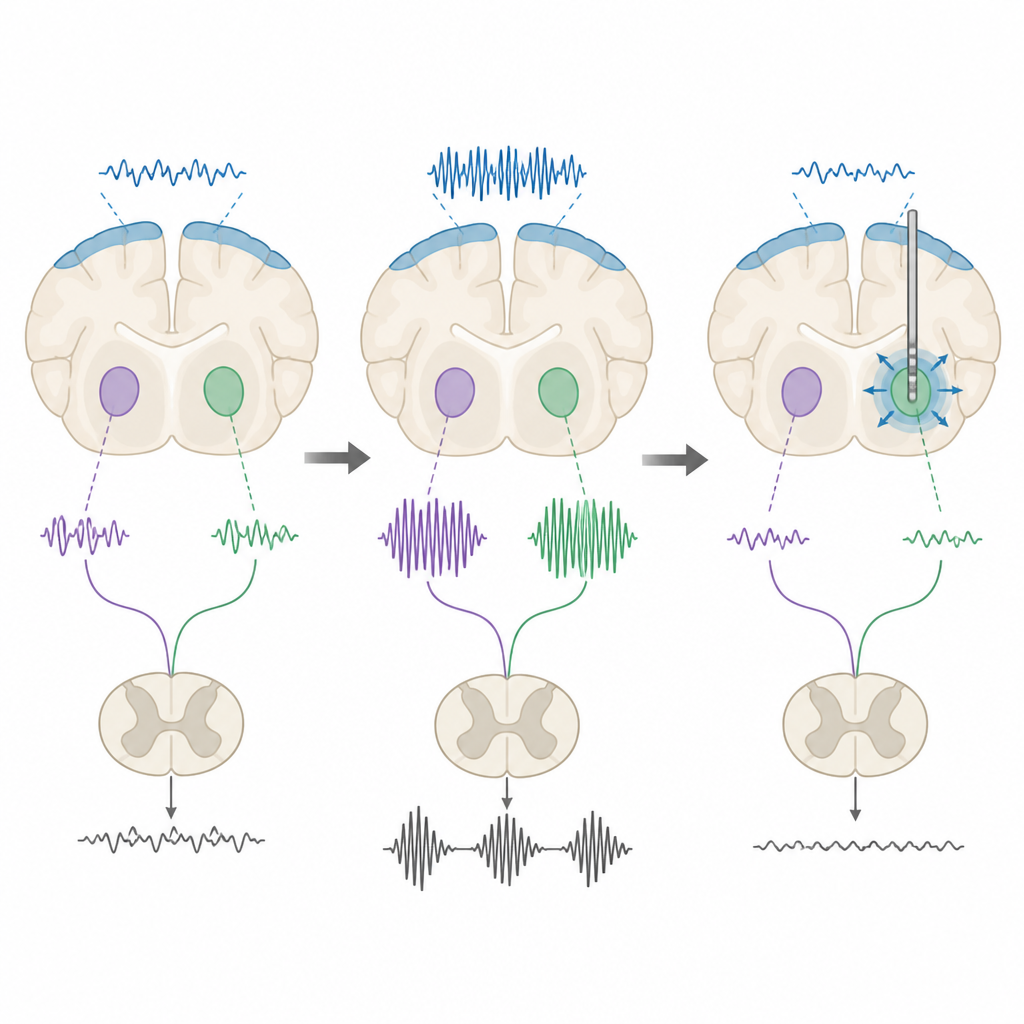
Testowanie wzorów stymulacji mózgu
Następnie badacze sprawdzili, czy stymulacja głęboka mózgu może dostroić te rytmy. Zastosowali zarówno niskoczęstotliwościowe, jak i wysokoczęstotliwościowe impulsy do jąder niskowzgórzowego i entopeduncularnego. Pod znieczuleniem oba rodzaje stymulacji zmniejszały ogólną moc beta u szczurów z patologią, ale nie u zdrowych kontrol, co pokazuje, że nieprawidłowe rytmy są szczególnie wrażliwe na stymulację. U świadomych szczurów obraz był bardziej zniuansowany. Stymulacja wysokimi częstotliwościami miała tendencję do skracania wybuchów beta lub zmniejszania czasu, jaki sygnał spędzał w stanie wysokiej aktywności beta, podczas gdy stymulacja niskimi częstotliwościami często działała odwrotnie — wydłużała wybuchy lub zwiększała ich łączny czas trwania. Gdy zespół mierzył ruchy na teście chodzenia po kratce, tylko wysokoczęstotliwościowa stymulacja jądra entopeduncularnego poprawiła precyzję stawiania kroków u szczurów.
Co to oznacza dla przyszłego leczenia
Podsumowując, wyniki pokazują, że ten szczurzy model niezawodnie rozwija ten sam rodzaj wybuchów beta i nieregularności w wyładowaniach obserwowany u osób z chorobą Parkinsona i reaguje na stymulację głęboką mózgu w sposób zależny od częstotliwości. Impulsy o wysokiej częstotliwości wydają się lepiej nadawać do przerywania długich, zakłócających wybuchów beta i wspierania płynniejszego ruchu niż impulsy o niskiej częstotliwości. Mapując, jak nieprawidłowe rytmy pojawiają się w sieci ruchowej i jak różne ustawienia stymulacji je przekształcają, praca ta dostarcza solidnego pola testowego dla przyszłych strategii, które mają na celu nie tylko uciszenie regionów mózgu, ale retuning ich elektrycznego timingu w celu lepszej kontroli objawów Parkinsona.
Cytowanie: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Słowa kluczowe: choroba Parkinsona, oscylacje beta, stymulacja głęboka mózgu, jądra podstawy, model szczura