Clear Sky Science · it
Oscillazioni beta corticali e dei gangli della base ed effetti della DBS dipendenti dalla frequenza nel modello di ratto A53T della malattia di Parkinson
Perché questo studio sui ritmi cerebrali è importante
La malattia di Parkinson è più conosciuta per i tremori e il rallentamento dei movimenti, ma nelle profondità del cervello si caratterizza anche per ritmi beta anomali, una sorta di battito elettrico di fondo. I neurochirurghi possono alleviare i sintomi con la stimolazione cerebrale profonda, una terapia simile a un pacemaker che invia impulsi a regioni cerebrali specifiche. Resta però poco chiaro quanto di questo beneficio derivi dall’attenuazione di quei ritmi beta e quali schemi di stimolazione funzionino meglio. Questo studio usa un modello di ratto che imita da vicino il Parkinson umano per osservare l’emergere di quei ritmi e testare come diversi tipi di stimolazione li modellano, offrendo indizi che potrebbero aiutare a perfezionare future terapie cerebrali.
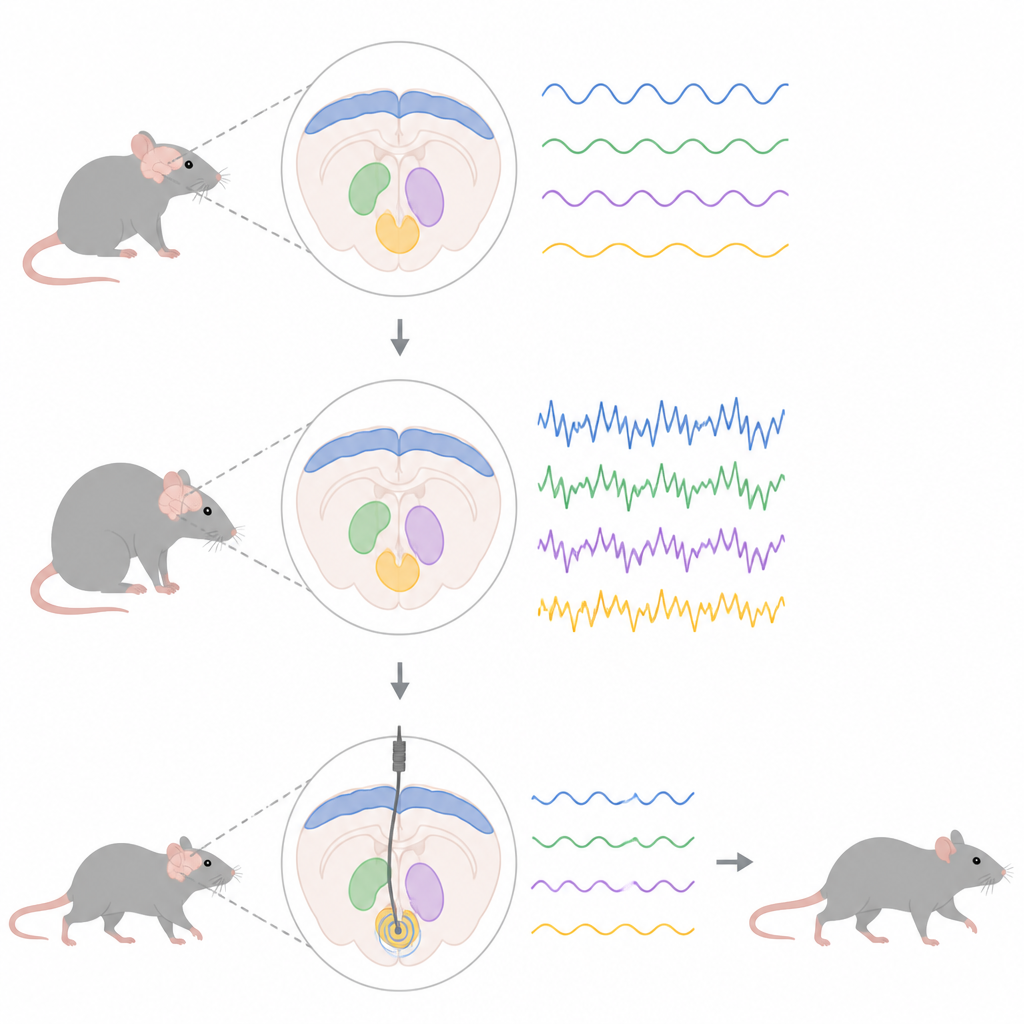
Seguire il battito nascosto del cervello
I ricercatori hanno impiegato un espediente genetico per indurre nei ratti una sovrapproduzione di una forma mutante della alfa-sinucleina, la stessa proteina che si accumula in molte persone con la malattia di Parkinson. Questo ha progressivamente ucciso le cellule che producono dopamina nel mesencefalo, innescando cambiamenti in una più ampia rete motoria che collega la corteccia esterna a strutture profonde chiamate nucleo subtalamico e nucleo entopeduncolare, l’equivalente nel ratto di un importante snodo di uscita umano. Inserendo elettrodi sottili in queste aree, il team ha registrato i potenziali di campo locali, l’attività elettrica combinata di molti neuroni, concentrandosi sull’attività nella banda beta tra 13 e 30 cicli al secondo.
Diffusione graduale dei ritmi patologici
Le registrazioni sotto lieve anestesia hanno mostrato che l’attività beta anomala non compariva ovunque contemporaneamente. All’inizio del processo patologico, quando la perdita di dopamina era ancora modesta, un aumento della potenza beta era già visibile nella corteccia motoria, lo strato esterno che aiuta a pianificare e avviare i movimenti. Solo più tardi, con la morte di un maggior numero di cellule dopaminergiche, emersero ritmi beta forti nel nucleo subtalamico e nel nucleo entopeduncolare. Nei ratti con la proteina legata alla malattia, i neuroni in queste regioni profonde cambiarono anche il loro pattern di scarica: le cellule nel nucleo entopeduncolare cominciarono a sparare più velocemente e a raffiche, mentre le cellule subtalamiche svilupparono pattern più irregolari e a raffiche nelle fasi successive, anche senza un grande cambiamento della loro frequenza di scarica media.
Raffiche che ostacolano il movimento fluido
Per capire come questi segnali si comportano durante il comportamento naturale, il team ripeté le registrazioni in ratti svegli che si muovevano liberamente. Invece di un ronzio costante, l’attività beta compariva come brevi raffiche. I ratti con i cambiamenti simili al Parkinson mostravano raffiche più lunghe, più frequenti e complessivamente più presenti rispetto agli animali di controllo. Nel nucleo subtalamico, una maggiore attività beta andava di pari passo con una riduzione del movimento, rispecchiando osservazioni fatte nelle persone con Parkinson dove i burst beta sono collegati a difficoltà nell’avviare e controllare le azioni. Questi schemi suggeriscono che è il timing e la forma delle raffiche, non solo la forza complessiva della beta, a essere rilevanti per il modo in cui la malattia compromette il movimento.
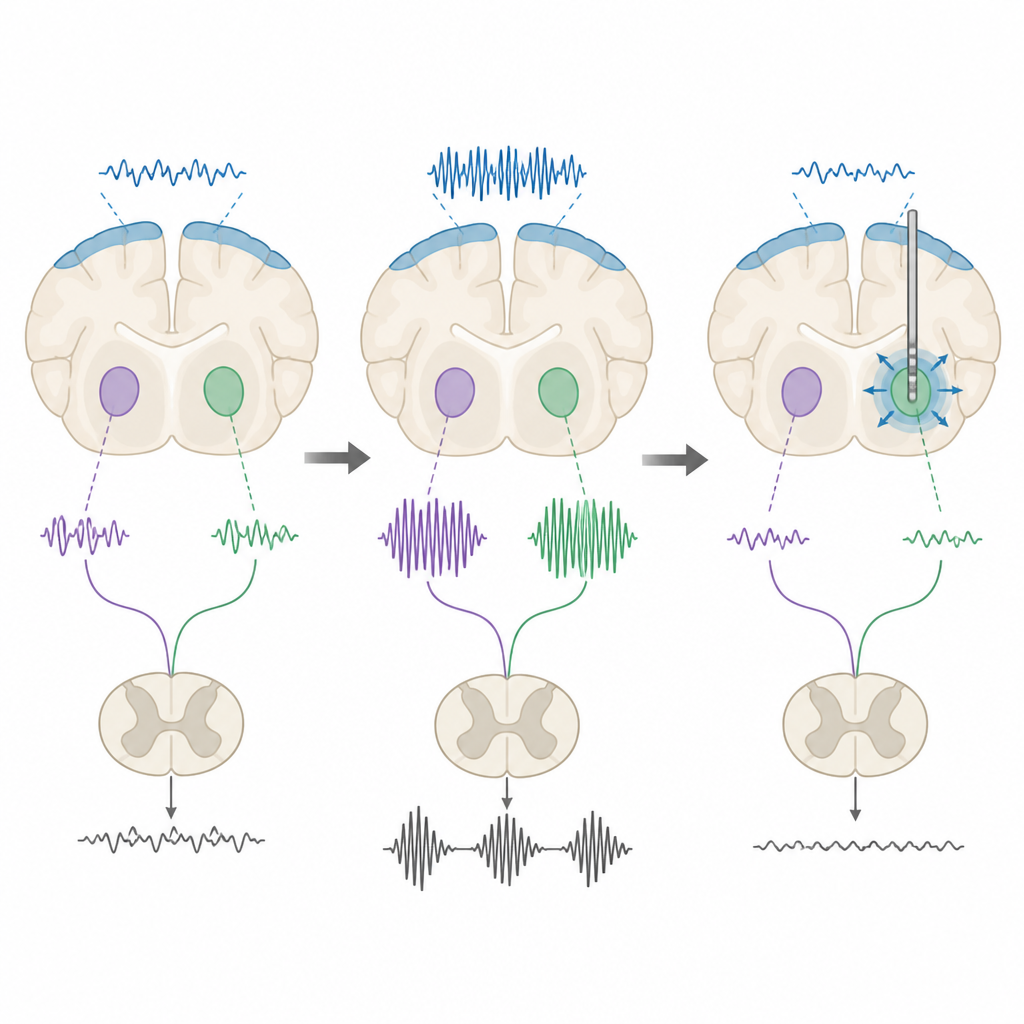
Testare schemi di stimolazione cerebrale
I ricercatori hanno quindi verificato se la stimolazione cerebrale profonda potesse modulare questi ritmi. Hanno applicato impulsi elettrici sia a bassa frequenza sia ad alta frequenza al nucleo subtalamico e al nucleo entopeduncolare. Sotto anestesia, entrambi i tipi di stimolazione ridussero la potenza beta complessiva nei ratti con i cambiamenti patologici, ma non nei controlli sani, indicando che i ritmi anomali sono particolarmente sensibili alla stimolazione. Nei ratti svegli emerse un quadro più sfumato. La stimolazione ad alta frequenza tendeva ad accorciare le raffiche beta o a ridurre il tempo in cui il segnale restava in uno stato di alta-beta, mentre la stimolazione a bassa frequenza spesso aveva l’effetto opposto, allungando le raffiche o aumentando la loro durata totale. Quando il team misurò il movimento con un test di camminata su griglia, solo la stimolazione ad alta frequenza del nucleo entopeduncolare migliorò la precisione dei passi dei ratti.
Cosa significa per i trattamenti futuri
Nel complesso, i risultati mostrano che questo modello di ratto sviluppa in modo affidabile lo stesso tipo di burst beta e di irregolarità di scarica osservati nelle persone con Parkinson e risponde alla stimolazione cerebrale profonda in modo dipendente dalla frequenza. Gli impulsi ad alta frequenza sembrano più efficaci delle basse frequenze nel frammentare le lunghe raffiche beta dannose e nel favorire movimenti più fluidi. Tracciando come i ritmi anomali emergono nella rete del movimento e come le diverse impostazioni di stimolazione li rimodellano, questo lavoro fornisce un campo di prova potente per strategie future che puntano non solo a silenziare regioni cerebrali, ma a ritunare il loro timing elettrico per un migliore controllo dei sintomi del Parkinson.
Citazione: Kondrataviciute, L., Kapadia, M., Skelin, I. et al. Cortical and basal ganglia beta oscillations and frequency-dependent DBS effects in the A53T Parkinson’s disease rat model. npj Parkinsons Dis. 12, 113 (2026). https://doi.org/10.1038/s41531-026-01304-z
Parole chiave: malattia di Parkinson, oscillazioni beta, stimolazione cerebrale profonda, gangli della base, modello di ratto