Clear Sky Science · tr
Genom çapında tarama, virüs benzeri parçacık üretimini ve taşıma etkinliğini artıran üretici hücre değişikliklerini ortaya koyuyor
Neden Daha İyi Taşıyıcılar Önemli?
CRISPR gibi modern gen düzenleme araçları teoride hastalığa yol açan mutasyonları kaynağında düzeltebilir, ancak merkezî bir zorluk hâlâ duruyor: bu moleküler araçları doğru hücreye, doğru miktarda ve yalnızca gerektiği süre boyunca güvenli ve verimli şekilde nasıl ulaştırırız? Bu çalışma, gen düzenleme makinesini taşıyabilen küçük, enfeksiyon oluşturmayacak kabuklar olan mühendislikli virüs benzeri parçacıklar (eVLP’ler) adındaki yükselen bir teslimat aracı üzerine odaklanıyor. Önceki çalışmalar çoğunlukla parçacıkların kendisini ayarlamaya odaklanmışken, bu makale farklı bir soruyu gündeme getiriyor: ya parçacıkları üreten canlı hücreleri yeniden mühendislik yaparak her partiyi baştan daha etkili hâle getirirsek?
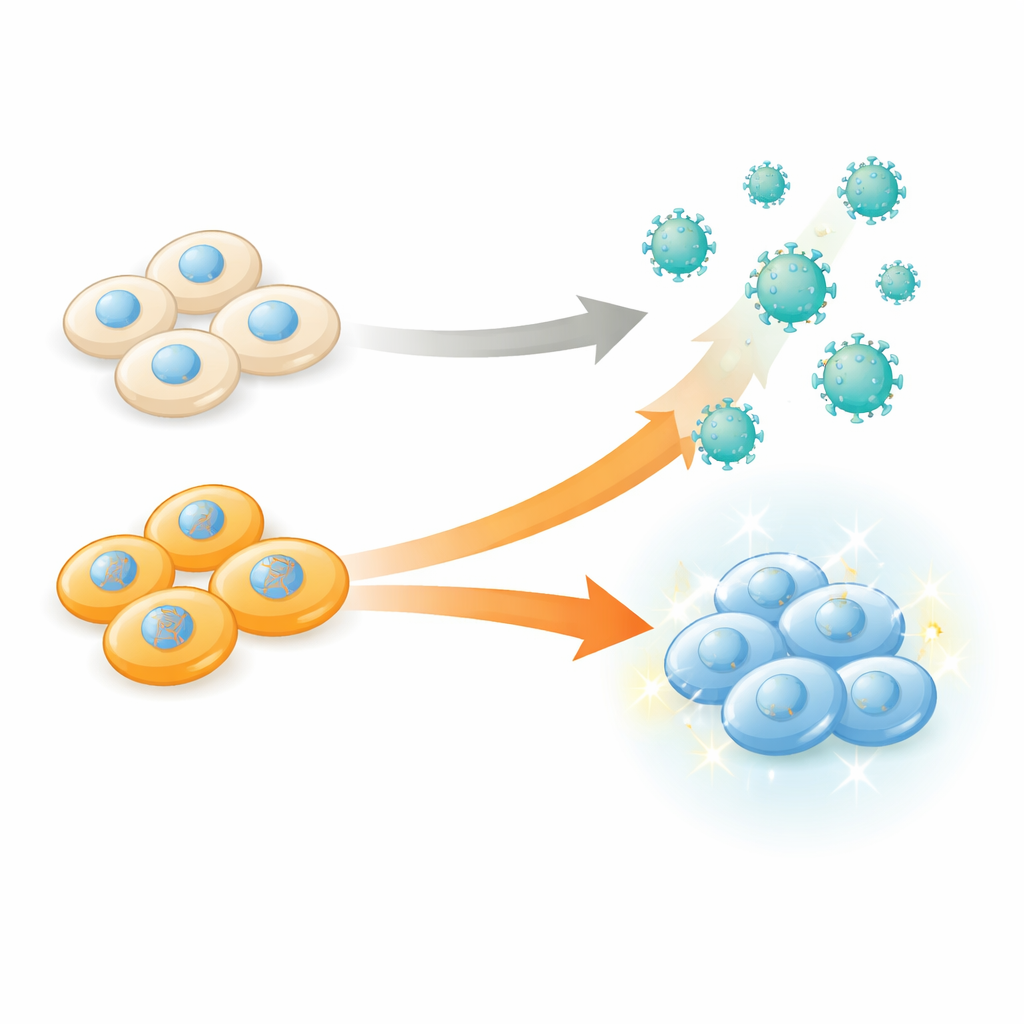
Ürünü Değil, Fabrikayı Yeniden Programlamak
eVLP’ler laboratuvarda viral kabuk proteinlerini bir araya getiren ve bunları gen düzenleme kargoyla yükleyip çevre sıvısına salan insan “üretici” hücreler tarafından üretilir. Geleneksel olarak bilim insanları parçacığın bileşenlerini ve mimarisini optimize etti—kabuk proteinlerini, kargo füzyonlarını veya yüzey moleküllerini değiştirerek—üretici hücrelerin yalnızca pasif fabrikalar olduğunu varsayarak. Yazarlar bu bakışı sorgulayarak üretici hücrelerin içindeki binlerce farklı genetik değişikliğin saldıkları eVLP’lerin sayısını ve kalitesini nasıl etkilediğini sistematik olarak test ettiler. Amaçları basit ama güçlüydü: hangi genlerin kapatılmasının hücreleri gen düzenleme araçlarını parçacıklara paketlemede daha iyi hâle getirdiğini belirlemek.
Yararlı Ayarlamalar İçin Genom Çapında Bir Arama
Bu devasa aramayı yürütmek için ekip, neredeyse her insan genini bozabilen genom çapında bir CRISPR “kapanış” kütüphanesi kullandı. Her üretici hücre, benzersiz bir RNA barkodu tarafından yönlendirilen bir mutasyon aldı ve eVLP’ler bu kılavuz RNA’ları gen düzenleme proteiniyle birlikte doğal olarak paketlediği için her parçacık, onu yapan hücrede hangi genetik değişiklik bulunduğunu gösteren moleküler bir etiket taşıdı. Araştırmacılar, her barkodun parçacıklarda hangi sıklıkta göründüğünü hücrelerdeki sıklığıyla karşılaştırarak hangi gen bozulumlarının parçacık üretimini ve kargo paketlemeyi artırdığını veya azalttığını görebildiler. Çoğu mutasyonun etkisi azdı, çoğu durum işleri kötüleştirdi ve küçük ama önemli bir grup mutasyon eVLP’lerin performansını belirgin şekilde iyileştirdi veya bozdu.
Gen Susturma ve RNA Üretimi İçin Beklenmedik Roller
En güçlü “negatif” bulgulardan bazıları, HUSH kompleksi olarak bilinen bir gen susturma sisteminin parçasını oluşturan üç gen (MPP8, TASOR, MORC2) idi. Bu genler kapatıldığında, ortaya çıkan parçacıklar daha az kılavuz RNA taşıdı ve hücrelerde teslimat daha zayıf görüldü; bunun nedeni büyük ölçüde modifiye hücrelerde fazladan bulunan Cas9 proteinlerinin, paketlenmeden önce kılavuzları yakalamasıydı. Ancak hikaye daha nüanslıydı: HUSH kaybı aynı zamanda kargo proteininin üretimini de artırdı. Kargo, hücre genomuna stabil şekilde entegre edilmiş DNA’dan sağlandığında (geçici olarak eklenen plazmidlerden değil), bu ekstra protein aslında parçacık bileşenleri dengesini iyileştirerek belirgin şekilde daha güçlü gen düzenleme etkinliği sağladı. Başka bir deyişle, aynı genetik ayar üretim sistemi nasıl kurulduğuna bağlı olarak ya zarar verebilir ya da yardımcı olabilirdi.
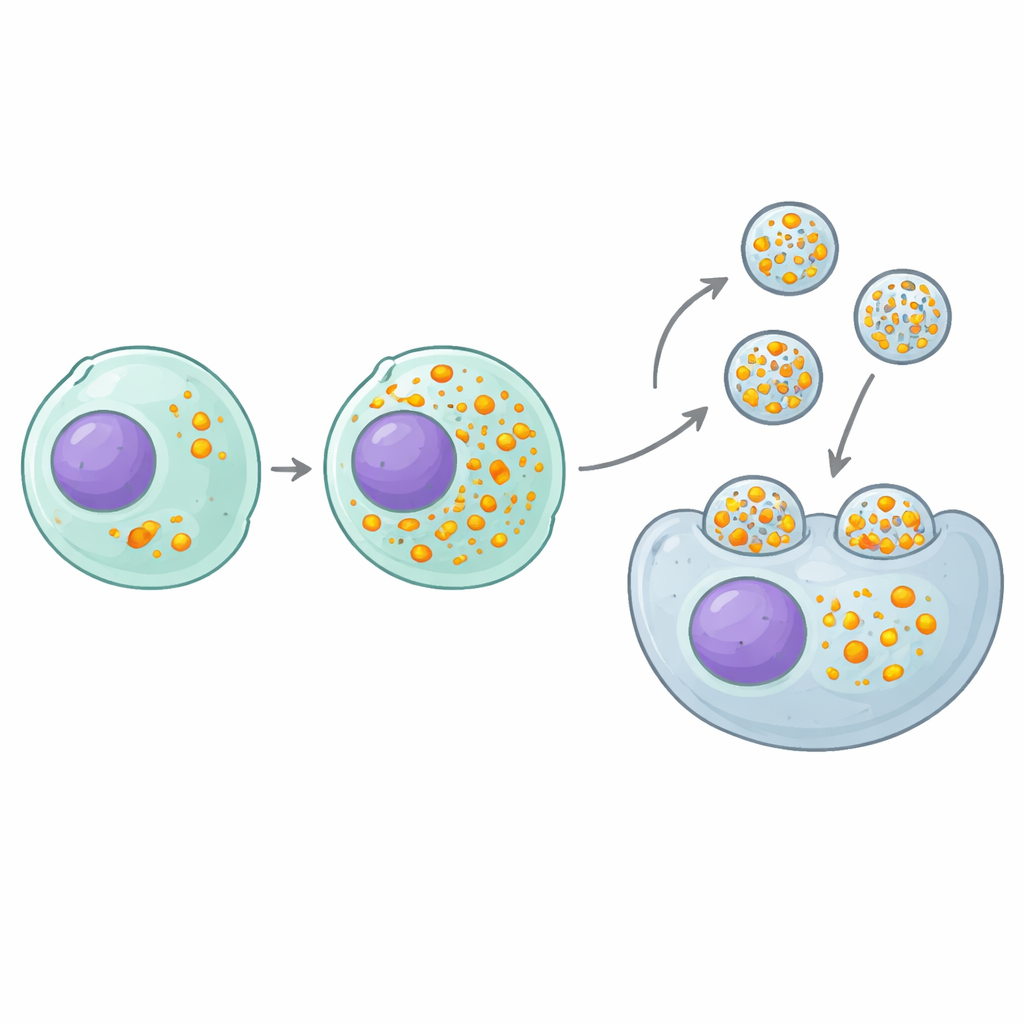
Her Parçacığa Daha Fazla Kargo Sığdıran Bir Anahtar Düğme
En umut verici “pozitif” bulgu, küçük RNA’ları üreten temel hücresel makine üzerinde doğal bir fren görevi gören MAF1 adlı bir gen oldu. CRISPR için kullanılan kılavuz RNA’lar bu makine tarafından üretildiği için MAF1 kaldırıldığında kılavuz RNA üretimi fiilen artmış olur. MAF1’den yoksun üretici hücreler, ürettikleri eVLP’lere her parçacık başına yaklaşık iki kat daha fazla kılavuz yükledi; bu, kaç parçacık yapıldığına veya her parçacığın taşıdığı protein miktarına dokunmadı. Bu durum, birçok farklı kılavuz dizisi, gen hedefi ve hücre tipi boyunca hücre kültüründe ve farelerde düzenleme etkinliğinde iki ila dokuz kat artışa dönüştü. Kritik olarak, fayda bu belirli eVLP tasarımının ötesine geçti: farklı iskeletler üzerine inşa edilmiş pek çok başka RNA–protein taşıyan parçacık sistemi de MAF1 eksik hücrelerde üretildiğinde daha etkili oldu.
Maksimum Etki İçin Stratejilerin Birleştirilmesi
Yazarlar, MAF1 kapanışının kılavuz RNA düzeylerini daha da yükseltmek için diğer hilelerle birlikte çalışıp çalışmayacağını da sordular. eVLP üretimi sırasında kullanılan standart plazmidlerin içine ekstra kılavuz RNA kasetleri yerleştirerek hücredeki genel DNA dengesini bozmayacak şekilde mevcut RNA miktarını artırdılar. Bu “++sgRNA” yaklaşımı ve MAF1 kapanışı her biri tek başına RNA paketlemeyi artırdı ve birlikte olduklarında etkileri toplamcıydı: parçacık içindeki Cas9 moleküllerinin doğru kılavuzlarla eşleşme oranı yaklaşık beşte birden yaklaşık yarıya yükseldi. Bu şekilde üretilen parçacıklar çalışmada görülen en yüksek gen düzenleme verimliliklerine ulaştı ve bunu aynı ya da daha düşük dozlarla yaptı.
Gelecekteki Gen Terapileri İçin Anlamı
Uzman olmayanlar için ana mesaj şudur: gen teslimatını iyileştirmek sadece daha iyi parçacıklar inşa etmekle ilgili değildir; onları üreten hücresel fabrikaları da yükseltmekle ilgilidir. Üretici hücrelerdeki her genin eVLP’lerin miktarını ve kalitesini nasıl etkilediğini eşleyerek bu çalışma, üreticilerin daha etkili partiler elde etmek için çevirebileceği pratik genetik “dümenleri” tanımlıyor. Özellikle MAF1-eksik hücreler, her parçacığa daha fazla aktif gen düzenleyici kargo güvenilir şekilde paketleyerek aynı terapötik etkiyi çok daha düşük dozlarda sağlayabiliyor. Gen düzenleme terapileri kliniğe doğru ilerlerken, bu tür üretici hücre mühendisliği tedavileri daha güvenli, daha verimli ve ölçeklenmesi daha kolay hale getirmek için güçlü ve esnek bir yol sunuyor.
Atıf: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Anahtar kelimeler: virüs benzeri parçacıklar, gen düzenleme teslimatı, üretici hücre mühendisliği, CRISPR terapötikleri, genom çapında tarama