Clear Sky Science · pt
Triagem em todo o genoma revela modificações nas células produtoras que melhoram a produção de partículas semelhantes a vírus e a potência de entrega
Por que veículos de entrega melhores importam
Ferramentas modernas de edição gênica como o CRISPR podem, em princípio, corrigir mutações causadoras de doenças na sua fonte, mas permanece um desafio central: como levar essas ferramentas moleculares de forma segura e eficiente às células certas, na quantidade certa e apenas pelo tempo necessário? Este estudo concentra-se em um veículo de entrega emergente chamado partículas semelhantes a vírus engenheiradas, ou eVLPs — cascas minúsculas e não infecciosas que podem transportar maquinário de edição gênica. Enquanto trabalhos anteriores ajustaram principalmente as partículas em si, este artigo faz uma pergunta diferente: e se reengenharmos as células vivas que fabricam as partículas para que cada lote já seja mais potente desde o início?
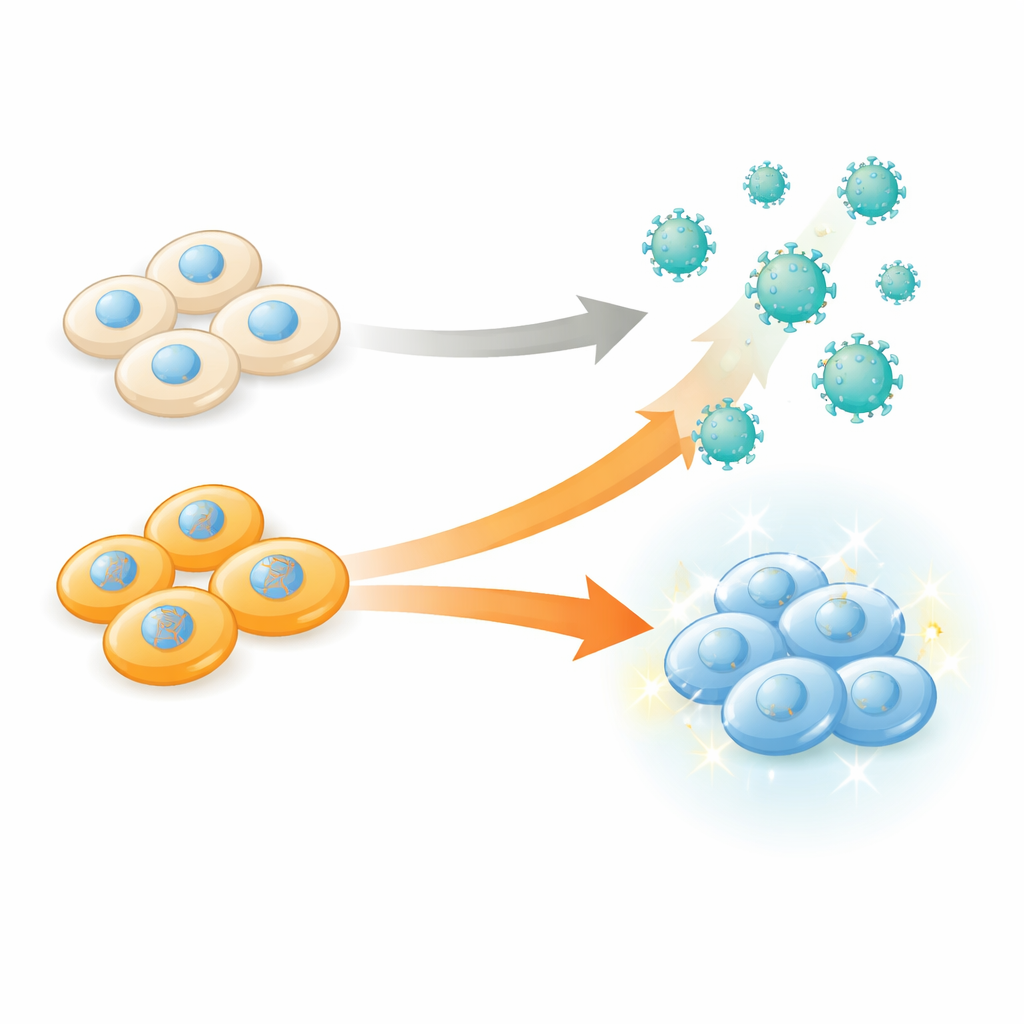
Reprogramando a fábrica, não apenas o produto
As eVLPs são produzidas por células humanas “produtoras” em laboratório, que montam proteínas da cápside viral e as carregam com carga de edição gênica antes de liberá-las no fluido circundante. Tradicionalmente, cientistas otimizaram os componentes e a arquitetura da partícula — mudando proteínas de cápside, fusões de carga ou moléculas de superfície — assumindo que as células produtoras eram apenas fábricas passivas. Os autores desafiaram essa visão testando sistematicamente como milhares de mudanças genéticas diferentes dentro das células produtoras alteram o número e a qualidade das eVLPs que elas liberam. O objetivo era simples, mas poderoso: identificar quais genes, quando desativados, tornam as células melhores em empacotar ferramentas de edição gênica dentro das partículas.
Uma busca em todo o genoma por ajustes úteis
Para executar essa busca maciça, a equipe usou uma biblioteca de CRISPR de “nocaute” em todo o genoma que interrompe quase todos os genes humanos. Cada célula produtora recebeu uma mutação guiada por um código de barras único de RNA, e porque as eVLPs naturalmente empacotam esses RNAs guias junto com a proteína de edição gênica, cada partícula carregava uma etiqueta molecular indicando qual alteração genética existia na célula que a produziu. Ao comparar com que frequência cada código de barras aparecia nas partículas versus nas próprias células, os pesquisadores puderam ver quais desativações gênicas aumentavam ou prejudicavam a produção de partículas e o carregamento de carga. A maioria das mutações teve pouco efeito, muitas pioraram a situação, e um conjunto pequeno, porém importante, melhorou ou prejudicou significativamente o desempenho das eVLPs.
Papéis inesperados para silenciamento gênico e produção de RNA
Entre os maiores resultados “negativos” estavam três genes (MPP8, TASOR, MORC2) que fazem parte de um sistema de silenciamento gênico conhecido como complexo HUSH. Quando esses genes foram nocauteados, as partículas resultantes carregavam menos RNAs guias e mostraram entrega mais fraca nas células, em grande parte porque o excesso de proteína Cas9 nas células modificadas capturou as guias antes que pudessem ser empacotadas. Ainda assim, a história foi mais sutil: a perda do HUSH também aumentou a produção da própria proteína de carga. Em situações em que a carga era fornecida a partir de DNA integrado de forma estável no genoma da célula (em vez de plasmídeos adicionados de forma transitória), essa proteína extra na verdade melhorou o equilíbrio dos componentes das partículas e levou a uma atividade de edição gênica marcadamente mais forte. Em outras palavras, o mesmo ajuste genético poderia tanto prejudicar quanto ajudar, dependendo de como o sistema de produção estava configurado.
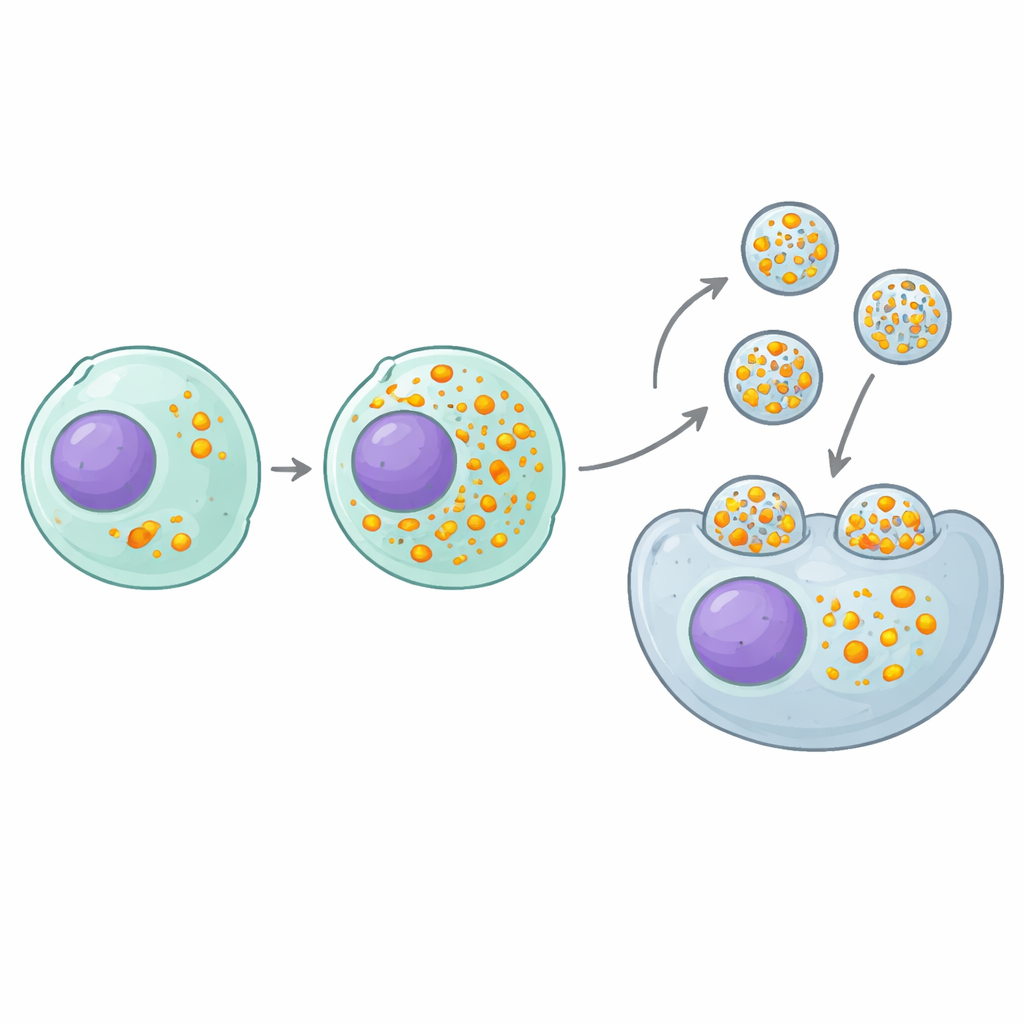
Um interruptor-chave que empacota mais carga por partícula
O resultado “positivo” mais promissor foi um gene chamado MAF1, um freio natural em uma máquina celular básica que produz pequenos RNAs. Os RNAs guias usados para o CRISPR são produzidos por essa máquina, então remover MAF1 efetivamente abre a torneira da produção de RNA guia. Células produtoras sem MAF1 carregaram aproximadamente o dobro de guias em cada eVLP sem alterar quantas partículas eram produzidas ou quanto de proteína cada partícula transportava. Isso se traduziu em um aumento de duas a nove vezes na potência de edição ao longo de muitas sequências guia diferentes, alvos gênicos e tipos celulares, tanto em cultura celular quanto em camundongos. Crucialmente, o benefício se estendeu além desse desenho específico de eVLP: vários outros sistemas de partículas que carregam RNA–proteína, construídos sobre plataformas diferentes, também se tornaram mais eficazes quando produzidos em células deficientes em MAF1.
Combinando estratégias para impacto máximo
Os autores então perguntaram se o nocaute de MAF1 poderia funcionar em conjunto com outros truques para aumentar ainda mais os níveis de RNA guia. Ao incorporar cassetes extras de RNA guia nos plasmídeos padrão usados durante a produção de eVLPs, eles aumentaram a quantidade de RNA disponível sem desequilibrar o balanço de DNA na célula. Essa abordagem “++sgRNA” e o nocaute de MAF1 cada um por si aumentaram o empacotamento de RNA, e juntos foram aditivos: a fração de moléculas de Cas9 dentro das partículas que estavam corretamente emparelhadas com guias aumentou de cerca de uma em cinco para cerca de uma em duas. Partículas produzidas dessa forma alcançaram as maiores eficiências de edição gênica observadas no estudo, tudo isso usando doses iguais ou até menores.
O que isso significa para futuras terapias gênicas
Para não especialistas, a mensagem chave é que melhorar a entrega gênica não é apenas sobre construir partículas melhores; trata-se também de atualizar as fábricas celulares que as produzem. Ao mapear como cada gene nas células produtoras influencia a quantidade e a qualidade das eVLPs, este trabalho identifica “botões” genéticos práticos que os fabricantes podem girar para obter lotes mais potentes. Células deficientes em MAF1, em particular, empacotam de forma confiável mais da carga ativa de edição gênica em cada partícula, permitindo o mesmo efeito terapêutico com doses muito menores. À medida que as terapias de edição gênica avançam rumo à clínica, essa engenharia das células produtoras oferece uma maneira poderosa e flexível de tornar os tratamentos mais seguros, mais eficientes e mais fáceis de escalar.
Citação: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Palavras-chave: partículas semelhantes a vírus, entrega para edição gênica, engenharia de células produtoras, terapêuticas CRISPR, triagem em todo o genoma