Clear Sky Science · he
סקר ברמת הגנום חושף שינויים בתאי המייצרים שמשפרים ייצור ונשיאת חלקיקים דמויי-וירוס
מדוע חשובים כלי העברה טובים יותר
כלי עריכת גנים מודרניים כמו CRISPR יכולים, בעקרון, לתקן מוטציות שגורמות למחלות במקורותיהן, אבל אתגר מרכזי נותר: כיצד להעביר את הכלים המולקולריים האלה לתאים הנכונים באופן בטוח ויעיל, בכמות הנכונה, ובמשך הזמן הנדרש בלבד? המחקר הזה מתמקד בכלי העברה חדש יחסית שנקרא חלקיקים דמויי-וירוס מהונדסים (eVLPs) — מעטפות זעירות, לא מדבקות, שיכולות לשאת את מכניקת עריכת הגנים. בעוד שעבודות קודמות עסקו בעיקר בכיוונון החלקיקים עצמם, המאמר הזה שואל שאלה שונה: מה אם נמהנד מחדש את התאים החיים שמייצרים את החלקיקים כך שכל אצווה תהיה עוצמתית יותר מלכתחילה?
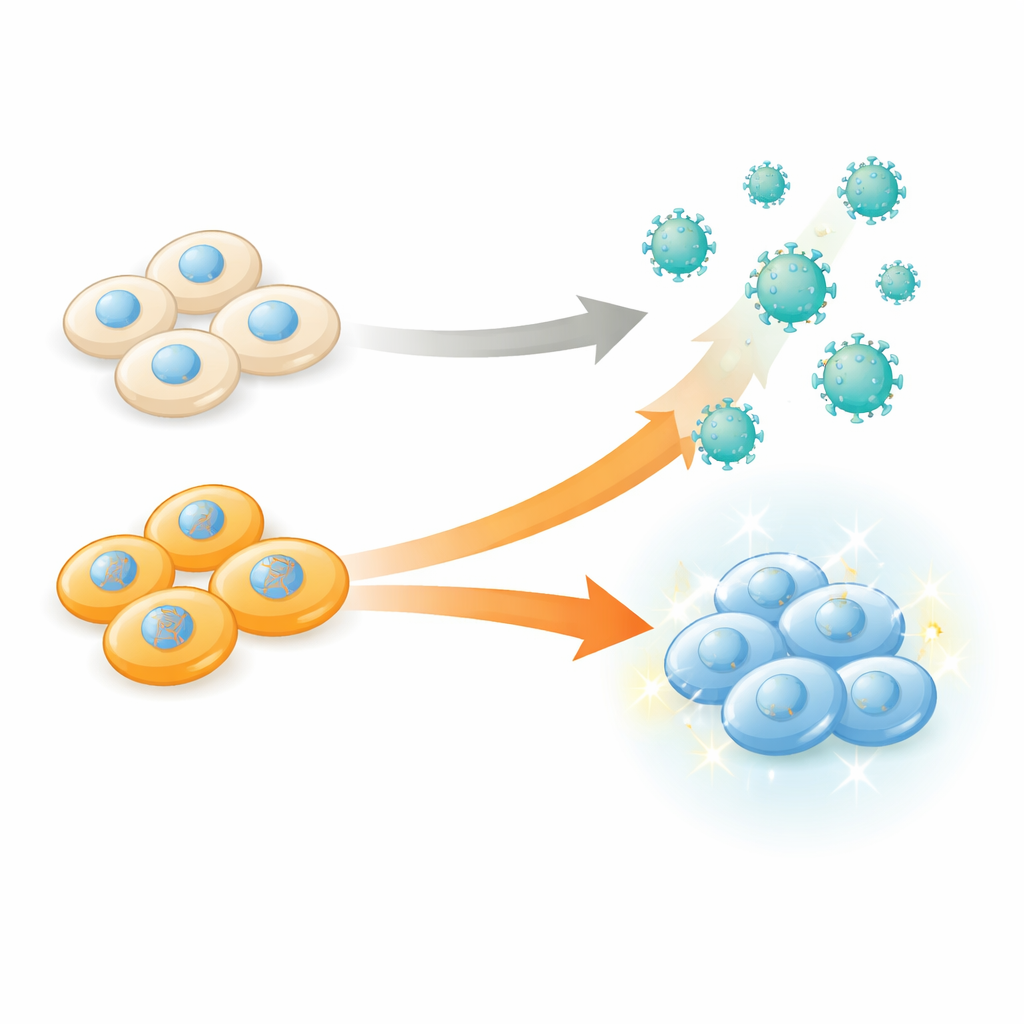
לתכנת את המפעל, לא רק את המוצר
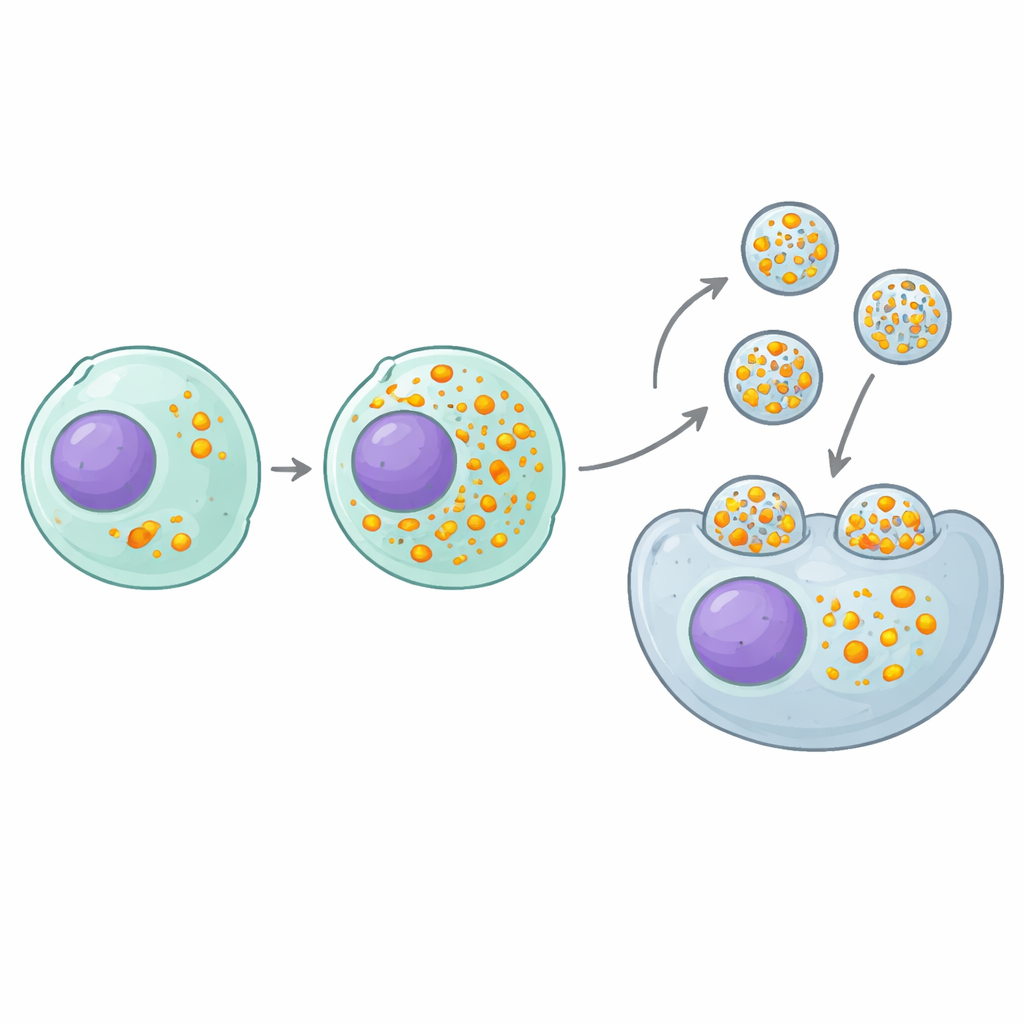
eVLPs מיוצרים על ידי תאי "יצרן" אנושיים במעבדה, שבונים חלבוני מעטפת וטעונים אותם במטען של עריכת גנים לפני שהם משחררים אותם לנוזל שמקיף אותם. באופן מסורתי, המדענים שיפרו את מרכיבי החלקיק והארכיטקטורה שלו — שינו חלבוני מעטפת, איחויים של מטען, או מולקולות על פני השטח — תוך הנחה שהתאים המייצרים הם רק מפעלים פסיביים. המחברים אתגרו את ההנחה הזו על ידי בדיקה שיטתית של אלפי שינויים גנטיים שונים בתוך תאי היצרן וכיצד הם משפיעים על כמות ואיכות ה-eVLPs שמשתחררים. המטרה שלהם הייתה פשוטה אך עוצמתית: לזהות אילו גנים, כאשר מכבים אותם, משפרים את היכולת של התאים לארוז כלים לעריכת גנים לתוך החלקיקים.
חיפוש רחב היקף אחרי שינויים מועילים
כדי להריץ את החיפוש ההמוני הזה, הצוות השתמש בספריית CRISPR "נוקאאוט" ברמת הגנום שמפריעה כמעט לכל גן אנושי. כל תא יצרן קיבל מוטציה מונחית על ידי ברקוד RNA ייחודי, ומכיוון ש-eVLPs אוטומטית אורזים גם את מדריכי ה-RNA יחד עם חלבון העריכה, כל חלקיק נשא תג מולקולרי שהצביע על איזו שינויית גנטית התקיימה בתא שייצר אותו. על ידי השוואת תדירות הופעת כל ברקוד בחלקיקים לעומת בתאים עצמם, החוקרים יכלו לראות אילו הפרעות גנטיות הגבירו או פגעו בייצור החלקיקים ובעריפת המטען. רוב המוטציות לא השפיעו הרבה, רבות הורעו את המצב, וקבוצה קטנה אך חשובה שיפרה או פגמה משמעותית את ביצועי ה-eVLPs.
תפקידים בלתי צפויים לדיכוי גנים ולייצור RNA
בין ההשפעות "הנמוכות" החזקות היו שלושה גנים (MPP8, TASOR, MORC2) שהם חלק ממערכת דיכוי גנים הידועה כקומפלקס HUSH. כאשר גנים אלה נותקו, החלקיקים שנוצרו נשאו פחות מדריכי RNA והראו הובלה חלשה יותר בתאים, בעיקר כי עודף חלבון Cas9 בתאים המותאמים תפס את המדריכים לפני שהם הספיקו להיארז. עם זאת, הסיפור היה מורכב יותר: אובדן HUSH הגדיל גם את ייצור חלבון המטען עצמו. במצבים שבהם המטען סופק מ-DNA המוטמע באופן יציב בגנום התא (ולא מפלסמידים שחדרו באופן חולף), החלבון הנוסף הזה שיפר למעשה את היחס בין מרכיבי החלקיק והוביל לפעילות עריכה חזקה משמעותית. במילים אחרות, אותו שינוי גנטי יכול לפגוע או לעזור, בהתאם לאופן שבו מערכת הייצור הוגדרה.
מתג מרכזי שמארז יותר מטען בכל חלקיק
הממצא החיובי המבטיח ביותר היה גן בשם MAF1, מעצור טבעי על מכונה תאית בסיסית שמייצרת RNAs קטנים. מדריכי ה-RNA שמשמשים ל-CRISPR מיוצרים על ידי המכונה הזו, לכן השמטת MAF1 מגדילה למעשה את הזרימה של ייצור מדריכי ה-RNA. תאי יצרן חסרי MAF1 טענו בערך כפול מדריכים בכל eVLP מבלי לשנות את כמות החלקיקים שהם ייצרו או כמה חלבון כל חלקיק נשא. הדבר תורגם להגברה של פי שניים עד תשעה בעוצמת העריכה עבור רצפי מדריך, מטרות גנטיות וסוגי תאים רבים, הן בתרבית תאים והן בעכברים. באופן מכריע, היתרון התפרס מעבר לעיצוב eVLP המסוים הזה: מספר מערכות נשיאת RNA–חלבון אחרות, שנבנו על שלד שונה, כללו שיפור ביעילות כאשר יוצרו בתאים חסרי MAF1.
שילוב אסטרטגיות להשפעה מקסימלית
המחברים בדקו האם נוקאאוט של MAF1 יכול לעבוד בשילוב עם טריקים אחרים כדי להעלות עוד יותר את רמות מדריך ה-RNA. על ידי החדרת קסטות נוספות של מדריך RNA לפלסמידים הסטנדרטיים המשמשים בייצור eVLP, הם הגדילו את כמות ה-RNA הזמינה מבלי להפר את שיווי המשקל הכולל של ה-DNA בתא. הגישה הזו של "++sgRNA" ונוקאאוט MAF1 כל אחת מהן הגבירה בנפרד את אריזת ה-RNA, וביחד הן השפיעו בצורת סכימה: החלק היחסי של מולקולות Cas9 בתוך החלקיקים שהיו מצמדות כראוי למדריכים עלה מכ־אחד בחמישה לכ־אחד בשניים. חלקיקים שיוצרו כך השיגו את היעילות הגבוהה ביותר של עריכת גנים שנצפתה במחקר, תוך שימוש באותן מינונים או במינונים נמוכים יותר.
מה המשמעות לכך עבור טיפולי גנים עתידיים
ללא-מומחים, המסר המרכזי הוא ששיפור העברת הגנים אינו רק עניין של בניית חלקיקים טובים יותר; זה גם עניין של שדרוג מפעלי התאים שמייצרים אותם. על ידי מיפוי כיצד כל גן בתאי היצרן משפיע על כמות ואיכות ה-eVLPs, עבודה זו מזהה "כפתורים" גנטיים מעשיים שמייצרים יכולים לסובב כדי לקבל אצוות עוצמתיות יותר. תאים חסרי MAF1, במיוחד, נארזים באמינות ביותר את המטען הפעיל של עריכת הגנים בכל חלקיק, מה שמאפשר את אותה השפעה תרפויטית במינונים נמוכים בהרבה. ככל שתרפיות עריכת גנים מתקדמות לעבר הקליניקה, הנדסת תאי היצרן מציעה דרך חזקה וגמישה להפוך טיפולים לבטוחים, יעילים וקלים יותר להרחבה.
ציטוט: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
מילות מפתח: חלקיקים דמויי-וירוס, העברת עריכת גנים, הנדסת תאי יצרן, תרפיית CRISPR, סקר ברמת הגנום