Clear Sky Science · fr
Un criblage à l’échelle du génome révèle des modifications des cellules productrices qui améliorent la production de particules de type viral et leur puissance de délivrance
Pourquoi des vecteurs de livraison meilleurs comptent
Les outils modernes d’édition génétique comme CRISPR peuvent, en principe, corriger les mutations responsables de maladies à la source, mais un défi central subsiste : comment acheminer ces outils moléculaires de manière sûre et efficace vers les bonnes cellules, à la bonne dose, et seulement pour la durée nécessaire ? Cette étude se concentre sur un vecteur de livraison émergent appelé particules de type viral ingénierées, ou eVLP — de minuscules coquilles non infectieuses capables de transporter la machinerie d’édition génétique. Alors que les travaux antérieurs ont principalement ajusté les particules elles-mêmes, cet article pose une question différente : et si l’on réingénierait les cellules vivantes qui fabriquent les particules pour que chaque lot soit plus puissant dès le départ ?
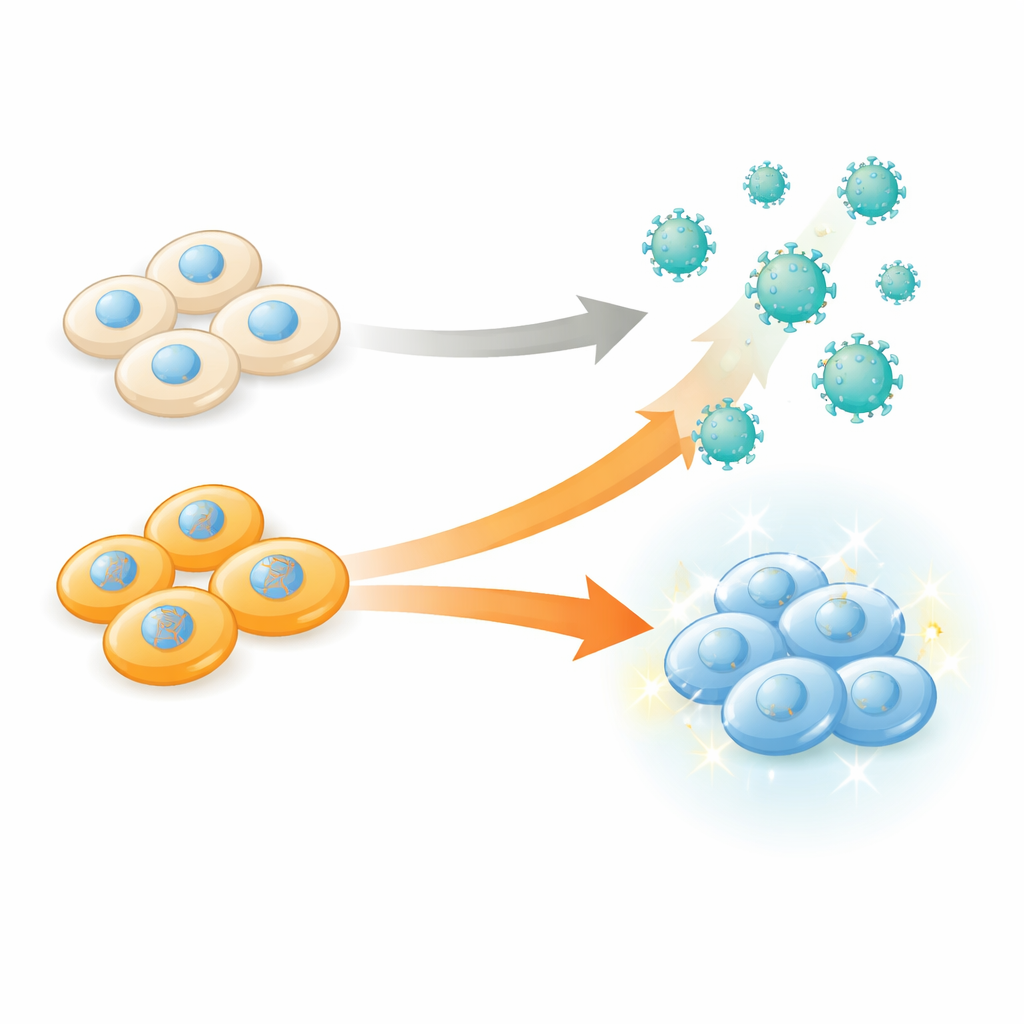
Reprogrammer l’usine, pas seulement le produit
Les eVLP sont produits en laboratoire par des cellules humaines « productrices », qui assemblent les protéines de l’enveloppe virale et les chargent avec le cargaison d’édition génétique avant de les libérer dans le milieu. Traditionnellement, les chercheurs ont optimisé les composants et l’architecture des particules — en modifiant les protéines de l’enveloppe, les fusions de cargaison ou les molécules de surface — en supposant que les cellules productrices n’étaient que des usines passives. Les auteurs remettent en question cette vision en testant systématiquement comment des milliers de modifications génétiques différentes à l’intérieur des cellules productrices modifient le nombre et la qualité des eVLP qu’elles libèrent. Leur objectif était simple mais puissant : identifier quels gènes, lorsqu’ils sont inactivés, rendent les cellules meilleures pour empaqueter les outils d’édition génétique dans les particules.
Une recherche à l’échelle du génome pour des ajustements utiles
Pour mener cette recherche massive, l’équipe a utilisé une bibliothèque CRISPR de type « knockout » à l’échelle du génome qui perturbe presque tous les gènes humains. Chaque cellule productrice a reçu une mutation guidée par un code-barres ARN unique, et parce que les eVLP empaquettent naturellement ces ARN guides avec la protéine d’édition, chaque particule portait une étiquette moléculaire indiquant quelle modification génétique existait dans la cellule qui l’avait produite. En comparant la fréquence d’apparition de chaque code-barres dans les particules par rapport aux cellules elles‑mêmes, les chercheurs pouvaient voir quelles disruptions génétiques stimulaient ou nuisaient à la production de particules et au chargement du cargo. La plupart des mutations avaient peu d’effet, beaucoup aggravaient les choses, et un petit mais important ensemble améliorait ou détériorait significativement les performances des eVLP.
Rôles inattendus de la répression génique et de la production d’ARN
Parmi les « hits » négatifs les plus marquants figuraient trois gènes (MPP8, TASOR, MORC2) qui font partie d’un système de répression génique connu sous le nom de complexe HUSH. Lorsque ces gènes étaient inactivés, les particules résultantes contenaient moins d’ARN guides et montraient une délivrance plus faible dans les cellules, essentiellement parce qu’un excès de protéine Cas9 dans les cellules modifiées capturait les guides avant qu’ils ne puissent être empaquetés. Mais l’histoire était plus nuancée : la perte du HUSH augmentait aussi la production de la protéine cargo elle‑même. Dans les situations où le cargo était fourni à partir d’ADN intégré de façon stable dans le génome de la cellule (plutôt qu’à partir de plasmides ajoutés de façon transitoire), cette protéine supplémentaire améliorait en réalité l’équilibre des composants des particules et conduisait à une activité d’édition génétique sensiblement renforcée. Autrement dit, la même modification génétique pouvait soit nuire, soit aider, selon la façon dont le système de production était configuré.
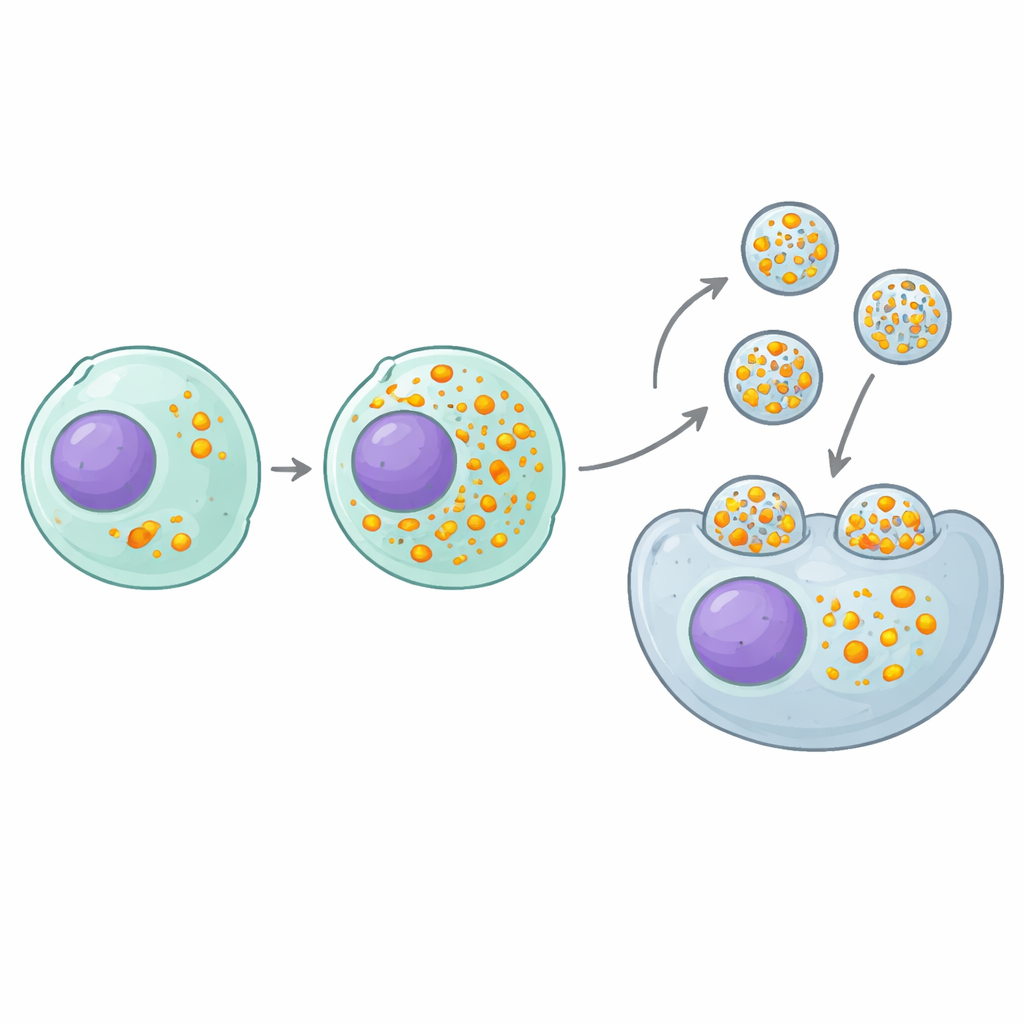
Un interrupteur clé qui emballe plus de cargaison par particule
Le « hit » positif le plus prometteur était un gène appelé MAF1, une bride naturelle sur une machinerie cellulaire basique qui fabrique de petits ARN. Les ARN guides utilisés pour CRISPR sont produits par cette machinerie, donc supprimer MAF1 équivaut à ouvrir le robinet de la production d’ARN guides. Les cellules productrices dépourvues de MAF1 ont chargé environ deux fois plus de guides dans chaque eVLP sans changer le nombre de particules produites ni la quantité de protéine portée par chaque particule. Cela s’est traduit par une augmentation de la puissance d’édition comprise entre deux et neuf fois selon les séquences guides, les cibles génétiques et les types cellulaires, à la fois en culture cellulaire et chez la souris. De façon cruciale, le bénéfice dépassait ce design d’eVLP particulier : plusieurs autres systèmes de particules transportant ARN–protéine, construits sur des échafaudages différents, sont devenus plus efficaces lorsqu’ils étaient produits dans des cellules déficientes en MAF1.
Combiner les stratégies pour un impact maximal
Les auteurs ont ensuite cherché à savoir si l’inactivation de MAF1 pouvait fonctionner de concert avec d’autres astuces pour augmenter encore davantage les niveaux d’ARN guides. En intégrant des cassettes supplémentaires d’ARN guides dans les plasmides standard utilisés pendant la production des eVLP, ils ont augmenté la quantité d’ARN disponible sans perturber l’équilibre global de l’ADN dans la cellule. Cette approche « ++sgRNA » et l’inactivation de MAF1 ont chacune augmenté le conditionnement de l’ARN de manière autonome, et ensemble elles étaient additives : la fraction de molécules de Cas9 à l’intérieur des particules correctement appariées avec des guides est passée d’environ une sur cinq à environ une sur deux. Les particules produites de cette façon ont atteint les efficacités d’édition les plus élevées observées dans l’étude, tout en utilisant des doses égales ou même plus faibles.
Ce que cela signifie pour les thérapies géniques futures
Pour les non‑spécialistes, le message clé est que l’amélioration de la délivrance génétique ne se limite pas à concevoir de meilleures particules ; il s’agit aussi d’optimiser les usines cellulaires qui les fabriquent. En cartographiant comment chaque gène des cellules productrices influence la quantité et la qualité des eVLP, ce travail identifie des « boutons » génétiques pratiques que les fabricants peuvent actionner pour obtenir des lots plus puissants. Les cellules déficientes en MAF1, en particulier, emballent de manière fiable davantage de cargaison active d’édition génétique dans chaque particule, permettant le même effet thérapeutique à des doses bien plus faibles. À mesure que les thérapies d’édition génétique progressent vers la clinique, l’ingénierie des cellules productrices offre un moyen puissant et flexible de rendre les traitements plus sûrs, plus efficaces et plus faciles à industrialiser.
Citation: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Mots-clés: particules de type viral, livraison pour édition génomique, ingénierie des cellules productrices, thérapeutiques CRISPR, criblage à l’échelle du génome