Clear Sky Science · pl
Przesiew genome-wide ujawnia modyfikacje komórek-producentów, które poprawiają produkcję i skuteczność dostarczania cząstek podobnych do wirusów
Dlaczego lepsze nośniki dostawy mają znaczenie
Nowoczesne narzędzia edycji genów, takie jak CRISPR, w zasadzie mogą naprawiać powodujące choroby mutacje u ich źródła, ale wciąż pozostaje kluczowe wyzwanie: jak bezpiecznie i wydajnie wprowadzić te molekularne narzędzia do właściwych komórek, we właściwej ilości i tylko na potrzebny czas? W tym badaniu skupiono się na nowym nośniku dostawy zwanym zaprojektowanymi cząstkami podobnymi do wirusów (eVLP) — maleńkich, nieinfekcyjnych osłonkach, które mogą przenosić aparaturę do edycji genów. Podczas gdy wcześniejsze prace głównie optymalizowały same cząstki, w tym artykule zadano inne pytanie: co jeśli przeprojektujemy żywe komórki, które wytwarzają cząstki, tak aby każda partia była od początku bardziej aktywna?
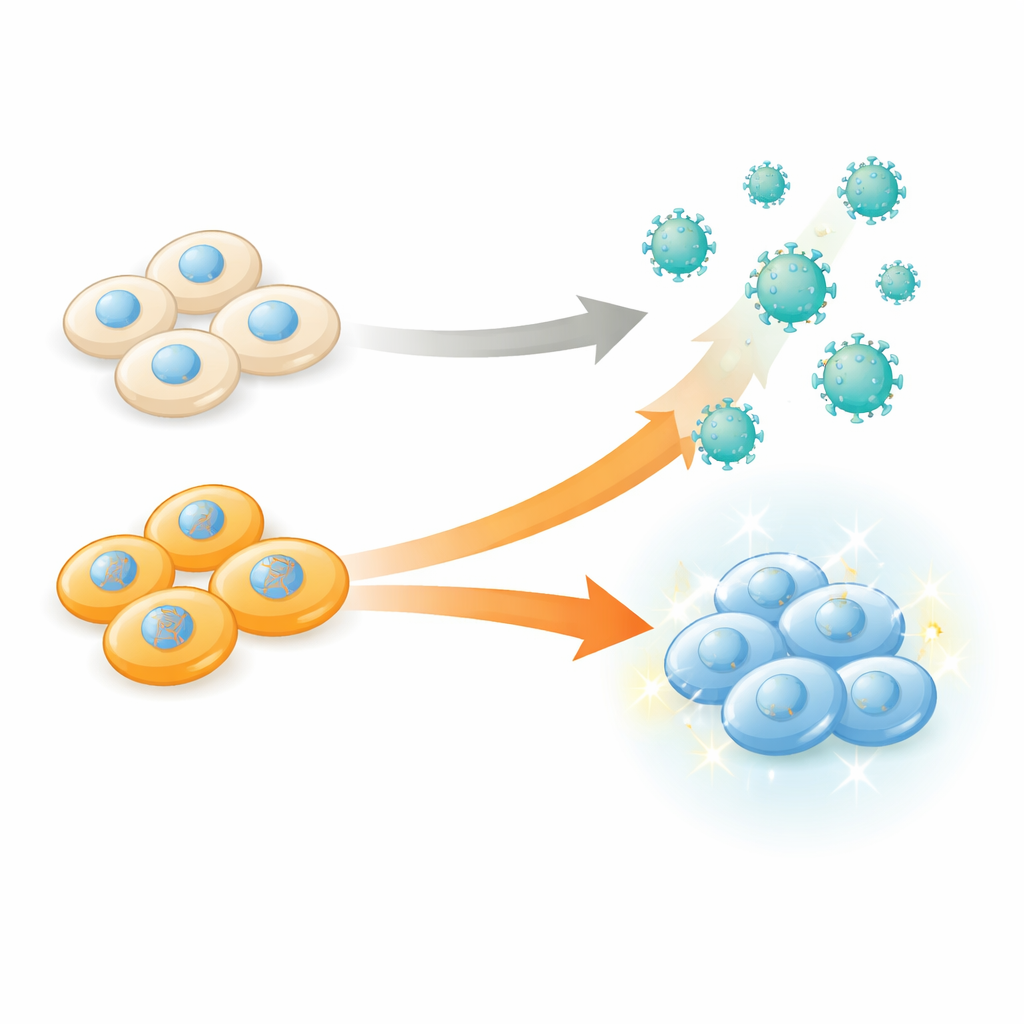
Przeprogramowanie fabryki, a nie tylko produktu
eVLP są produkowane w laboratorium przez ludzkie komórki „producenckie”, które składają białka osłonowe wirusa i ładują je ładunkiem edycji genów, zanim uwolnią je do otaczającego płynu. Tradycyjnie naukowcy optymalizowali komponenty i architekturę cząstek — zmieniając białka osłony, fuzje ładunku czy cząsteczki powierzchniowe — przy założeniu, że komórki-producenci są jedynie biernymi fabrykami. Autorzy zakwestionowali to podejście, systematycznie testując, jak tysiące różnych zmian genetycznych wewnątrz komórek-producentów wpływają na liczbę i jakość wydawanych eVLP. Ich cel był prosty, lecz silny: zidentyfikować, które geny, po wyłączeniu, sprawiają, że komórki lepiej pakują narzędzia do edycji genów w cząstki.
Poszukiwanie pomocnych modyfikacji w skali całego genomu
Aby przeprowadzić to masowe przeszukanie, zespół użył biblioteki CRISPR „knockout” obejmującej niemal każdy gen ludzki. Każda komórka-producer otrzymała mutację kierowaną przez unikatowy pasek RNA, a ponieważ eVLP naturalnie pakują te prowadzące RNA razem z białkiem edycji genów, każda cząstka niosła znak molekularny wskazujący, która zmiana genetyczna istniała w komórce ją wytwarzającej. Porównując, jak często każdy pasek pojawiał się w cząstkach w porównaniu z samymi komórkami, badacze mogli zobaczyć, które zaburzenia genów zwiększały lub zmniejszały produkcję cząstek i załadunek ładunku. Większość mutacji miała niewielki efekt, wiele pogarszało sytuację, a niewielki, lecz istotny zestaw znacząco poprawiał lub upośledzał wydajność eVLP.
Niespodziewane role wyciszania genów i produkcji RNA
Wśród najsilniejszych „negatywnych” trafień znalazły się trzy geny (MPP8, TASOR, MORC2), które wchodzą w skład układu wyciszania genów znanego jako kompleks HUSH. Gdy te geny zostały wyłączone, powstałe cząstki niosły mniej prowadzących RNA i wykazywały słabsze dostarczanie do komórek, głównie dlatego, że nadmiar białka Cas9 w zmodyfikowanych komórkach wiązał prowadzące RNA zanim mogły zostać zapakowane. Historia była jednak bardziej zniuansowana: utrata funkcji HUSH także zwiększała produkcję samego białka ładunku. W sytuacjach, gdy ładunek pochodził z DNA trwale zintegrowanego z genomem komórki (zamiast z przejściowo dostarczanych plazmidów), dodatkowe białko faktycznie poprawiało proporcje komponentów cząstki i prowadziło do wyraźnie silniejszej aktywności edycyjnej. Innymi słowy, ta sama modyfikacja genetyczna mogła zaszkodzić lub pomóc, w zależności od konfiguracji systemu produkcji.
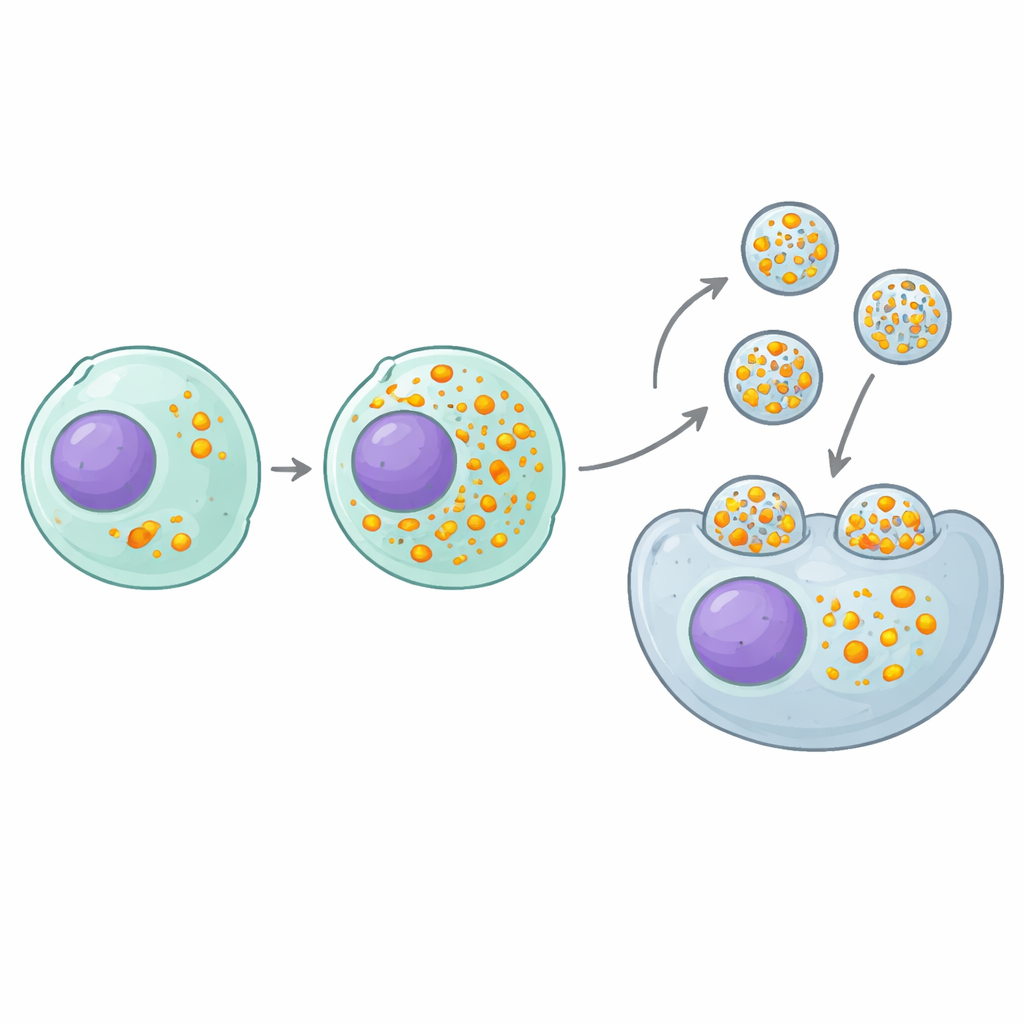
Kluczowy przełącznik, który pakuje więcej ładunku na cząstkę
Najbardziej obiecującym „pozytywnym” trafieniem był gen o nazwie MAF1, naturalny hamulec dla podstawowego mechanizmu komórkowego produkującego małe RNA. Prowadzące RNA używane w CRISPR są wytwarzane przez ten mechanizm, więc usunięcie MAF1 skutecznie zwiększa produkcję prowadzących RNA. Komórki-producenci pozbawione MAF1 ładowały w przybliżeniu dwukrotnie więcej prowadzących do każdej eVLP bez zmiany liczby wytwarzanych cząstek ani ilości białka przenoszonego przez każdą cząstkę. Przekładało się to na dwukrotny do dziewięciokrotnego wzrostu mocy edycji w wielu różnych sekwencjach prowadzących, celach genowych i typach komórek, zarówno w hodowlach komórkowych, jak i u myszy. Co ważne, korzyść wykraczała poza ten konkretny projekt eVLP: kilka innych systemów przenoszących RNA–białko, zbudowanych na różnych rusztowaniach, również stało się bardziej skutecznych, gdy były produkowane w komórkach pozbawionych MAF1.
Łączenie strategii dla maksymalnego efektu
Następnie autorzy zapytali, czy knockout MAF1 może współdziałać z innymi sztuczkami podnoszącymi poziomy prowadzącego RNA jeszcze bardziej. Poprzez osadzenie dodatkowych kaset prowadzących RNA w standardowych plazmidach używanych podczas produkcji eVLP, zwiększyli ilość dostępnego RNA bez zaburzania ogólnej równowagi DNA w komórce. Podejście „++sgRNA” oraz knockout MAF1 każdy z osobna zwiększały pakowanie RNA, a razem dawały efekt addytywny: odsetek cząsteczek Cas9 wewnątrz cząstek poprawnie sparowanych z prowadzącymi wzrósł z około jednej na pięć do około jednej na dwie. Cząstki wytworzone w ten sposób osiągnęły najwyższą efektywność edycji genów zaobserwowaną w badaniu, przy użyciu tych samych lub nawet niższych dawek.
Co to oznacza dla przyszłych terapii genowych
Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że poprawa dostarczania genów to nie tylko budowanie lepszych cząstek; to także unowocześnianie komórkowych fabryk, które je wytwarzają. Mapując, jak każdy gen w komórkach-producentach wpływa na ilość i jakość eVLP, praca ta identyfikuje praktyczne „pokrętła” genetyczne, które producenci mogą regulować, by uzyskać silniejsze partie. Szczególnie komórki pozbawione MAF1 niezawodnie pakują więcej aktywnego ładunku edycji genów do każdej cząstki, pozwalając osiągnąć ten sam efekt terapeutyczny przy znacznie niższych dawkach. W miarę jak terapie edycji genów trafiają do kliniki, taka inżynieria komórek-producentów oferuje potężny i elastyczny sposób na uczynienie terapii bezpieczniejszymi, wydajniejszymi i łatwiejszymi do skalowania.
Cytowanie: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Słowa kluczowe: cząstki podobne do wirusów, dostarczanie edycji genów, inżynieria komórek-producentów, terapie CRISPR, przesiew genome-wide