Clear Sky Science · es
Cribado a escala genómica revela modificaciones en células productoras que mejoran la producción y la potencia de entrega de partículas tipo virus
Por qué importan mejores vehículos de entrega
Las herramientas modernas de edición genética como CRISPR pueden, en principio, corregir mutaciones causantes de enfermedad en su origen, pero sigue existiendo un problema central: ¿cómo introducimos estas herramientas moleculares de forma segura y eficaz en las células correctas, en la cantidad adecuada y solo durante el tiempo necesario? Este estudio se centra en un vehículo de entrega emergente llamado partículas tipo virus diseñadas (eVLPs): cápsulas diminutas y no infecciosas que pueden transportar la maquinaria de edición genética. Mientras que trabajos previos se han enfocado principalmente en afinar las partículas en sí, este artículo plantea una pregunta distinta: ¿y si reingeniamos las células vivas que fabrican las partículas para que cada lote sea más potente desde el origen?
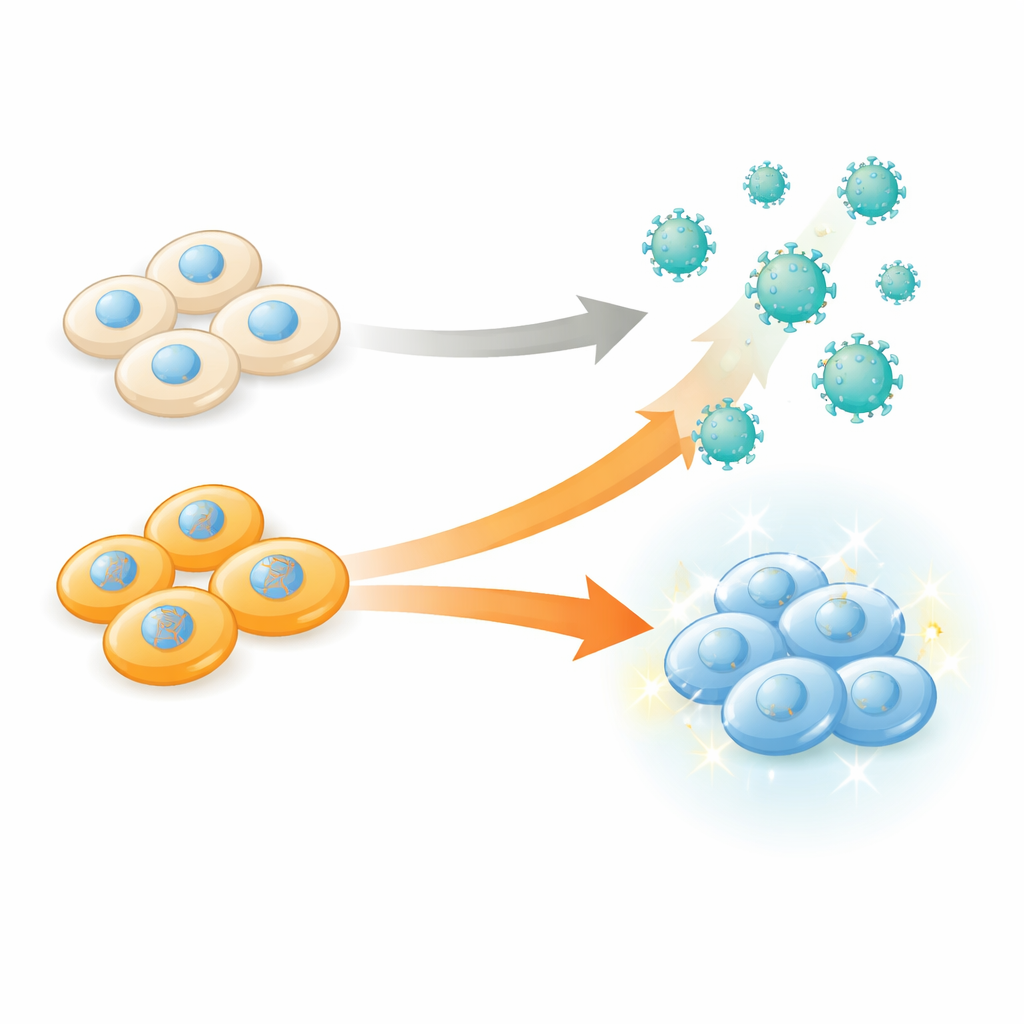
Reprogramar la fábrica, no solo el producto
Las eVLPs se producen en el laboratorio por células humanas “productoras”, que ensamblan las proteínas de la cápside viral y las cargan con la carga de edición genética antes de liberarlas al medio. Tradicionalmente, los científicos han optimizado los componentes y la arquitectura de la partícula—cambiando proteínas de la cápside, fusiones de la carga o moléculas de superficie—dando por hecho que las células productoras son meras fábricas pasivas. Los autores cuestionaron esta visión probando de forma sistemática cómo miles de cambios genéticos distintos dentro de las células productoras alteran la cantidad y la calidad de eVLPs que liberan. Su objetivo era simple pero potente: identificar qué genes, cuando se inactivan, hacen que las células empaqueten mejor las herramientas de edición genética en las partículas.
Una búsqueda a escala genómica de ajustes útiles
Para llevar a cabo esta búsqueda masiva, el equipo usó una biblioteca CRISPR de “knockout” a escala genómica que interrumpe casi todos los genes humanos. Cada célula productora recibió una mutación guiada por un código de barras de ARN único y, puesto que las eVLPs empaquetan de forma natural estos ARN guías junto con la proteína de edición, cada partícula llevaba una etiqueta molecular que indicaba qué cambio genético existía en la célula que la produjo. Comparando la frecuencia con la que aparecía cada código de barras en las partículas frente a en las propias células, los investigadores pudieron ver qué interrupciones genéticas aumentaban o dañaban la producción de partículas y la carga. La mayoría de las mutaciones tuvieron poco efecto, muchas empeoraron las cosas, y un pequeño pero importante conjunto mejoró o perjudicó de forma significativa el rendimiento de las eVLPs.
Roles inesperados del silenciamiento génico y la producción de ARN
Entre los aciertos “negativos” más destacados estaban tres genes (MPP8, TASOR, MORC2) que forman parte de un sistema de silenciamiento génico conocido como complejo HUSH. Cuando se eliminaron estos genes, las partículas resultantes llevaban menos ARN guías y mostraron una entrega más débil en las células, en gran parte porque el exceso de proteína Cas9 en las células modificadas capturaba las guías antes de que pudieran empaquetarse. Sin embargo, la historia fue más matizada: la pérdida de HUSH también aumentó la producción de la propia proteína de carga. En situaciones en las que la carga se suministraba desde ADN integrado de forma estable en el genoma de la célula (en lugar de plasmidos añadidos de forma transitoria), esta proteína adicional mejoró en realidad el equilibrio de los componentes de la partícula y condujo a una actividad de edición genética notablemente más fuerte. Dicho de otro modo, la misma modificación genética podía perjudicar o ayudar, dependiendo de cómo se configurara el sistema de producción.
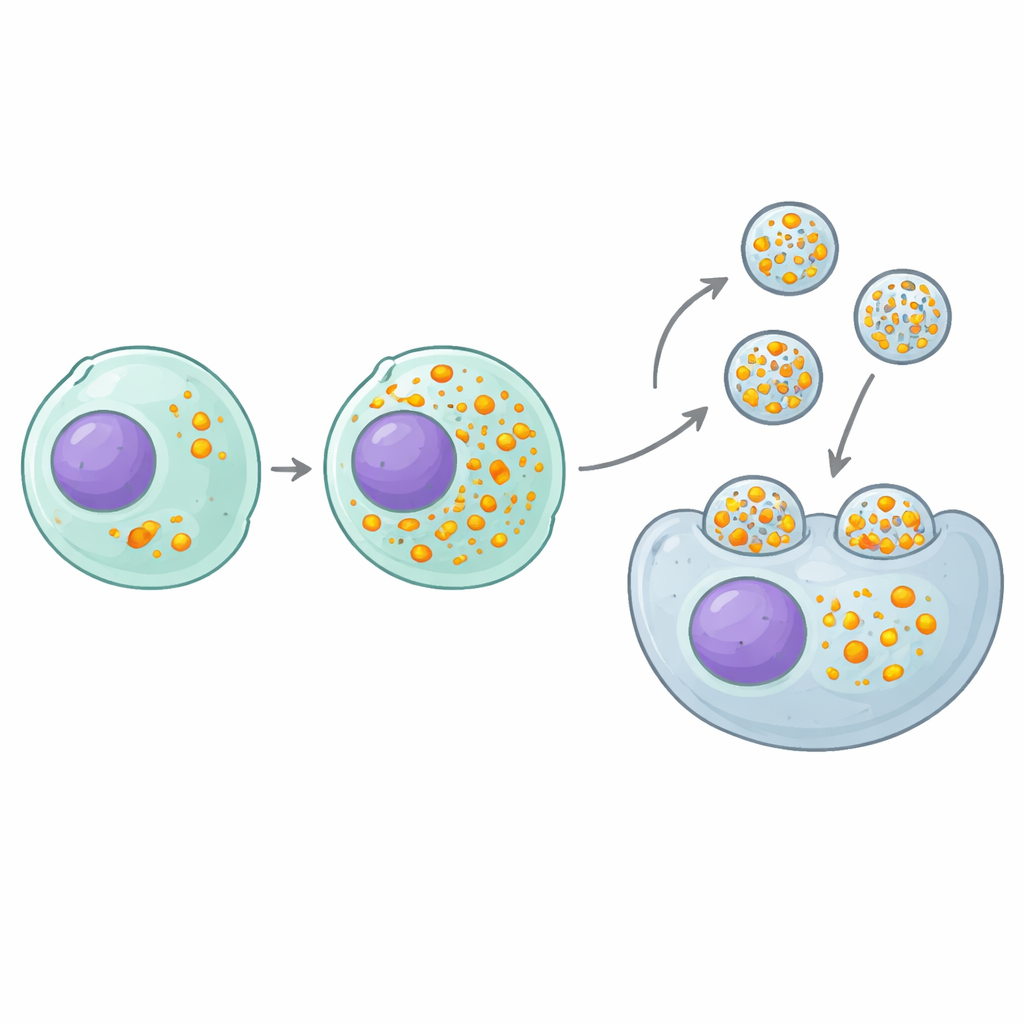
Un interruptor clave que empaqueta más carga por partícula
El hallazgo “positivo” más prometedor fue un gen llamado MAF1, un freno natural sobre una maquinaria celular básica que produce ARN pequeños. Los ARN guías usados para CRISPR se generan mediante esta maquinaria, por lo que eliminar MAF1 equivale a abrir el grifo de la producción de ARN guía. Las células productoras carentes de MAF1 cargaron aproximadamente el doble de guías en cada eVLP sin cambiar cuántas partículas producían ni cuánto proteína llevaba cada partícula. Esto se tradujo en un aumento de la potencia de edición de entre dos y nueve veces a lo largo de muchas secuencias guía distintas, objetivos génicos y tipos celulares, tanto en cultivo celular como en ratones. Críticamente, el beneficio se extendió más allá de este diseño particular de eVLP: varios otros sistemas de partículas que transportan complejos ARN–proteína, construidos sobre andamiajes diferentes, también se volvieron más eficaces cuando se produjeron en células deficientes en MAF1.
Combinar estrategias para un impacto máximo
Los autores preguntaron a continuación si el knockout de MAF1 podía funcionar junto con otras tácticas para aumentar aún más los niveles de ARN guía. Insertando cassettes adicionales de ARN guía en los plasmidos estándar usados durante la producción de eVLPs, aumentaron la cantidad de ARN disponible sin alterar el equilibrio total de ADN en la célula. Este enfoque “++sgRNA” y el knockout de MAF1 cada uno aumentaron por separado el empaquetamiento de ARN, y juntos fueron aditivos: la fracción de moléculas de Cas9 dentro de las partículas que estaban correctamente emparejadas con guías pasó de aproximadamente una de cada cinco a cerca de una de cada dos. Las partículas fabricadas de esta manera alcanzaron las eficiencias de edición génica más altas observadas en el estudio, todo ello usando las mismas dosis o incluso dosis más bajas.
Qué significa esto para futuras terapias génicas
Para quienes no son especialistas, el mensaje clave es que mejorar la entrega génica no se trata solo de construir mejores partículas; también consiste en actualizar las fábricas celulares que las producen. Al mapear cómo cada gen en las células productoras influye en la cantidad y la calidad de las eVLPs, este trabajo identifica “perillas” genéticas prácticas que los fabricantes pueden ajustar para obtener lotes más potentes. Las células deficientes en MAF1, en particular, empaquetan de forma fiable más carga activa de edición genética en cada partícula, permitiendo el mismo efecto terapéutico con dosis mucho más bajas. A medida que las terapias de edición genética avanzan hacia la clínica, la ingeniería de células productoras ofrece una vía potente y flexible para hacer los tratamientos más seguros, eficaces y escalables.
Cita: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Palabras clave: partículas tipo virus, entrega de edición genética, ingeniería de células productoras, terapéutica CRISPR, cribado a escala genómica