Clear Sky Science · ar
مسح شامل عبر الجينوم يكشف تعديلات في خلايا المُنتِج تُحسِّن إنتاج جسيمات شبيهة بالفيروس وقدرة التوصيل
لماذا تهم ناقلات التوصيل الأفضل
يمكن لأدوات تعديل الجينات الحديثة مثل كريسبر، من حيث المبدأ، إصلاح الطفرات المسببة للأمراض عند مصدرها، لكن يبقى تحدٍّ أساسي: كيف نوصل هذه الأدوات الجزيئية بأمان وكفاءة إلى الخلايا الصحيحة، بكميات مناسبة، ولمدة زمنية محدودة فقط؟ تركز هذه الدراسة على ناقل توصيل ناشئ يُسمى الجسيمات المهندَسة الشبيهة بالفيروس (eVLPs) — أُغشية صغيرة غير مُعدية قادرة على حمل آليات تعديل الجينات. بينما ركزت الأعمال السابقة بشكل أساسي على تعديل الجسيمات نفسها، تطرح هذه الورقة سؤالًا مختلفًا: ماذا لو أعدنا هندسة الخلايا الحية التي تصنع الجسيمات بحيث تكون كل دفعة أقوى من البداية؟
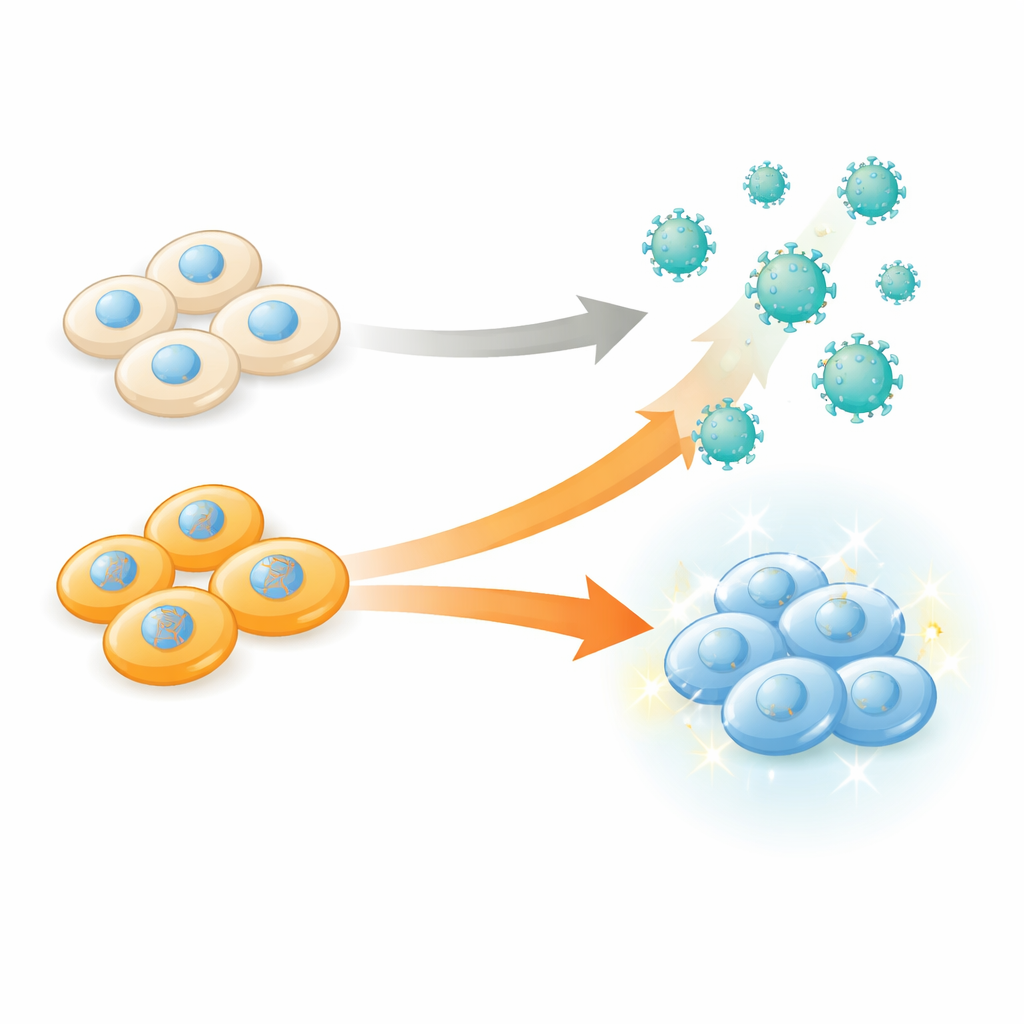
إعادة برمجة المصنع، وليس المنتج فقط
يتم إنتاج eVLPs بواسطة خلايا بشرية «مُنتِجة» في المختبر، حيث تجمع بروتينات الغلاف الفيروسي وتحشوها بحمولات تعديل الجينات قبل إطلاقها في السائل المحيط. تقليديًا، قام العلماء بتحسين مكونات وبنية الجسيم — بتغيير بروتينات الغلاف أو رباطات الحمولة أو جزيئات السطح — مع افتراض أن خلايا المُنتِج مجرد مصانع خاملة. تحدى المؤلفون هذا التصور عبر اختبار منهجي لكيفية تأثير آلاف التغييرات الجينية المختلفة داخل خلايا المُنتِج على عدد وجودة eVLPs التي تطلقها. كان هدفهم بسيطًا لكنه قويًا: تحديد أي الجينات، عند إيقافها، تجعل الخلايا أفضل في تعبئة أدوات تعديل الجينات داخل الجسيمات.
بحث شامل عبر الجينوم عن تعديلات مفيدة
لتنفيذ هذا البحث الضخم، استخدم الفريق مكتبة تعطيل جيني CRISPR شاملة تعطل تقريبًا كل جين بشري. تلقّت كل خلية مُنتِجة طفرة تُوجَّه بواسطة شريط RNA فريد، ولأن eVLPs تقوم بطبيعتها بتعبئة هذه إرشادات الدليل (guide RNAs) إلى جانب بروتين تعديل الجينات، حمل كل جسيم وسمًا جزيئيًا يشير إلى التغيير الجيني الذي وُجد في الخلية المصنِّعة له. بمقارنة مدى تواتر ظهور كل شريط في الجسيمات مقابل ظهوره في الخلايا نفسها، تمكن الباحثون من رؤية أي تعطيلات جينية عززت أو أضرت بإنتاج الجسيمات وتحميل الحمولة. كان لمعظم الطفرات أثر ضئيل، وكثير منها زاد الأمور سوءًا، ومجموعة صغيرة لكن مهمة حسّنت أو أضعفت أداء eVLPs بشكل ملحوظ.
أدوار غير متوقعة لكبت الجينات وإنتاج الحمض النووي الريبوزي
من بين أقوى الضربات «السلبية» كانت ثلاثة جينات (MPP8، TASOR، MORC2) تشكّل جزءًا من نظام كبت الجينات المعروف باسم مركب HUSH. عندما تم تعطيل هذه الجينات، حملت الجسيمات الناتجة عددًا أقل من إرشادات الدليل وأظهرت توصيلًا أضعف في الخلايا، ويرجع ذلك إلى حد كبير إلى أن فائض بروتين Cas9 في الخلايا المعدَّلة استولى على الأدلة قبل أن تُغَلَّف. لكن القصة كانت أكثر تعقيدًا: فقد أدى فقدان HUSH أيضًا إلى زيادة إنتاج بروتين الحمولة نفسه. في الحالات التي كانت فيها الحمولة مُقدمة من DNA مدمج بشكل ثابت في جينوم الخلية (بدلًا من البلازميدات المضافة مؤقتًا)، حسّن هذا البروتين الإضافي فعليًا توازن مكونات الجسيم وأدى إلى نشاط تعديل جيني أقوى بشكل ملحوظ. بعبارة أخرى، نفس التعديل الجيني قد يُضر أو يُفيد اعتمادًا على كيفية إعداد نظام الإنتاج.
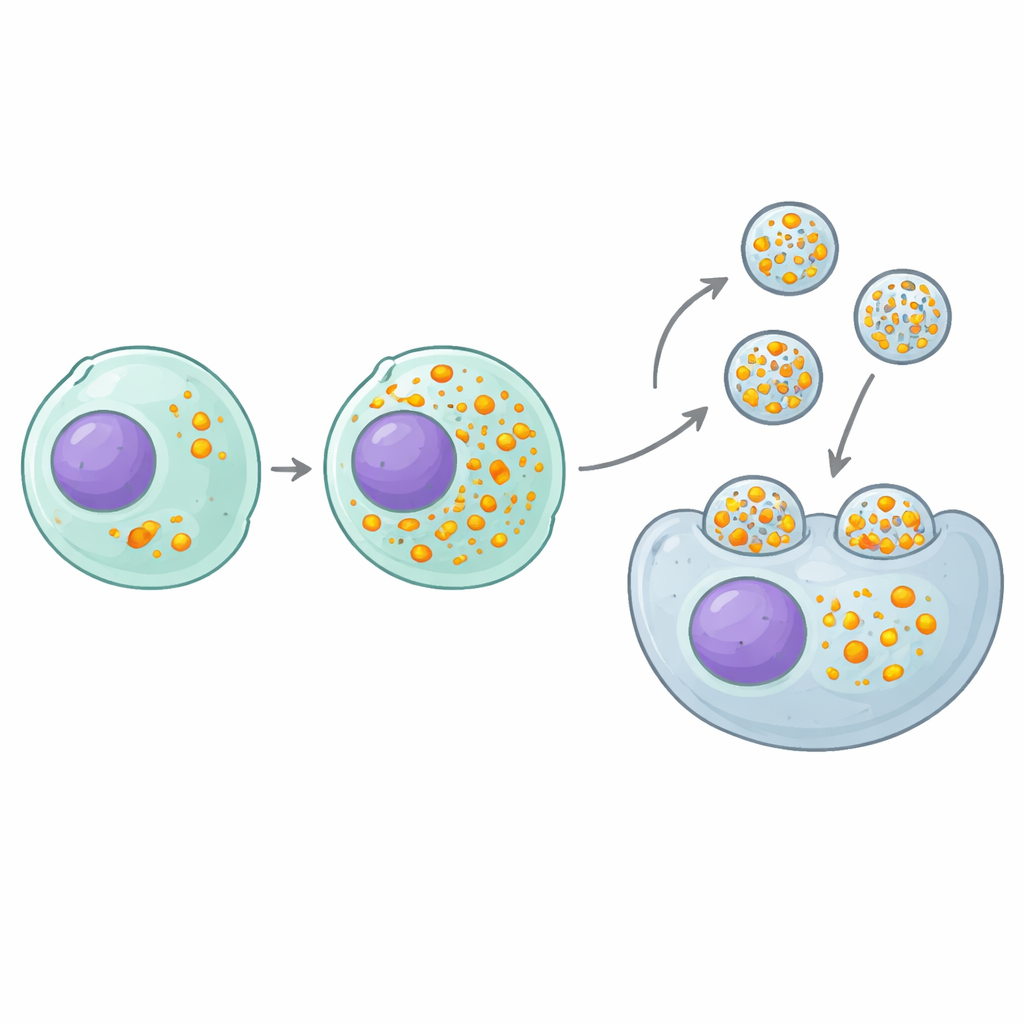
مفتاح رئيسي يعبئ حمولة أكثر لكل جسيم
كانت الضربة «الإيجابية» الأكثر واعدة جينًا يُدعى MAF1، وهو فرامل طبيعية لآلة خلوية أساسية تصنع الحمض النووي الريبوزي الصغير. تُنتَج إرشادات الدليل المستخدمة في كريسبر بواسطة هذه الآلة، لذا فإن إزالة MAF1 تفتح صنبور إنتاج إرشادات الدليل. حمّلت خلايا المُنتِج التي تفتقر إلى MAF1 نحو ضعف عدد الأدلة في كل eVLP دون تغيير عدد الجسيمات المُنتَجة أو مقدار البروتين الذي يحمله كل جسيم. تُرجم هذا إلى تعزيز في الفعالية التحريرية بمقدار يتراوح بين ضعفين وتسعة أضعاف عبر تسلسلات أدلة مختلفة، أهداف جينية وأنواع خلايا متعددة، سواء في زراعة الخلايا أو في الفئران. والأهم، أن الفائدة امتدت إلى ما بعد تصميم eVLP هذا بعينه: فقد أصبحت عدة أنظمة أخرى لحمل RNA–بروتين، مبنية على هياكل مختلفة، أكثر فعالية عندما نُنتِجها في خلايا ناقصة MAF1.
دمج استراتيجيات لتحقيق تأثير أقصى
سأل المؤلفون بعد ذلك ما إذا كان تعطيل MAF1 يمكن أن يعمل بالتوازي مع حيل أخرى لرفع مستويات إرشادات الدليل أكثر. من خلال تضمين كاسيتات إضافية لإرشادات الدليل داخل البلازميدات القياسية المستخدمة أثناء إنتاج eVLP، زادوا كمية RNA المتاحة دون إزعاج التوازن الكلي للـDNA في الخلية. نهجا «++sgRNA» وتعطيل MAF1 كل منهما على حدة عززا تعبئة RNA، ومعًا كانا إضافيين: ارتفعت نسبة جزيئات Cas9 داخل الجسيمات التي كانت مقترنة بشكل صحيح مع الأدلة من نحو واحد من كل خمسة إلى نحو واحد من كل اثنين. حققت الجسيمات المصنوعة بهذه الطريقة أعلى كفاءات تعديل جيني لوحظت في الدراسة، وكل ذلك مع استخدام نفس الجرعات أو جرعات أقل.
ما الذي يعنيه هذا لعلاجات تعديل الجينات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن تحسين توصيل الجينات ليس مجرد بناء جسيمات أفضل؛ بل يتعلق أيضًا بترقية مصانع الخلايا التي تصنعها. من خلال رسم خريطة كيفية تأثير كل جين في خلايا المُنتِج على كمية وجودة eVLPs، تُحدد هذه العملة «مقابض» جينية عملية يمكن للمصنِّعين قلبها للحصول على دفعات أكثر فاعلية. خلايا ناقصة MAF1، على وجه الخصوص، تعبئ بثبات المزيد من الحمولة الفعالة لتعديل الجينات في كل جسيم، مما يسمح بنفس التأثير العلاجي بجرعات أقل بكثير. ومع تقدم علاجات تعديل الجينات نحو العيادات، توفر هندسة خلايا المُنتِج هذه وسيلة قوية ومرنة لجعل العلاجات أكثر أمانًا وكفاءة وأسهل في التوسع.
الاستشهاد: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
الكلمات المفتاحية: جسيمات شبيهة بالفيروس, توصيل تحرير الجينات, هندسة خلايا المُنتِج, العلاجات القائمة على كريسبر, مسح شامل عبر الجينوم