Clear Sky Science · de
Genomweite Suche zeigt Produzenten-Zellmodifikationen, die Produktion und Wirksamkeit von virusähnlichen Partikeln verbessern
Warum bessere Transportvehikel wichtig sind
Moderne Geneditierungswerkzeuge wie CRISPR können im Prinzip krankheitsverursachende Mutationen an ihrer Quelle korrigieren, aber eine zentrale Herausforderung bleibt: Wie bringen wir diese molekularen Werkzeuge sicher und effizient in die richtigen Zellen, in der richtigen Menge und nur so lange, wie nötig? Diese Studie konzentriert sich auf ein sich abzeichnendes Liefervehikel, sogenannte engineered virus-like particles oder eVLPs — winzige, nicht-infektiöse Hüllen, die Geneditierungswerkzeuge transportieren können. Während frühere Arbeiten hauptsächlich die Partikel selbst optimierten, stellt dieses Paper eine andere Frage: Was, wenn wir die lebenden Zellen, die die Partikel herstellen, neu gestalten, sodass jede Charge von Anfang an potenter ist?
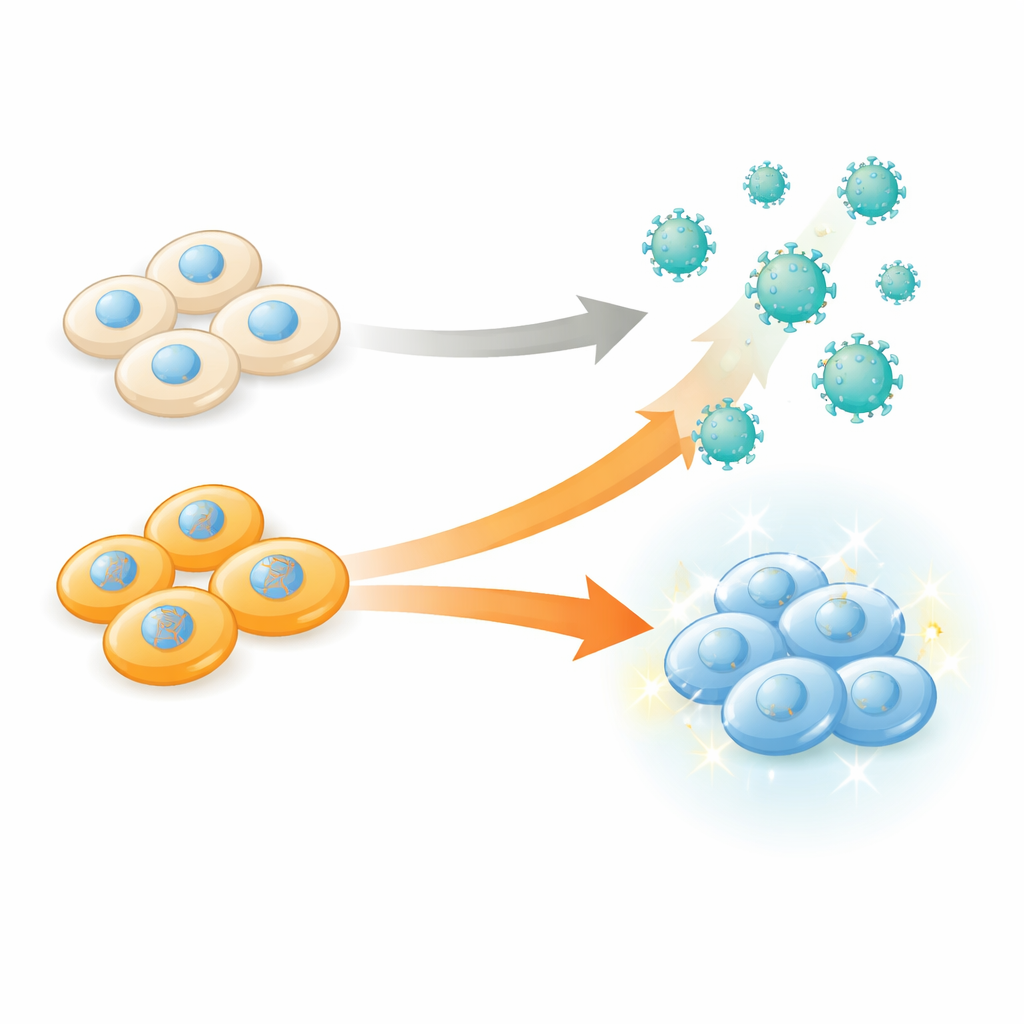
Die Fabrik umprogrammieren, nicht nur das Produkt
eVLPs werden im Labor von menschlichen „Produzenten“-Zellen hergestellt, die virale Hüllproteine zusammenbauen und mit Geneditierungsfracht beladen, bevor sie in das umgebende Medium freigesetzt werden. Traditionell haben Forscher die Komponenten und die Architektur der Partikel optimiert — etwa Hüllproteine, Fusionskonstrukte des Cargos oder Oberflächenmoleküle — und die Produzenten-Zellen als passive Fabriken betrachtet. Die Autoren hinterfragten diese Sichtweise, indem sie systematisch testeten, wie tausende unterschiedliche genetische Veränderungen in den Produzenten-Zellen die Anzahl und Qualität der freigesetzten eVLPs beeinflussen. Ihr Ziel war einfach, aber wirkungsvoll: herauszufinden, welche Gene durch Abschalten die Zellen besser darin machen, Geneditierungswerkzeuge in Partikeln zu verpacken.
Eine genomweite Suche nach nützlichen Anpassungen
Um diese umfangreiche Suche durchzuführen, nutzte das Team eine genomweite CRISPR-„Knockout“-Bibliothek, die nahezu jedes menschliche Gen stört. Jede Produzentenzelle erhielt eine Mutation, die durch eine einzigartige RNA-Barcode-Anleitung gesteuert wurde, und da eVLPs diese Guide-RNAs zusammen mit dem Geneditierungsprotein natürlicherweise einpacken, trug jedes Partikel einen molekularen Tag, der anzeigte, welche genetische Veränderung in der Zelle vorlag, die es produziert hatte. Indem die Forscher verglichen, wie häufig jeder Barcode in den Partikeln gegenüber den Zellen selbst vorkam, konnten sie erkennen, welche Gen-Störungen die Partikelproduktion und das Beladen der Fracht förderten oder schadeten. Die meisten Mutationen hatten wenig Effekt, viele verschlechterten die Dinge, und eine kleine, aber wichtige Gruppe verbesserte oder beeinträchtigte die Leistung der eVLPs deutlich.
Unerwartete Rollen für Gen-Silencing und RNA-Produktion
Zu den stärksten negativen Treffern gehörten drei Gene (MPP8, TASOR, MORC2), die Teil eines Gen-Silencing-Systems sind, das als HUSH-Komplex bekannt ist. Wenn diese Gene ausgeschaltet wurden, trugen die resultierenden Partikel weniger Guide-RNAs und zeigten eine schwächere Lieferung in Zellen — hauptsächlich weil überschüssiges Cas9-Protein in den modifizierten Zellen die Guides ergriff, bevor sie verpackt werden konnten. Die Geschichte war jedoch nuanciert: Der Verlust von HUSH erhöhte auch die Produktion des Cargo-Proteins selbst. In Situationen, in denen das Cargo aus DNA stammt, die stabil ins Zellgenom integriert ist (statt aus transient eingebrachten Plasmiden), verbesserte dieses zusätzliche Protein tatsächlich die Balance der Partikelkomponenten und führte zu deutlich stärkeren Geneditierungsaktivitäten. Mit anderen Worten: Derselbe genetische Eingriff konnte je nach Produktionssystem entweder schaden oder nützen.
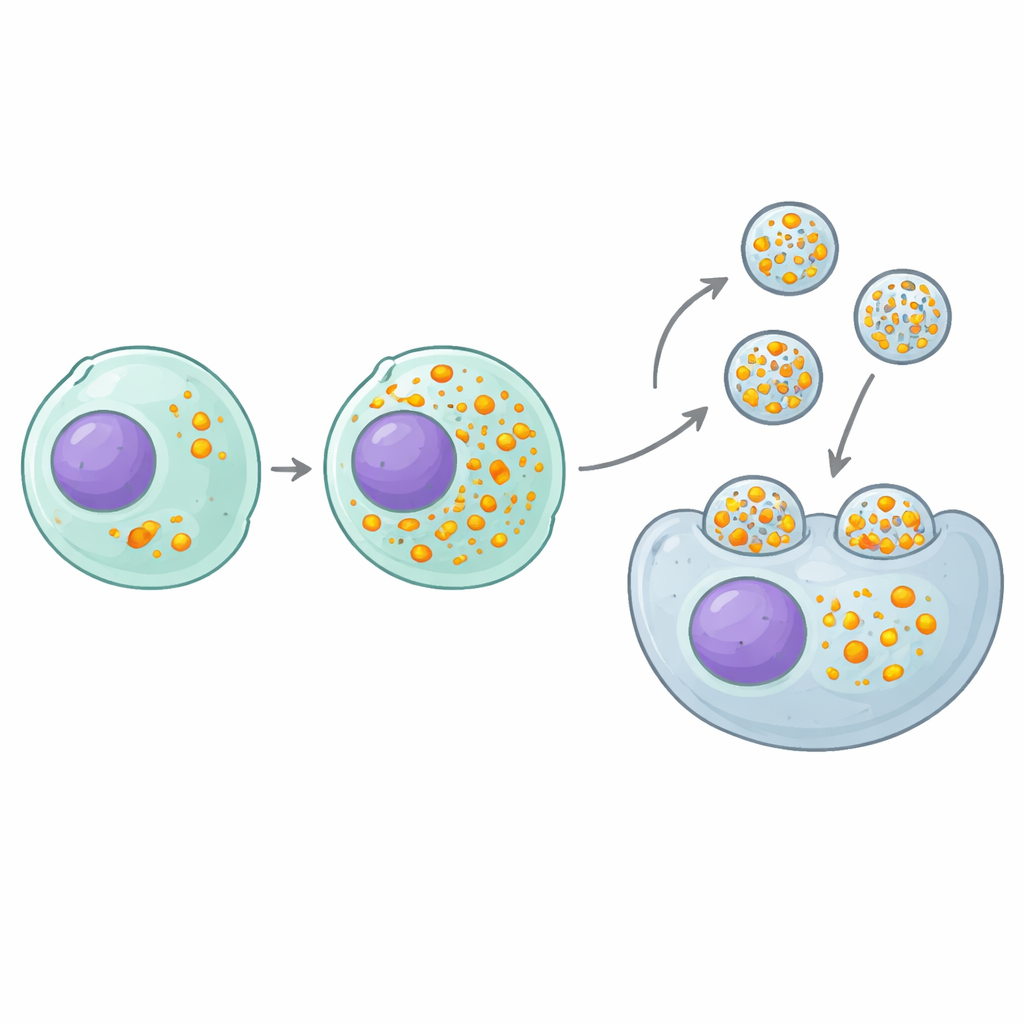
Ein Schalter, der mehr Fracht pro Partikel verpackt
Der vielversprechendste positive Treffer war ein Gen namens MAF1, eine natürliche Bremse eines grundlegenden zellulären Mechanismus, der kleine RNAs herstellt. Die für CRISPR verwendeten Guide-RNAs werden von diesem Mechanismus produziert, sodass das Entfernen von MAF1 effektiv den Hahn für die Guide-RNA-Produktion aufdreht. Produzentenzellen ohne MAF1 luden etwa doppelt so viele Guides in jedes eVLP, ohne die Anzahl der hergestellten Partikel oder die Proteinmenge pro Partikel zu verändern. Dies übersetzte sich in eine zwei- bis neunfache Steigerung der Editier-Wirksamkeit über viele verschiedene Guide-Sequenzen, Zielgene und Zelltypen, sowohl in Zellkultur als auch in Mäusen. Entscheidend ist, dass der Nutzen über dieses spezielle eVLP-Design hinausging: Mehrere andere RNA–Protein-tragende Partikelsysteme, die auf unterschiedlichen Gerüsten basieren, wurden ebenfalls wirksamer, wenn sie in MAF1-defizienten Zellen produziert wurden.
Strategien kombinieren für maximale Wirkung
Die Autoren fragten anschließend, ob ein MAF1-Knockout mit anderen Tricks zusammenwirken könne, um die Guide-RNA-Spiegel noch weiter zu erhöhen. Durch Einbetten zusätzlicher Guide-RNA-Kassetten in die Standardplasmide, die während der eVLP-Produktion verwendet werden, erhöhten sie die verfügbare RNA-Menge, ohne das gesamte DNA-Gleichgewicht der Zelle zu stören. Dieser „++sgRNA“-Ansatz und der MAF1-Knockout steigerten jeweils für sich die RNA-Verpackung, und zusammen waren sie additiv: Der Anteil der Cas9-Moleküle innerhalb der Partikel, der korrekt mit Guides gepaart war, stieg von etwa einem von fünf auf etwa einen von zwei. Auf diese Weise hergestellte Partikel erreichten die höchsten in der Studie beobachteten Geneditierungseffizienzen, und das bei gleichen oder sogar niedrigeren Dosen.
Was das für zukünftige Gen‑Therapien bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft: Die Verbesserung der Genlieferung geht nicht nur darum, bessere Partikel zu bauen; es geht auch darum, die zellulären Fabriken, die sie herstellen, aufzurüsten. Indem diese Arbeit kartiert, wie jedes Gen in Produzenten-Zellen die Menge und Qualität von eVLPs beeinflusst, identifiziert sie praktische genetische „Regler“, die Hersteller drehen können, um potenteren Chargen zu erzielen. Besonders MAF1-defiziente Zellen packen zuverlässig mehr der aktiven Geneditierungsfracht in jedes Partikel und ermöglichen so denselben therapeutischen Effekt bei deutlich niedrigeren Dosen. Während Geneditierungstherapien in die Klinik voranschreiten, bietet solches Produzenten-Zell-Engineering einen kraftvollen und flexiblen Weg, Behandlungen sicherer, effizienter und besser skalierbar zu machen.
Zitation: Ly, D., Jang, H., Goel, A. et al. Genome-wide screening reveals producer-cell modifications that improve virus-like particle production and delivery potency. Nat Commun 17, 3695 (2026). https://doi.org/10.1038/s41467-026-71925-8
Schlüsselwörter: virusähnliche Partikel, Lieferung von Geneditierung, Produzenten-Zell-Engineering, CRISPR-Therapeutika, genomweite Suche