Clear Sky Science · tr
Yüksek Mertebe Gephyrin Oligomerlerinin Cryo‑EM Yapıları, İnhibitör Postsinaptik İskelet Organizasyonu İlkelerini Ortaya Koyuyor
Beynin Frenleri Nasıl Ayarlı Kalır
Beynimiz “git” ve “dur” sinyalleri arasındaki hassas bir dengeye dayanır. “Dur” sinyallerini taşıyan inhibitör sinapslar, nöbetler, kaygı ve diğer bozukluklarla ilişkilendirilen kontrolsüz aktiviteyi engeller. Bu çalışma, inhibitör reseptörleri sinapslarda yerinde tutan mikroskobik iskeletleri kuran anahtar bir protein olan gephyrin’i inceliyor. Araştırmacılar gephyrin’in üç boyutlu yapılarını kriyo‑elektron mikroskopisi ile görselleştirerek, bu proteinin reseptörleri şaşırtıcı bir hassasiyetle düzenleyen daha büyük yapılara nasıl kendi kendine bir araya geldiğini gösteriyor.
İnhibitör Sinapsların Sessiz Mimarisi
Birçok inhibitör sinapsta gephyrin, glisin reseptörleri ve GABAA reseptörleri olmak üzere iki tip reseptörü sabitleyen ana düzenleyicidir. Her bir gephyrin molekülü, esnek bir orta bölge ile birbirine bağlı katı uç domainlere sahiptir ve farklı ekzon bağlanma (splicing) çeşitleri ek karmaşıklık katar. Yıllarca bilim insanları, tam uzunluklu gephyrinin çoğunlukla üçlü (trimero) bir araya gelişler oluşturduğunu düşündü ve bu trimeler postsinaptik iskeletin kafes‑benzeri taslaklarını çizmeye yaradı. Ancak sağlam beyin dokusunun daha yeni görüntülenmesi, reseptörlerin ve iskelerin daha esnek bir ağını öne sürerek eski trimer‑merkezli görüşün eksik olduğunu işaret etti.
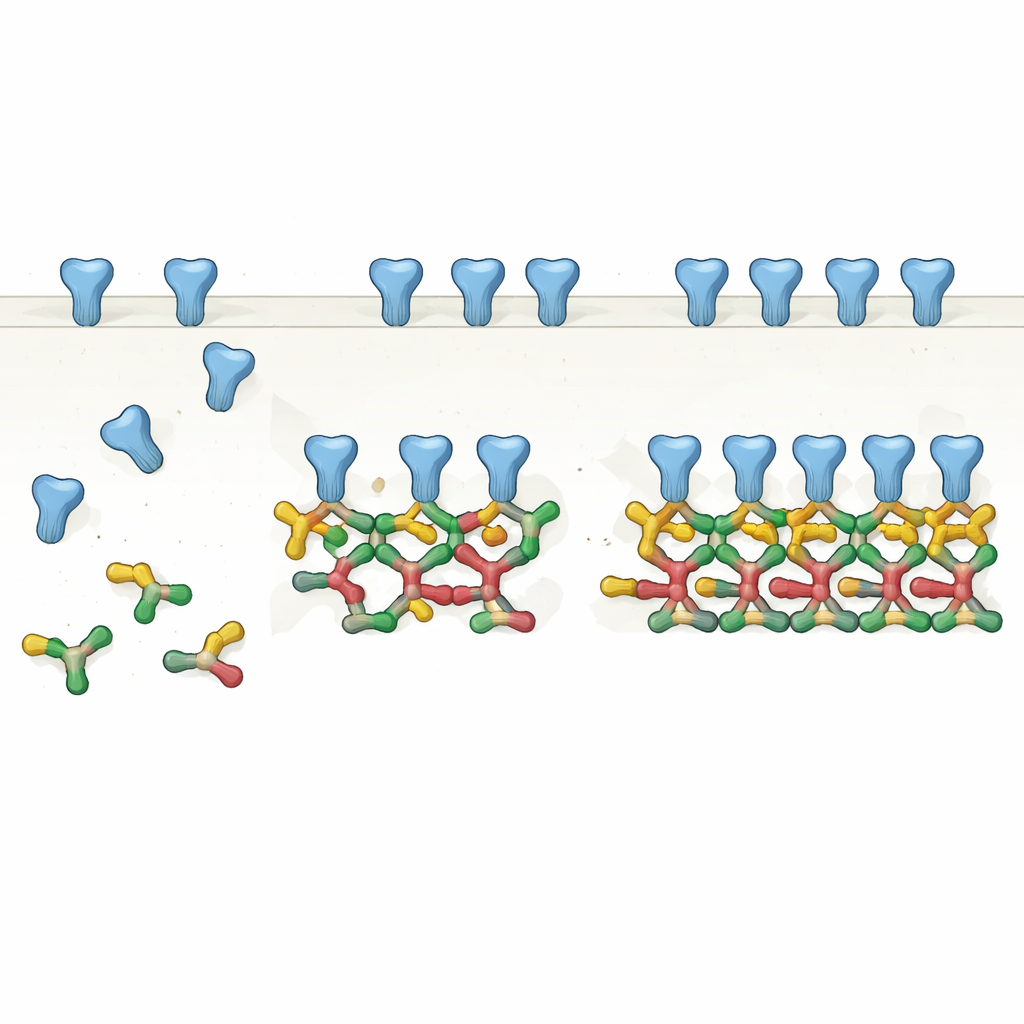
Çiftlerden Zincirlere: İskelete Yeni Bir Bakış
Yazarlar, tam uzunluklu gephyrinin yaygın bir splice formunu dikkatle saflaştırıp çeşitli biyokimyasal yöntemlerle analiz ederek, gephyrin’in en doğal halinde çiftler yani dimerler oluşturduğunu gösteriyor. Bu dimerler daha sonra daha büyük yapıların temel yapı taşları olarak görev yapıyor: dört molekülden oluşan düz zincirler (dimerlerin dimeri) ve hatta altı üyeli zincirler. Kriyo‑elektron mikroskopisi kullanarak bu yapıların yüksek çözünürlüklü yapılarını çözdüklerinde, gephyrin’in bir bölümündeki belirli yüzeylerin komşu dimerlerdeki uyumlu yüzeylerle tekrar tekrar temas ettiğini buldular. Statik bir trimerik merkez yerine, gephyrin doğrusal ve açılı zincirlere genişleyebilen modüler bir sistem olarak ortaya çıkıyor; bu da önceki in‑situ beyin görüntülemelerinde görülen reseptörlerin aralığına ve düzenlerine uyuyor.
Gizli Anahtarlı Esnek Bağlantı Bölgesi
En ilgi çekici keşiflerden biri, uzun süredir yapısal olarak çözülemeyen proteinin esnek orta segmenti yani linker’da yatıyor. Ekip, bu linkerin gephyrin’in bir uç domainine geri sarıldığını yakaladı; burada hem proteini stabilize ediyor hem de reseptör bağlayan yüzeye giriyor. Bir konformasyonda linkerin bir kısmı reseptör‑bağlama cebinin içinde oturarak etkin bir şekilde onu engelliyor; başka bir konformasyonda ise dışarı savrularak cebi reseptörlere açık bırakıyor. Bu “içeride” ve “dışarıda” durumları arasında pozisyon değiştiren amino asitlerden bazılarının fosforilasyonun hedefleri olduğu biliniyor; fosforilasyon hücrelerin kullandığı yaygın bir açma‑kapama kimyasal değişimi. Bu, beyin hücrelerinin gephyrin’in linker’ını reseptör‑engelleyici ile reseptör‑karşılayıcı şekil arasında kimyasal olarak iterek inhibitör gücünü ayarlayabileceğini düşündürüyor.
Elektriksel Tutkal ve Sıvı Damlacıkları
Çalışma ayrıca gephyrin dimerlerinin daha yüksek mertebeli zincirlere bağlanmasına yardımcı olan elektrostatik “Velcro” görevindeki yüklü kalıntıkları ve hücre içinde sıvı benzeri protein damlacıkları yani kondensatların oluşumunu destekleyen bölgeleri belirliyor. Araştırmacılar temel pozitif ya da negatif yükleri mutasyona uğrattıklarında, kültürdeki hücrelerde gephyrin büyük damlacıklar oluşturma yeteneğini yitirdi ve çok daha az ya da daha küçük kümeler halinde toplandı. Nöronlarda aynı mutasyonlar, değiştirilmiş proteinler o bölgelere ulaşabilse bile, inhibitör sinapslardaki gephyrin birikimini zayıflattı. Birlikte, bu deneyler gephyrin’in yapısını stabil hale getiren aynı yüklü bölgelerin ve linker segmentinin gerçek sinapslarda yoğun reseptör kümeleri oluşturmak için de gerekli olduğunu gösteriyor.
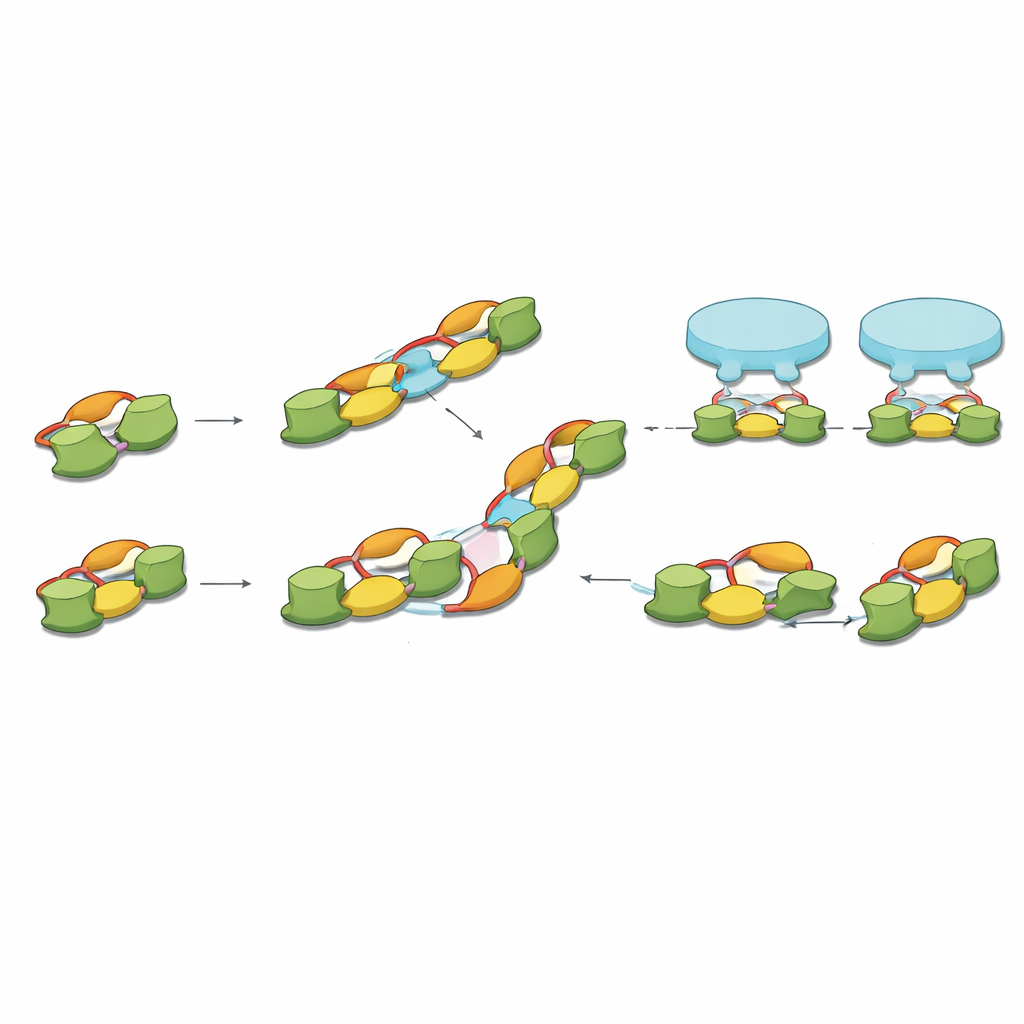
Molekülleri Sinaptik Desenlerle Bağlamak
Son olarak yazarlar, moleküler anlık görüntülerini önceki sağlam beyin dokusunun kriyo‑elektron tomografisi ile ilişkilendiriyor; bu çalışmalar komşu inhibitör reseptörler arasında karakteristik bir aralık ölçmüştü. Gephyrin dimer‑of‑dimerin uzunluğu bu aralığa yakın şekilde eşleşiyor ve düz ile açılı zincir kombinasyonları nöronlarda gözlenen en yaygın reseptör desenlerini yeniden oluşturabiliyor. Bu tasvirde, gephyrin dimerleri reseptör çiftleri için temel kelepçe sağlar ve daha yüksek mertebeli zincirler bu kelepçelerin yüklü arayüzler aracılığıyla yan yana bağlanmasıyla ortaya çıkar.
Bunun Beyin Sağlığı İçin Önemi Nedir
Genel olarak bu çalışma, gephyrin’in basit bir trimer‑temelli çizimini dinamik, zincir‑oluşturan bir iskeletle değiştiriyor; bu iskeletin şekli ve reseptör‑bağlama kapasitesi esnek bir linker üzerindeki ince kimyasal işaretlerle ayarlanabiliyor. Bu, inhibitör sinapsların hem yapısal olarak düzenli hem de hızlıca ayarlanabilir olmasını açıklamaya yardımcı oluyor ve gephyrin’in bir araya gelişini bozan hastalık ilişkili mutasyonları anlamak için moleküler bir çerçeve sunuyor. Beynin fren sisteminin fiziksel olarak nasıl kurulduğunu ve modüle edildiğini aydınlatarak, çalışma epilepsi, otizm spektrum bozuklukları ve kaygı gibi durumlarda inhibitör dengesini hedeflemenin yollarını açıyor.
Atıf: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Anahtar kelimeler: gephyrin, inhibitör sinaps, GABAA reseptörü, kriyo‑elektron mikroskopisi, sinaptik iskelet