Clear Sky Science · de
Cryo‑EM‑Strukturen höherer Ordnungsstufen von Gephyrin‑Oligomeren enthüllen Prinzipien der Organisation des inhibitorischen postsynaptischen Gerüsts
Wie die Bremsen des Gehirns in Balance bleiben
Unser Gehirn beruht auf einem empfindlichen Gleichgewicht zwischen „Los“‑ und „Stopp“‑Signalen. Die „Stopp“‑Signale, vermittelt von inhibitorischen Synapsen, verhindern unkontrollierte Aktivität, die mit Anfällen, Angststörungen und anderen Erkrankungen verbunden ist. Diese Studie untersucht Gephyrin, ein Schlüss eiweiß, das die mikroskopischen Gerüste aufbaut, die inhibitorische Rezeptoren an Synapsen an ihrem Platz halten. Durch die Visualisierung der dreidimensionalen Gestalt von Gephyrin mittels Kryo‑Elektronenmikroskopie zeigen die Autoren, wie dieses Protein sich zu größeren Strukturen selbst‑assemblieren kann, die Rezeptoren mit überraschender Präzision organisieren.
Der stille Architekt inhibitorischer Synapsen
An vielen inhibitorischen Synapsen ist Gephyrin der Hauptorganisator, der zwei Rezeptortypen verankert: Glycinrezeptoren und GABAA‑Rezeptoren. Jedes Gephyrinmolekül besitzt starre Enddomänen, die durch einen beweglichen Mittelbereich verbunden sind, und verschiedene Spleißvarianten fügen zusätzliche Komplexität hinzu. Lange Zeit ging man davon aus, dass voll‑längiges Gephyrin vorwiegend dreiteilige Assemblies bildet – Trimere –, und auf dieser Grundlage wurden gitterähnliche Modelle des postsynaptischen Gerüsts skizziert. Neuere Aufnahmen intakten Hirngewebes deuteten jedoch auf ein flexibleres Netzwerk von Rezeptoren und Gerüsten hin und legten nahe, dass die trimere Sicht unvollständig war.
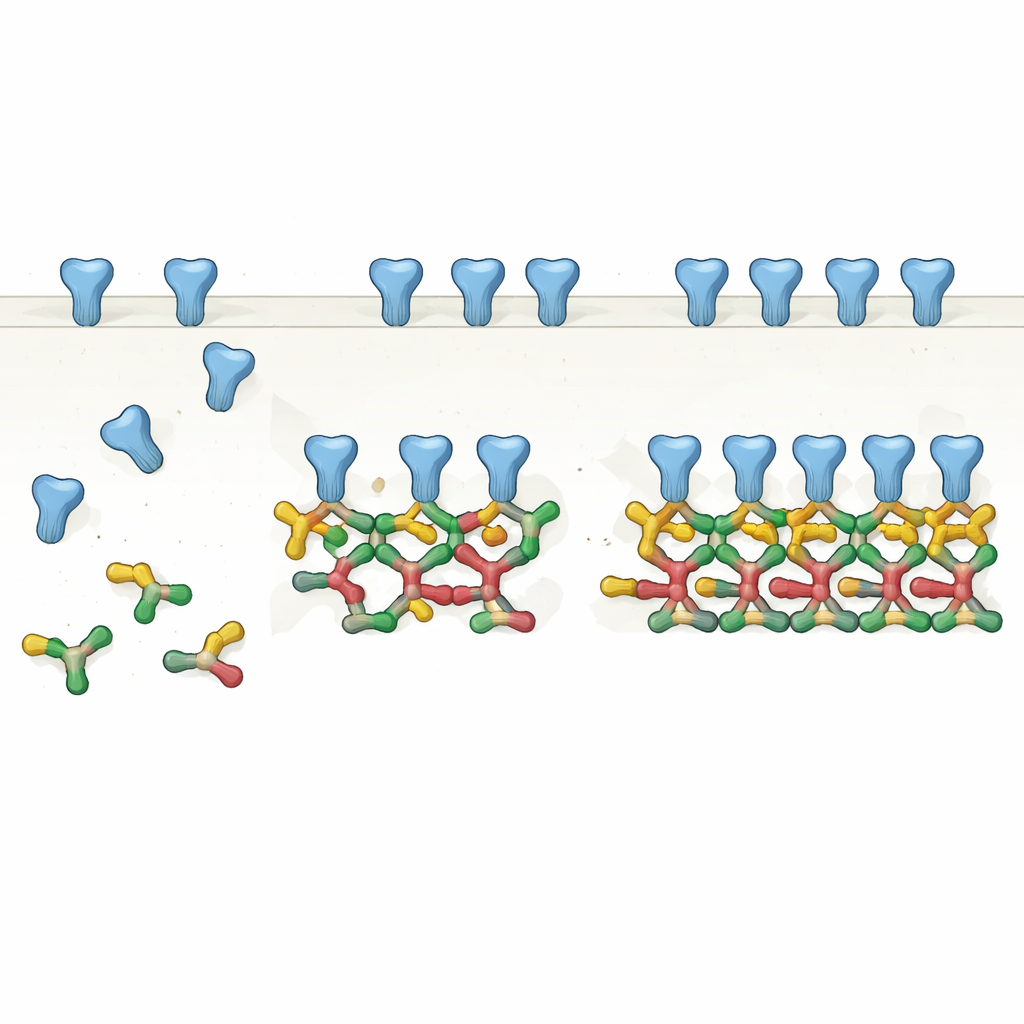
Von Paaren zu Ketten: Eine neue Sicht auf das Gerüst
Durch sorgfältige Reinigung einer häufigen Spleißform des voll‑längigen Gephyrins und Analyse mit mehreren biochemischen Methoden zeigen die Autoren, dass Gephyrin natürlicherweise eher Paare, also Dimere, bildet. Diese Dimere dienen dann als Bausteine für größere Strukturen: gerade Ketten aus vier Molekülen (Dimere von Dimeren) und sogar sechsgliedrige Ketten. Mithilfe der Kryo‑Elektronenmikroskopie lösten sie hochauflösende Strukturen dieser Assemblies und fanden heraus, dass spezifische Flächen an einem Gephyrinabschnitt wiederholt passende Flächen an benachbarten Dimeren kontaktieren. Anstatt eines statischen trimeren Hubs erscheint Gephyrin als modulares System, das sich in lineare und gewinkelte Ketten ausdehnen kann und so die Abstände und Anordnungen der Rezeptoren reproduziert, die in früheren in situ‑Aufnahmen beobachtet wurden.
Ein flexibler Linker mit verstecktem Schalter
Einer der faszinierendsten Befunde betrifft das flexible Mittelstück des Proteins, den Linker, der lange der strukturellen Analyse entgangen war. Das Team fing diesen Linker ein, wie er sich zurück auf eine Enddomäne von Gephyrin legt, wo er das Protein sowohl stabilisiert als auch in dieselbe Oberfläche hineinreicht, die zur Rezeptorbindung verwendet wird. In einer Konformation sitzt ein Teil des Linkers in der rezeptorbindenden Tasche und blockiert sie effektiv; in einer anderen schwingt er heraus und lässt die Tasche offen für Rezeptoren. Mehrere Aminosäuren, die zwischen diesen „in“‑ und „out“‑Zuständen ihre Position ändern, sind bekannte Ziele der Phosphorylierung, einer häufigen chemischen Modifikation, die Zellen als Ein‑/Aus‑Schalter verwenden. Dies legt nahe, dass Nervenzellen die Stärke der Hemmung dadurch feinjustieren könnten, dass sie Gephyrins Linker chemisch zwischen receptorblockierender und rezeptorfreundlicher Form umschalten.
Elektrostatische Klebe und flüssige Tröpfchen
Die Studie identifiziert zudem geladene Reste, die als elektrostatisches „Klettband“ wirken und Gephyrin‑Dimere zu höhergeordneten Ketten verbinden sowie die Bildung von flüssigkeitsähnlichen Proteintröpfchen oder Kondensaten in Zellen fördern. Wenn die Forscher wichtige positive oder negative Ladungen veränderten, verlor Gephyrin in kultivierten Zellen die Fähigkeit, große Tröpfchen zu bilden, und assemblierten in deutlich weniger oder kleinere Cluster. In Neuronen schwächten dieselben Mutationen die Anreicherung von Gephyrin an inhibitorischen Synapsen, obwohl die veränderten Proteine diese Orte noch erreichen konnten. Zusammen zeigen diese Experimente, dass dieselben geladenen Regionen und der Linker, die Gephyrins Struktur stabilisieren, auch grundlegend dafür sind, dichte Rezeptorcluster an echten Synapsen zu erzeugen.
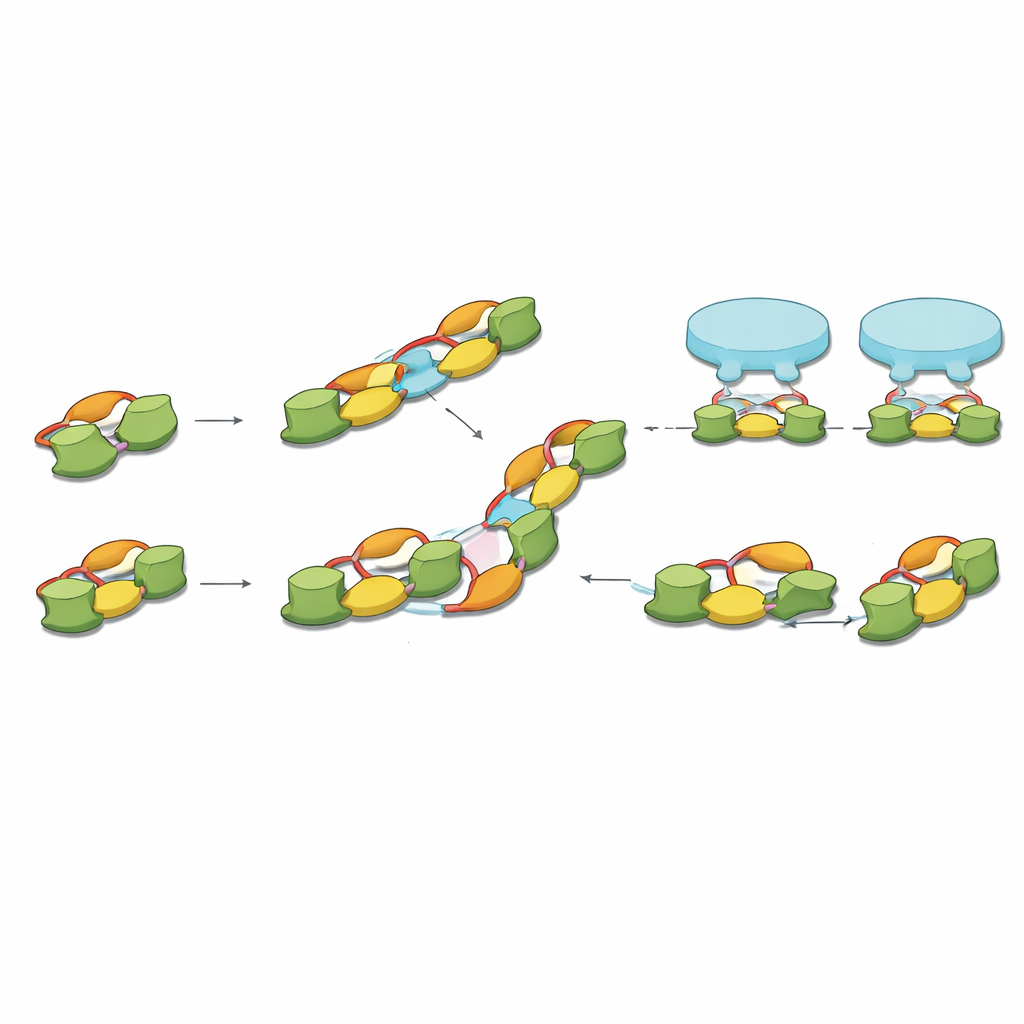
Moleküle mit synaptischen Mustern verbinden
Schließlich bringen die Autoren ihre molekularen Momentaufnahmen in Verbindung mit früheren kryo‑Elektronentomographien intakten Hirngewebes, die einen charakteristischen Abstand zwischen benachbarten inhibitorischen Rezeptoren gemessen hatten. Die Länge des Gephyrin‑Dimer‑von‑Dimeren stimmt eng mit diesem Abstand überein, und Kombinationen aus geraden und gewinkelten Ketten können die häufigsten Rezeptormuster nachbilden, die in Neuronen beobachtet wurden. In diesem Bild liefern Gephyrin‑Dimere die grundlegende Klammer für Rezeptorpaare, und höhergeordnete Ketten entstehen, wenn diese Klammern sich durch geladene Schnittstellen nebeneinander verbinden.
Warum das für die Gehirngesundheit wichtig ist
Insgesamt ersetzt die Arbeit die einfache, auf Trimere basierende Darstellung von Gephyrin durch ein dynamisches, kettenbildendes Gerüst, dessen Gestalt und rezeptorbindende Kapazität durch subtile chemische Markierungen an einem flexiblen Linker gesteuert werden kann. Das hilft zu erklären, wie inhibitorische Synapsen zugleich strukturell geordnet und schnell anpassbar sein können, und bietet einen molekularen Rahmen zum Verständnis krankheitsassoziierter Mutationen, die Gephyrins Assemblierung stören. Indem sie klärt, wie das Bremsensystem des Gehirns physikalisch aufgebaut und moduliert wird, eröffnet die Studie Wege, das inhibitorische Gleichgewicht bei Erkrankungen wie Epilepsie, Autismus‑Spektrum‑Störungen und Angststörungen gezielt anzugehen.
Zitation: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Schlüsselwörter: gephyrin, inhibitorische Synapse, GABAA‑Rezeptor, Kryo‑Elektronenmikroskopie, synaptisches Gerüst