Clear Sky Science · sv
Cryo-EM-strukturer av högre ordningens Gephyrin‑oligomerer avslöjar principer för organisationen av den inhibitoriska postsynaptiska skelettstrukturen
Hur hjärnans bromsar håller sig i takt
Våra hjärnor bygger på en känslig balans mellan ”kör” och ”stopp”-signaler. ”Stopp”-signalerna, som förmedlas av inhibitoriska synapser, förhindrar okontrollerad aktivitet som kan kopplas till anfall, ångest och andra störningar. Denna studie undersöker gephyrin, ett nyckelprotein som bygger de mikroskopiska ställningar som håller inhibitoriska receptorer på plats vid synapser. Genom att visualisera gephyrins tredimensionella former med kryo‑elektronmikroskopi visar författarna hur detta protein självmonterar till större strukturer som organiserar receptorer med förvånansvärd precision.
Den tysta arkitekten vid inhibitoriska synapser
Vid många inhibitoriska synapser är gephyrin huvudorganisatören som förankrar två typer av receptorer: glycinreceptorer och GABAA-receptorer. Varje gephyrinmolekyl har styva änddomäner förbundna med en mer sladdrig mellanregion, och olika splitsvarianter tillför ytterligare komplexitet. Under lång tid trodde forskare att fullängds‑gephyrin huvudsakligen bildade trepartsaggregat, och dessa trimrar användes för att skissera gallerliknande modeller av det postsynaptiska skelettet. Nyare avbildning av intakt hjärnvävnad antydde dock ett mer flexibelt nätverk av receptorer och skelett, vilket tyder på att den gamla trimercentrerade bilden var ofullständig.
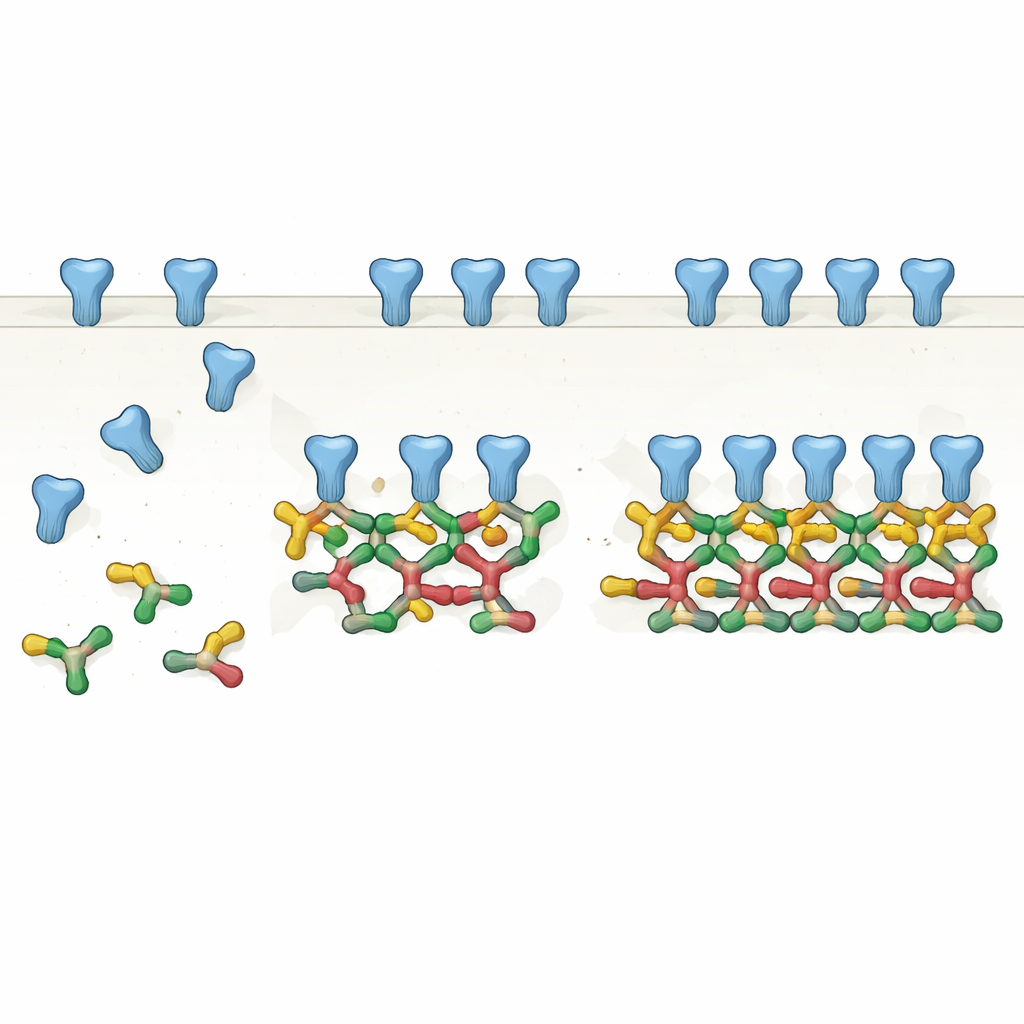
Från par till kedjor: en ny bild av skelettet
Genom att noggrant rena en vanlig splitsvariant av fullängds‑gephyrin och analysera den med flera biokemiska metoder visar författarna att gephyrin mest naturligt bildar par, det vill säga dimerer. Dessa dimerer fungerar sedan som grundblock för större strukturer: raka kedjor av fyra molekyler (dimerer av dimerer) och till och med sexledade kedjor. Med kryo‑elektronmikroskopi löste de högupplösta strukturer av dessa komplex och fann att specifika ytor på en del av gephyrin upprepade gånger kontaktar matchande ytor på intilliggande dimerer. Istället för en statisk trimerisk nav framträder gephyrin som ett modulärt system som kan förlängas till linjära och vinklade kedjor, i takt med de avstånd och arrangemang av receptorer som setts i tidigare in situ‑avbildning av hjärnan.
En flexibel länk med en dold brytare
En av de mest fascinerande upptäckterna ligger i proteinets flexibla mittsegment, eller länkaren, som länge undgått strukturanalys. Forskargruppen fångade denna länkare när den veckade tillbaka sig över en änddomän av gephyrin, där den både stabiliserar proteinet och når in i samma yta som används för att binda receptorer. I en konformation sitter en del av länkaren inne i receptorbindningsfickan och blockerar den; i en annan svänger den ut och lämnar fickan öppen för receptorer. Flera av de aminosyror som ändrar position mellan dessa ”in”‑ och ”ut”‑tillstånd är kända mål för fosforylering, en vanlig kemisk modifiering som celler använder som en på‑/av‑brytare. Detta tyder på att hjärnceller kan justera inhibitorytstyrkan genom att kemiskt förflytta gephyrins länkare mellan en receptor‑blockerande och en receptor‑mottagande form.
Elektrostatisk klister och flytande droppar
Studien pekar också ut laddade rester som agerar som elektrostatisk ”kardborre”, vilket hjälper gephyrin‑dimerer att länka ihop sig till högre ordningens kedjor och främjar bildningen av proteinlika droppar, eller kondensat, inne i celler. När forskarna muterade viktiga positiva eller negativa laddningar förlorade gephyrin i odlade celler förmågan att bilda stora droppar och sammanfogades i betydligt färre eller mindre kluster. I neuroner försvagade samma mutationer uppbyggnaden av gephyrin vid inhibitoriska synapser, även om de förändrade proteinerna fortfarande kunde nå dessa platser. Tillsammans visar dessa experiment att samma laddade regioner och länksegment som stabiliserar gephyrins struktur också är avgörande för att skapa täta receptoransamlingar vid verkliga synapser.
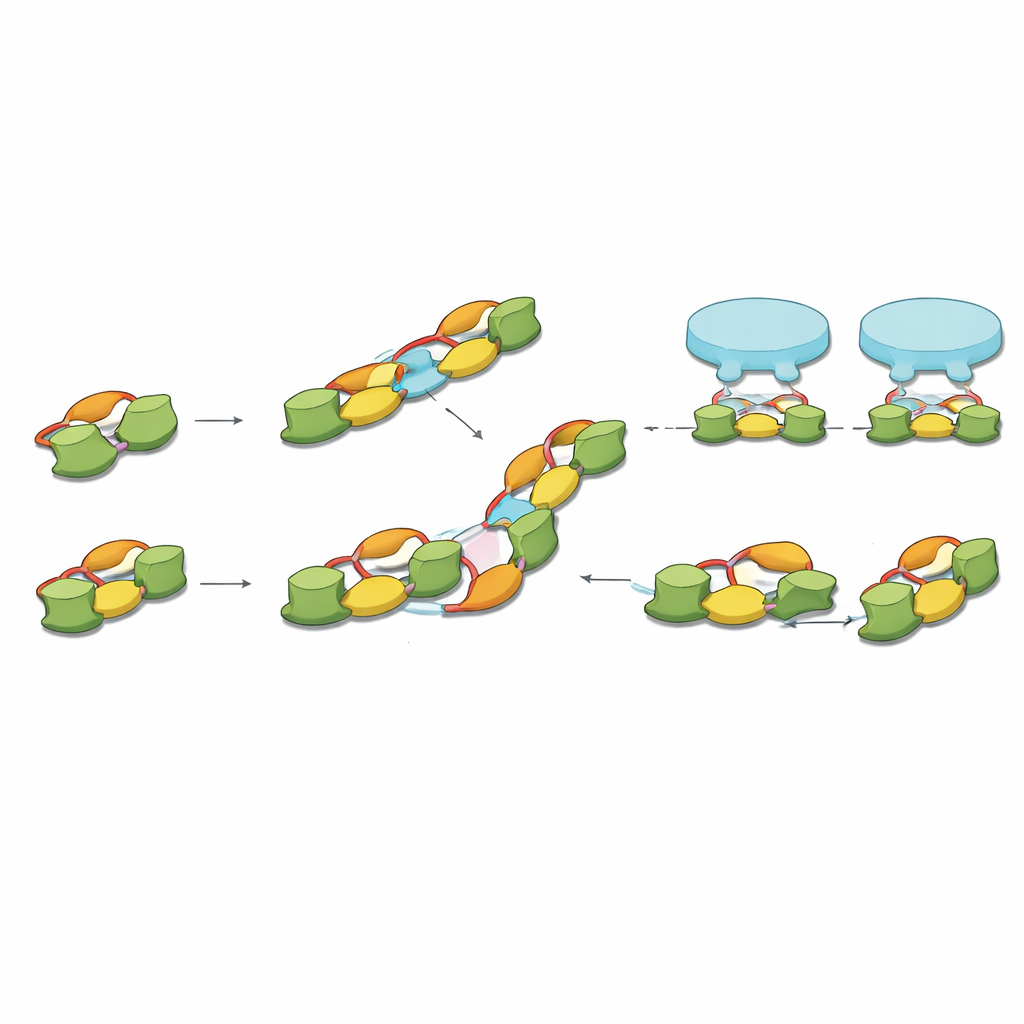
Att koppla molekyler till synaptiska mönster
Slutligen förbinder författarna sina molekylära ögonblicksbilder med tidigare kryo‑elektrontomografi av intakt hjärnvävnad, som mätt ett karakteristiskt avstånd mellan intilliggande inhibitoriska receptorer. Längden på gephyrinets dimer‑av‑dimerer överensstämmer nära detta avstånd, och kombinationer av raka och vinklade kedjor kan återskapa de vanligaste receptormönstren som observerats i neuroner. I denna bild utgör gephyrin‑dimerer den grundläggande klämman för receptorpar, och högre ordningens kedjor uppstår när dessa klämmor kopplas sida vid sida genom laddade gränssnitt.
Varför detta spelar roll för hjärnhälsa
Sammanfattningsvis ersätter arbetet en enkel trimerbaserad skiss av gephyrin med ett dynamiskt, kedjebildande skelett vars form och receptorbindande kapacitet kan finjusteras av subtila kemiska markeringar på en flexibel länkare. Detta hjälper till att förklara hur inhibitoriska synapser kan vara både strukturellt ordnade och snabbt justerbara, och ger en molekylär ram för att förstå sjukdomsrelaterade mutationer som stör gephyrins montering. Genom att klargöra hur hjärnans bromssystem är fysiskt uppbyggt och reglerat öppnar studien möjligheter för att rikta in sig på inhibitorisk balans vid tillstånd som epilepsi, autismdiagnosspektrum och ångest.
Citering: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Nyckelord: gephyrin, inhibitorisk synaps, GABAA‑receptor, kryo‑elektronmikroskopi, synaptiskt skelett