Clear Sky Science · pl
Struktury Cryo-EM wyższych porządków oligomerów gephyryny ujawniają zasady organizacji postsynaptycznego szkieletu hamującego
Jak hamulce mózgu zachowują równowagę
Nasz mózg opiera się na delikatnej równowadze między sygnałami „dalej” a „stop”. Sygnały „stop”, przekazywane przez synapsy hamujące, zapobiegają wymykającej się spod kontroli aktywności związanej z napadami, lękiem i innymi zaburzeniami. W tej pracy badano gephyrynę, kluczowe białko budujące mikroskopijne rusztowania utrzymujące receptory hamujące na miejscu w synapsach. Poprzez wizualizację trójwymiarowych kształtów gephyryny za pomocą kriomikroskopii elektronowej autorzy ujawniają, jak to białko samoorganizuje się w większe struktury, które z zaskakującą precyzją porządkują receptory.
Cichy architekt synaps hamujących
W wielu synapsach hamujących gephyryna jest głównym organizatorem kotwiczącym dwa typy receptorów: receptory glicynowe i receptory GABAA. Każda cząsteczka gephyryny ma sztywne domeny końcowe połączone giętkim środkowym odcinkiem, a różne warianty splicingowe dodają dalszą złożoność. Przez lata naukowcy sądzili, że pełnej długości gephyryna tworzy głównie trójczłonowe zespoły, i na tej podstawie szkicowano siatkowe projekty postsynaptycznego szkieletu. Jednak nowsze obrazowanie intacttkowej tkanki mózgowej sugerowało bardziej elastyczną sieć receptorów i rusztowań, co wskazywało, że stary pogląd skoncentrowany na trimerach jest niepełny.
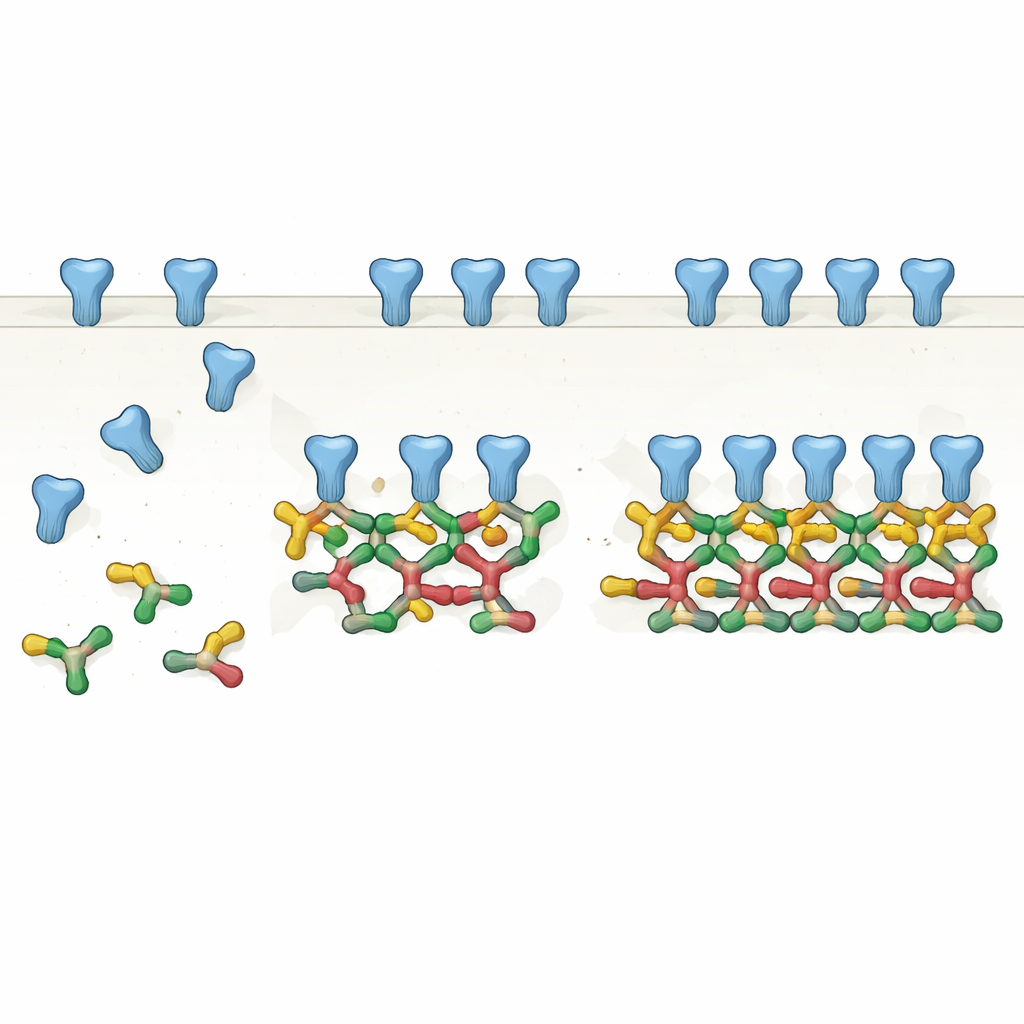
Od par do łańcuchów: nowy obraz szkieletu
Poprzez staranne oczyszczenie jednego powszechnego wariantu splicingowego pełnej długości gephyryny i analizę za pomocą kilku metod biochemicznych, autorzy wykazali, że gephyryna najchętniej tworzy pary, czyli dymery. Te dymery działają następnie jako podstawowe cegiełki do budowy większych struktur: prostych łańcuchów złożonych z czterech cząsteczek (dymery dimerów) a nawet łańcuchów sześcioelementowych. Przy użyciu kriomikroskopii elektronowej rozwiązano struktury wysokiej rozdzielczości tych zespołów i odkryto, że określone powierzchnie jednej części gephyryny wielokrotnie stykają się z odpowiadającymi powierzchniami sąsiednich dimerów. Zamiast statycznego, trójczłonowego węzła, gephyryna jawi się jako modułowy system, który może rozszerzać się w linie i pod kątem ustawione łańcuchy, dopasowując się do rozstawu i układów receptorów widzianych we wcześniejszych obrazach in situ tkanki mózgowej.
Giętki łącznik z ukrytym przełącznikiem
Jedno z najbardziej intrygujących odkryć dotyczy giętkiego środkowego odcinka białka, czyli łącznika, który długo wymykał się analizie strukturalnej. Zespół uchwycił ten łącznik owinięty z powrotem wokół jednej domeny końcowej gephyryny, gdzie stabilizuje białko i wchodzi w obszar używany do wiązania receptorów. W jednej konformacji część łącznika osadza się w kieszeni wiążącej receptor, skutecznie ją blokując; w innej wychyla się na zewnątrz, pozostawiając kieszeń otwartą dla receptorów. Kilka aminokwasów zmieniających pozycję między stanami „wewnątrz” i „na zewnątrz” jest znanych jako cele fosforylacji — powszechnej modyfikacji chemicznej, której komórki używają jak przełącznika on–off. To sugeruje, że komórki mózgowe mogą dostrajać siłę hamowania przez chemiczne przesuwanie łącznika gephyryny między kształtem blokującym receptor a kształtem go akceptującym.
Elektrostatyczny klej i krople ciekłe
Praca identyfikuje także naładowane reszty działające jak elektrostatyczne „rzepy”, pomagające dimerom gephyryny łączyć się w łańcuchy wyższego rzędu i sprzyjające powstawaniu kropli białkowych o charakterze ciekłym, czyli kondensatów, wewnątrz komórek. Gdy badacze mutowali kluczowe ładunki dodatnie lub ujemne, gephyryna w hodowanych komórkach traciła zdolność tworzenia dużych kropli i tworzyła znacznie mniej lub mniejsze skupiska. W neuronach te same mutacje osłabiały gromadzenie się gephyryny w synapsach hamujących, mimo że zmodyfikowane białka nadal mogły docierać do tych miejsc. W sumie eksperymenty te pokazują, że te same naładowane regiony i segment łącznika, które stabilizują strukturę gephyryny, są także niezbędne do tworzenia gęstych klastrów receptorów w rzeczywistych synapsach.
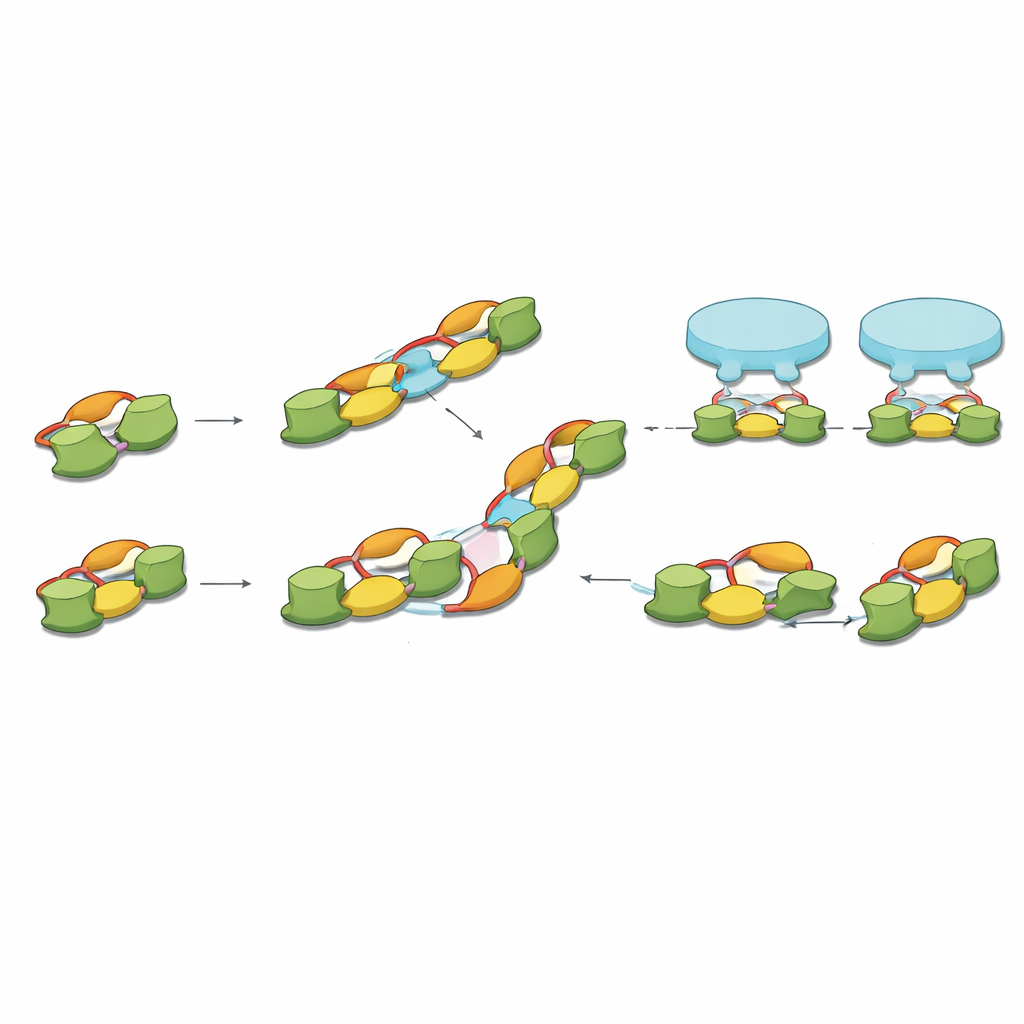
Łączenie cząsteczek z wzorcami synaptycznymi
Na koniec autorzy powiązali swoje molekularne „migawki” z wcześniejszą tomografią krioelektronową nienaruszonej tkanki mózgowej, która mierzyła charakterystyczny rozstaw między sąsiednimi receptorami hamującymi. Długość dimeru dimerów gephyryny dobrze odpowiada temu rozstawowi, a kombinacje prostych i kątowych łańcuchów mogą odtworzyć najczęstsze wzory receptorów obserwowane w neuronach. W tym obrazie dymery gephyryny zapewniają podstawowe zaciski dla par receptorów, a łańcuchy wyższego rzędu powstają, gdy te zaciski łączą się bocznie przez naładowane interfejsy.
Dlaczego ma to znaczenie dla zdrowia mózgu
Ogólnie rzecz biorąc, praca zastępuje prosty, oparty na trimerach schemat gephyryny dynamicznym, łańcuchotwórczym szkieletem, którego kształt i zdolność wiązania receptorów mogą być regulowane przez subtelne chemiczne znaki na giętkim łączniku. To pomaga wyjaśnić, jak synapsy hamujące mogą być jednocześnie strukturalnie uporządkowane i szybko regulowane, oraz dostarcza molekularnych ram do zrozumienia mutacji związanych z chorobami, które zaburzają montaż gephyryny. Poprzez wyjaśnienie, jak fizycznie zbudowany i modulowany jest system hamowania mózgu, badanie otwiera ścieżki do celowania w równowagę hamowania w stanach takich jak padaczka, zaburzenia ze spektrum autyzmu i lęk.
Cytowanie: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Słowa kluczowe: gephyryna, synapsa hamująca, receptor GABAA, kriomikroskopia elektronowa, szkielet synaptyczny