Clear Sky Science · it
Strutture cryo-EM di oligomeri di gephyrin di ordine superiore rivelano i principi di organizzazione dello scaffold postsinaptico inibitorio
Come i freni cerebrali restano sintonizzati
I nostri cervelli si basano su un equilibrio delicato tra segnali di “vai” e di “stop”. I segnali di “stop”, trasportati dalle sinapsi inibitorie, impediscono un’attività incontrollata legata a crisi epilettiche, ansia e altri disturbi. Questo studio esamina la gephyrin, una proteina chiave che costruisce gli scaffold microscopici che tengono i recettori inibitori al loro posto nelle sinapsi. Visualizzando le forme tridimensionali della gephyrin mediante crio-microscopia elettronica, gli autori rivelano come questa proteina si autoassemblia in strutture più grandi che organizzano i recettori con sorprendente precisione.
L’architetto silenzioso delle sinapsi inibitorie
In molte sinapsi inibitorie, la gephyrin è il principale organizzatore che ancorazza due tipi di recettori: i recettori della glicina e i recettori GABAA. Ogni molecola di gephyrin possiede domini terminali rigidi collegati da una regione centrale flessibile, e varianti di splicing diverse aggiungono ulteriore complessità. Per anni, gli scienziati hanno pensato che la gephyrin a lunghezza intera formasse principalmente assemblaggi trimetrici, e questi trimeri venivano usati per schematiche a reticolo dello scaffold postsinaptico. Tuttavia, immagini più recenti di tessuto cerebrale intatto suggerivano una trama più flessibile di recettori e scaffold, lasciando intendere che la visione centrata sul trimero fosse incompleta.
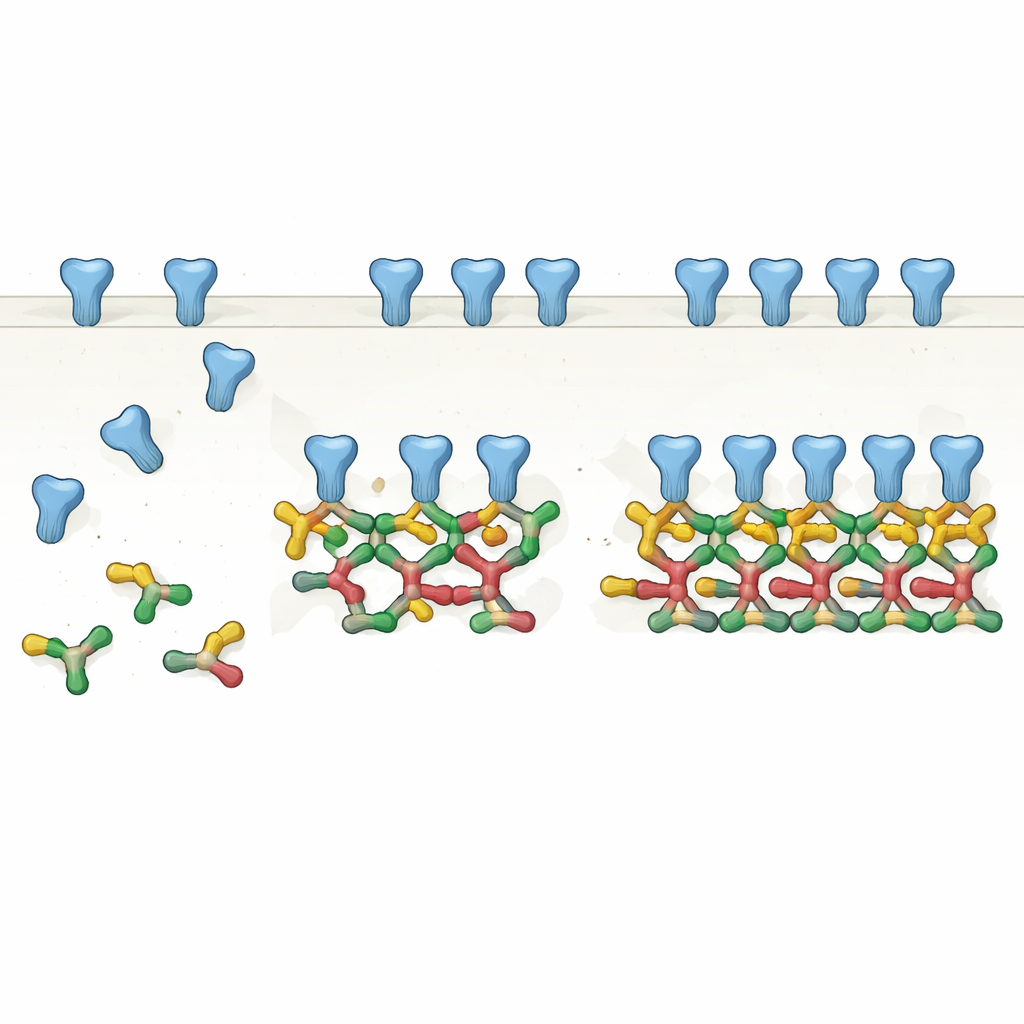
Dalle coppie alle catene: una nuova visione dello scaffold
Purificando con cura una forma di splicing comune della gephyrin a lunghezza intera e analizzandola con diversi metodi biochimici, gli autori mostrano che la gephyrin forma più naturalmente coppie, o dimeri. Questi dimeri poi fungono da mattoni di base per strutture più grandi: catene rette di quattro molecole (dimeri di dimeri) e persino catene a sei elementi. Utilizzando la crio-microscopia elettronica, hanno risolto strutture ad alta risoluzione di questi assemblaggi e trovato che superfici specifiche di una parte della gephyrin entrano ripetutamente in contatto con superfici corrispondenti sui dimeri vicini. Piuttosto che un hub trimetrico statico, la gephyrin emerge come un sistema modulare che può estendersi in catene lineari e angolate, adattandosi alla spaziatura e agli arrangiamenti dei recettori osservati in precedenti imaging in situ del cervello.
Un connettore flessibile con un interruttore nascosto
Una delle scoperte più intriganti riguarda il segmento centrale flessibile della proteina, o linker, che a lungo era sfuggito all’analisi strutturale. Il gruppo ha catturato questo linker che si avvolge indietro su uno dei domini terminali della gephyrin, dove sia stabilizza la proteina sia raggiunge la stessa superficie usata per legare i recettori. In una conformazione, parte del linker si trova all’interno della tasca di legame del recettore, bloccandola effettivamente; in un’altra, si estende verso l’esterno, lasciando la tasca aperta ai recettori. Diverse delle aminoacidi che cambiano posizione tra questi stati “dentro” e “fuori” sono noti bersagli della fosforilazione, una comune modifica chimica che le cellule usano come interruttore on–off. Questo suggerisce che le cellule cerebrali possano modulare la forza inibitoria spostando chimicamente il linker della gephyrin tra una forma che blocca il recettore e una che lo accoglie.
Colla elettrostatica e gocce liquide
Lo studio individua anche residui carichi che agiscono come un “Velcro” elettrostatico, aiutando i dimeri di gephyrin a collegarsi in catene di ordine superiore e promuovendo la formazione di gocce proteiche di tipo liquido, o condensati, all’interno delle cellule. Quando i ricercatori hanno mutato cariche chiave positive o negative, la gephyrin nelle cellule coltivate ha perso la capacità di formare grandi gocce e si è assemblata in ammassi molto meno numerosi o più piccoli. Nei neuroni, le stesse mutazioni hanno indebolito l’accumulo di gephyrin nelle sinapsi inibitorie, anche se le proteine alterate potevano comunque raggiungere quei siti. Complessivamente, questi esperimenti mostrano che le stesse regioni cariche e il segmento linker che stabilizzano la struttura della gephyrin sono anche essenziali per creare ammassi densi di recettori nelle sinapsi reali.
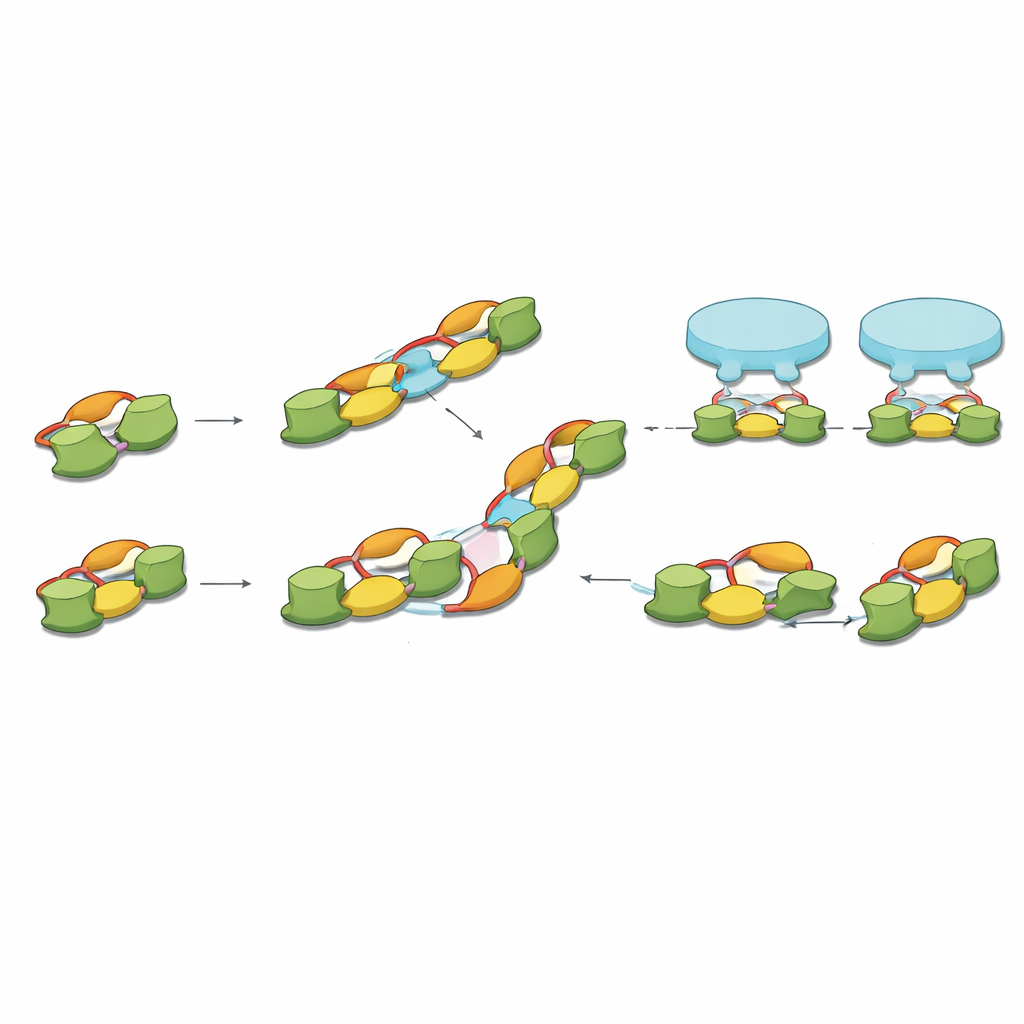
Collegare le molecole ai modelli sinaptici
Infine, gli autori collegano i loro istantanee molecolari a precedenti tomografie crio-elettroniche di tessuto cerebrale intatto, che avevano misurato una spaziatura caratteristica tra recettori inibitori adiacenti. La lunghezza del dimero-di-dimeri di gephyrin corrisponde da vicino a questa spaziatura, e combinazioni di catene rette e angolate possono ricreare i modelli di recettori più comuni osservati nei neuroni. In questo quadro, i dimeri di gephyrin forniscono la morsetta di base per le coppie di recettori, e catene di ordine superiore emergono mentre queste morse si connettono fianco a fianco tramite interfaccie cariche.
Perché questo è importante per la salute del cervello
Nel complesso, il lavoro sostituisce il semplice schema trimetrico della gephyrin con uno scaffold dinamico che forma catene, la cui forma e capacità di legare i recettori possono essere regolate da sottili segnali chimici su un linker flessibile. Questo aiuta a spiegare come le sinapsi inibitorie possano essere sia strutturalmente ordinate sia rapidamente modulabili, e offre un quadro molecolare per comprendere le mutazioni legate a malattie che disturbano l’assemblaggio della gephyrin. Chiarendo come il sistema frenante del cervello sia costruito e modulato fisicamente, lo studio apre strade per intervenire sull’equilibrio inibitorio in condizioni come l’epilessia, i disturbi dello spettro autistico e l’ansia.
Citazione: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Parole chiave: gephyrin, sinapsi inibitoria, recettore GABAA, crio-microscopia elettronica, scaffold sinaptico