Clear Sky Science · ru
Крио-ЭМ структуры более высоких порядка олигомеров гефирина раскрывают принципы организации ингибиторного постсинаптического каркаса
Как «тормоза» мозга сохраняют настрой
Наши мозги зависят от тонкого баланса между сигналами «вперёд» и «стоп». Сигналы «стоп», передаваемые ингибиторными синапсами, предотвращают неконтролируемую активность, связанную с приступами, тревогой и другими расстройствами. В этом исследовании рассматривают гефирин — ключевой белок, строящий микроскопические каркасы, удерживающие ингибиторные рецепторы на местах в синапсах. Визуализируя трёхмерные формы гефирина с помощью крио-электронной микроскопии, авторы показывают, как этот белок самоорганизуется в более крупные структуры, которые с удивительной точностью располагают рецепторы.
Молчаливый архитектор ингибиторных синапсов
На многих ингибиторных синапсах гефирин является главным организатором, закрепляющим два типа рецепторов: глициновые рецепторы и GABAA-рецепторы. Каждая молекула гефирина имеет жёсткие концевые домены, соединённые гибким средним участком, а разные варианты сплайсинга добавляют дополнительную сложность. В течение многих лет считали, что полноразмерный гефирин преимущественно формирует трёхчастные сборки, и эти тримеры использовали для набросков решётчатых схем постсинаптического каркаса. Однако более современные изображения цельной ткани мозга указывали на более гибкую сетчатую структуру рецепторов и каркасов, намекая, что старая тример-центричная модель была неполной.
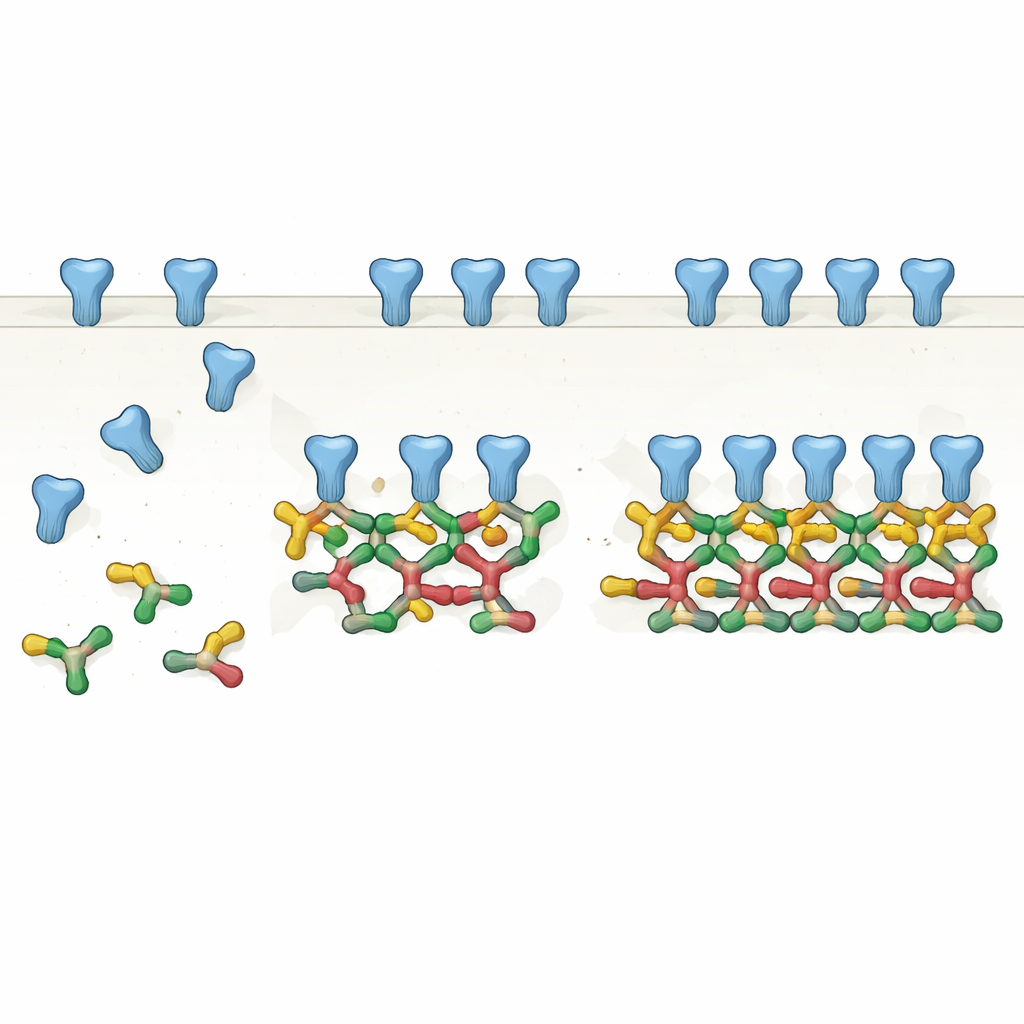
От пар к цепочкам: новый взгляд на каркас
Тщательно очистив одну распространённую форму сплайсинга полноразмерного гефирина и проанализировав её несколькими биохимическими методами, авторы показали, что гефирин естественным образом образует пары, или димеры. Эти димеры затем служат базовыми строительными блоками для более крупных структур: прямых цепочек из четырёх молекул (димеров димеров) и даже шестичленных цепочек. С помощью крио-ЭМ они получили высокоразрешающие структуры этих сборок и обнаружили, что определённые поверхности одной части гефирина многократно контактируют с соответствующими поверхностями соседних димеров. Вместо статичного тримерного центра гефирин предстает как модульная система, способная вытягиваться в линейные и изломанные цепочки, соответствуя расстояниям и расположениям рецепторов, наблюдавшимся в предыдущих in situ изображениях мозга.
Гибкий линкер с скрытым переключателем
Одно из наиболее интригующих открытий касается гибкого среднего сегмента белка, или линкера, который долгое время ускользал от структурного анализа. Команда засняла этот линкер, обёрнутый обратно на один концевой домен гефирина, где он одновременно стабилизирует белок и проникает в ту же поверхность, что и связывает рецепторы. В одной конформации часть линкера располагается внутри рецептор-связывающего кармана, фактически блокируя его; в другой она откидывается наружу, оставляя карман открытым для рецепторов. Несколько аминокислот, меняющих положение между этими «внутренним» и «внешним» состояниями, известны как мишени фосфорилирования — распространённой химической модификации, которую клетки используют как переключатель вкл/выкл. Это предполагает, что клетки мозга могут регулировать силу ингибирования, химически сдвигая линкер гефирина между блокирующей и приёмной формами.
Электростатический клей и жидкие капли
Исследование также выявляет заряженные остатки, действующие как электростатическое «велькро», помогая димерам гефирина связываться в структуры более высокого порядка и способствуя образованию белковых жидкоподобных капель, или конденсатов, внутри клеток. Когда исследователи мутировали ключевые положительные или отрицательные заряды, гефирин в культурах клеток утратил способность формировать крупные капли и собрался в гораздо меньшее или более мелкие кластеры. В нейронах те же мутации ослабляли накопление гефирина на ингибиторных синапсах, хотя изменённые белки всё ещё могли достигать этих участков. В совокупности эти эксперименты показывают, что те же заряженные участки и сегмент линкера, которые стабилизируют структуру гефирина, также необходимы для создания плотных скоплений рецепторов в реальных синапсах.
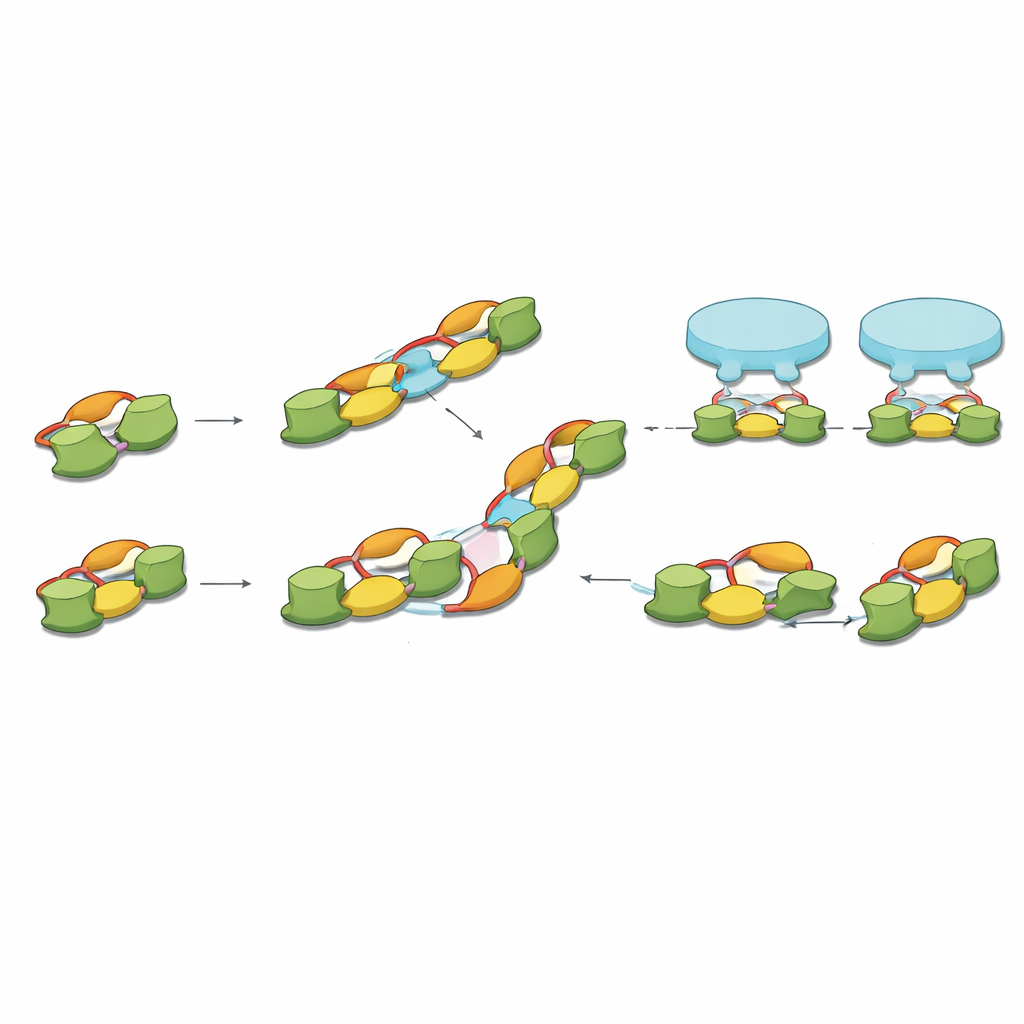
Связывание молекул с синаптическими узорами
Наконец, авторы связывают свои молекулярные «моментальные снимки» с ранней крио-электронной томографией цельной ткани мозга, которая измеряла характерное расстояние между соседними ингибиторными рецепторами. Длина димера-димеров гефирина тесно совпадает с этим расстоянием, и комбинации прямых и изломанных цепочек могут воссоздать наиболее распространённые схемы расположения рецепторов, наблюдаемые в нейронах. В этой модели димеры гефирина обеспечивают базовую скобу для пар рецепторов, а структуры более высокого порядка возникают, когда эти скобы соединяются бок о бок через заряженные интерфейсы.
Почему это важно для здоровья мозга
В целом работа заменяет простую тримерную схему гефирина динамичным, образующим цепочки каркасом, форма и способность связывать рецепторы которого могут настраиваться тонкими химическими метками на гибком линкере. Это помогает объяснить, как ингибиторные синапсы могут быть одновременно структурно упорядоченными и быстро поддающимися регулированию, а также даёт молекулярную основу для понимания болезнетворных мутаций, нарушающих сборку гефирина. Проясняя, как физически строится и модулируется тормозная система мозга, исследование открывает пути для вмешательства в баланс ингибирования при таких состояниях, как эпилепсия, расстройства аутистического спектра и тревожные расстройства.
Цитирование: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Ключевые слова: гефирин, ингибиторный синапс, GABAA рецептор, крио-электронная микроскопия, синаптический каркас