Clear Sky Science · fr
Structures Cryo-EM d’oligomères de gephyrine d’ordre supérieur révèlent les principes d’organisation de l’échafaudage postsynaptique inhibiteur
Comment les freins du cerveau restent accordés
Notre cerveau repose sur un équilibre délicat entre signaux « go » et « stop ». Les signaux « stop », portés par les synapses inhibitrices, empêchent une activité incontrôlée liée aux crises d’épilepsie, à l’anxiété et à d’autres troubles. Cette étude se penche sur la gephyrine, une protéine clé qui construit les échafaudages microscopiques maintenant les récepteurs inhibiteurs en place aux synapses. En visualisant les formes tridimensionnelles de la gephyrine par cryo‑microscopie électronique, les auteurs révèlent comment cette protéine s’auto‑assemble en structures plus larges qui organisent les récepteurs avec une précision surprenante.
L’architecte silencieux des synapses inhibitrices
Dans de nombreuses synapses inhibitrices, la gephyrine est le principal organisateur qui ancre deux types de récepteurs : les récepteurs à glycine et les récepteurs GABAA. Chaque molécule de gephyrine possède des domaines terminaux rigides reliés par une région centrale flexible, et différents variants d’épissage ajoutent une complexité supplémentaire. Pendant des années, les scientifiques ont pensé que la gephyrine pleine longueur formait principalement des assemblages à trois unités, et ces trimères servaient à esquisser des schémas en treillis de l’échafaudage postsynaptique. Cependant, des images récentes de tissu cérébral intact ont suggéré un réseau plus flexible de récepteurs et d’échafaudages, laissant entendre que la vision centrée sur le trimère était incomplète.
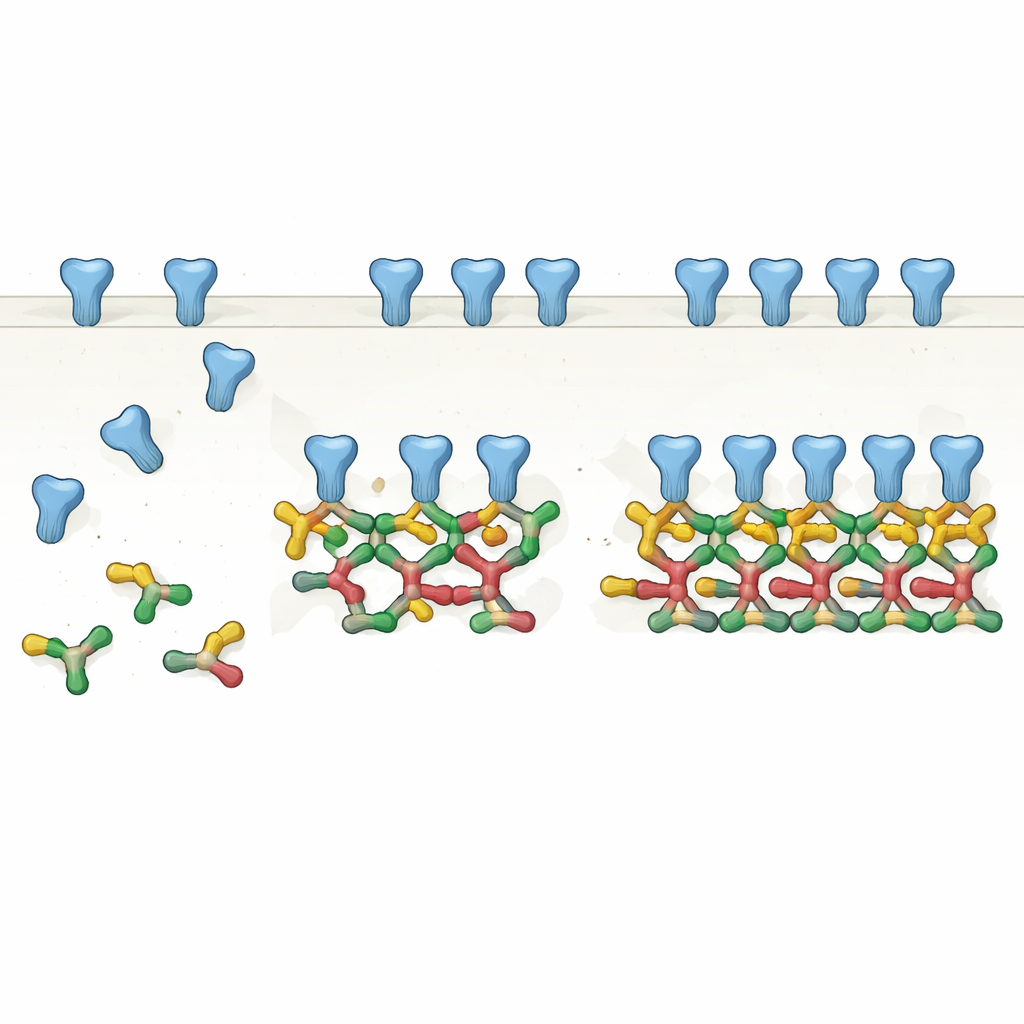
Des paires aux chaînes : une nouvelle vue de l’échafaudage
En purifiant soigneusement une forme d’épissage courante de la gephyrine pleine longueur et en l’analysant par plusieurs méthodes biochimiques, les auteurs montrent que la gephyrine forme naturellement des paires, ou dimères. Ces dimères servent ensuite d’éléments de base pour des structures plus grandes : des chaînes droites de quatre molécules (dimères de dimères) et même des chaînes à six éléments. Grâce à la cryo‑microscopie électronique, ils ont résolu des structures haute résolution de ces assemblages et découvert que des surfaces spécifiques d’une partie de la gephyrine entrent de manière répétée en contact avec des surfaces correspondantes de dimères voisins. Plutôt qu’un hub trimérique statique, la gephyrine apparaît comme un système modulaire pouvant s’étendre en chaînes linéaires et angulées, correspondant aux espacements et aux agencements des récepteurs observés dans des images in situ antérieures du cerveau.
Un lien flexible avec un interrupteur caché
Une des découvertes les plus intrigantes concerne le segment central flexible de la protéine, ou linker, qui a longtemps échappé à l’analyse structurale. L’équipe a capturé ce linker s’enroulant sur l’un des domaines terminaux de la gephyrine, où il stabilise la protéine tout en atteignant la même surface utilisée pour lier les récepteurs. Dans une conformation, une partie du linker siège à l’intérieur de la poche de liaison au récepteur, la bloquant effectivement ; dans une autre, il se replie vers l’extérieur, laissant la poche ouverte pour les récepteurs. Plusieurs acides aminés qui changent de position entre ces états « entré » et « sorti » sont connus pour être des cibles de phosphorylation, une modification chimique fréquente que les cellules utilisent comme interrupteur marche/arrêt. Cela suggère que les cellules du cerveau peuvent régler la force inhibitrice en faisant basculer chimiquement le linker de la gephyrine entre une conformation qui bloque le récepteur et une conformation qui l’accueille.
Colle électrostatique et gouttelettes liquides
L’étude identifie également des résidus chargés qui agissent comme un « velcro » électrostatique, aidant les dimères de gephyrine à se lier en chaînes d’ordre supérieur et favorisant la formation de gouttelettes protéiques de type liquide, ou condensats, à l’intérieur des cellules. Lorsque les chercheurs ont muté des charges positives ou négatives clés, la gephyrine dans des cellules en culture a perdu sa capacité à former de grandes gouttelettes et s’est assemblée en amas beaucoup moins nombreux ou plus petits. Dans les neurones, ces mêmes mutations ont affaibli l’accumulation de gephyrine aux synapses inhibitrices, bien que les protéines altérées puissent encore atteindre ces sites. Ensemble, ces expériences montrent que les mêmes régions chargées et le segment linker qui stabilisent la structure de la gephyrine sont aussi essentiels pour créer des agrégats denses de récepteurs aux synapses réelles.
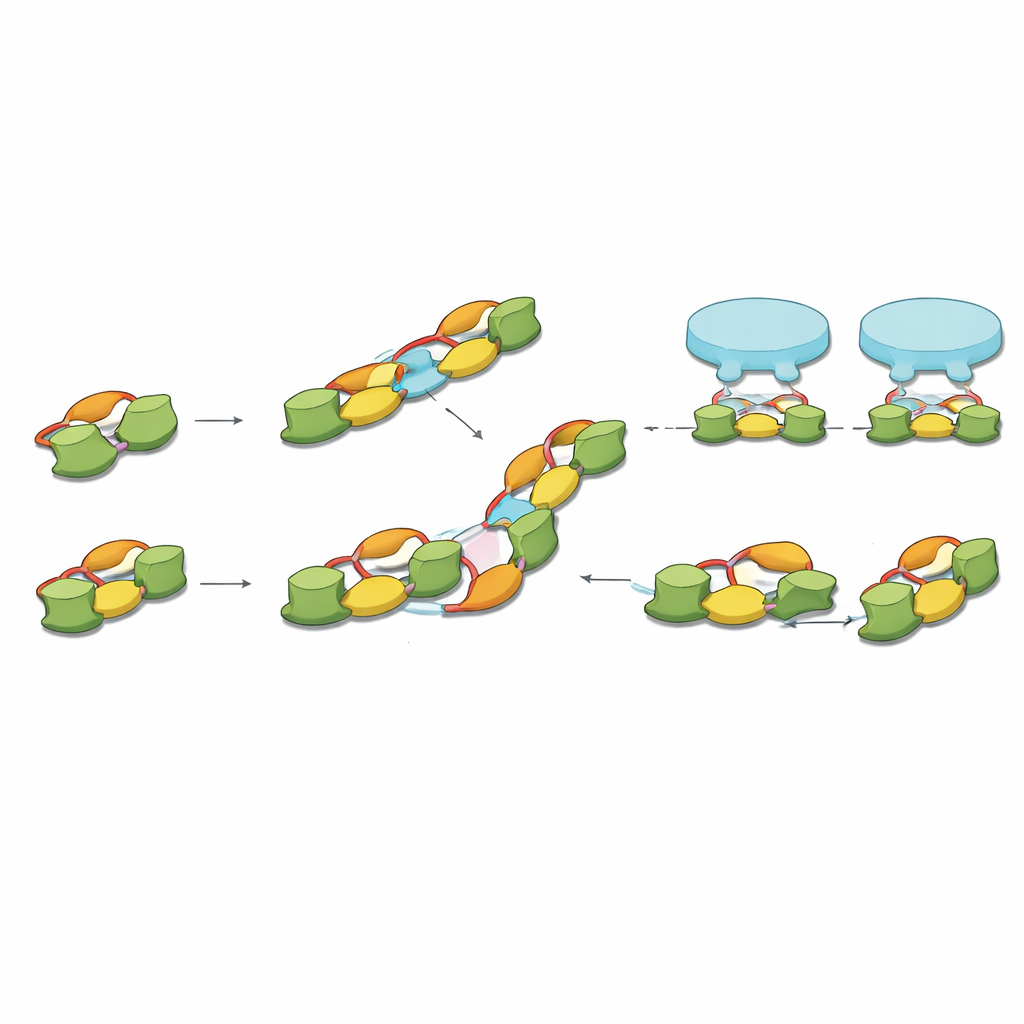
Relier les molécules aux motifs synaptiques
Enfin, les auteurs relient leurs instantanés moléculaires à la cryo‑tomographie électronique antérieure de tissu cérébral intact, qui avait mesuré un espacement caractéristique entre récepteurs inhibiteurs voisins. La longueur du dimère‑de‑dimères de gephyrine correspond étroitement à cet espacement, et des combinaisons de chaînes droites et angulées peuvent recréer les motifs de récepteurs les plus courants observés dans les neurones. Dans ce schéma, les dimères de gephyrine fournissent la pince de base pour les paires de récepteurs, et des chaînes d’ordre supérieur émergent lorsque ces pinces se connectent côte à côte via des interfaces chargées.
Pourquoi cela importe pour la santé cérébrale
Globalement, ce travail remplace le schéma simple centré sur le trimère par un échafaudage dynamique formant des chaînes dont la forme et la capacité de liaison aux récepteurs peuvent être modulées par de subtiles marques chimiques sur un linker flexible. Cela aide à expliquer comment les synapses inhibitrices peuvent être à la fois structurellement ordonnées et rapidement ajustables, et offre un cadre moléculaire pour comprendre les mutations liées à des maladies qui perturbent l’assemblage de la gephyrine. En clarifiant comment le système de freinage du cerveau est construit et modulé physiquement, l’étude ouvre des pistes pour cibler l’équilibre inhibiteur dans des affections telles que l’épilepsie, les troubles du spectre autistique et l’anxiété.
Citation: Ortiz-López, D., Hove, T.T., Huhn, C. et al. Cryo-EM structures of higher order Gephyrin oligomers reveal principles of inhibitory postsynaptic scaffold organization. Nat Commun 17, 3541 (2026). https://doi.org/10.1038/s41467-026-71771-8
Mots-clés: gephyrine, synapse inhibitrice, récepteur GABAA, cryomicroscopie électronique, échafaudage synaptique