Clear Sky Science · tr
p38 MAPK, hayatta kalma için dokular arası potasyum dengesini koordine ediyor
Günlük Sağlık Açısından Neden Önemli
Potasyum, gıda etiketlerinde sıkça gördüğünüz basit bir mineral olsa da vücutta eksikliği kas spazmlarına, kalp sorunlarına ve hatta yaşamı tehdit eden durumlara yol açabilir. Bu çalışma, hayvanların potasyum eksikliğini hücre hücre ele almadığını gösteriyor. Bunun yerine, p38 adı verilen stres algılayıcı bir yolak tarafından koordine edilen vücut çapında bir alarm-ve-yanıt sistemi kullanarak potasyum seviyelerini dengede tutuyor ve hayatta kalmayı sağlıyor. Bu sistemin küçük solucanlardan memelilere kadar kısmen korunmuş olması, insanlarda düşük potasyum ve yaşlanmayla ilişkili bozuklukları anlamaya yönelik yeni yaklaşımlar için ipuçları veriyor.
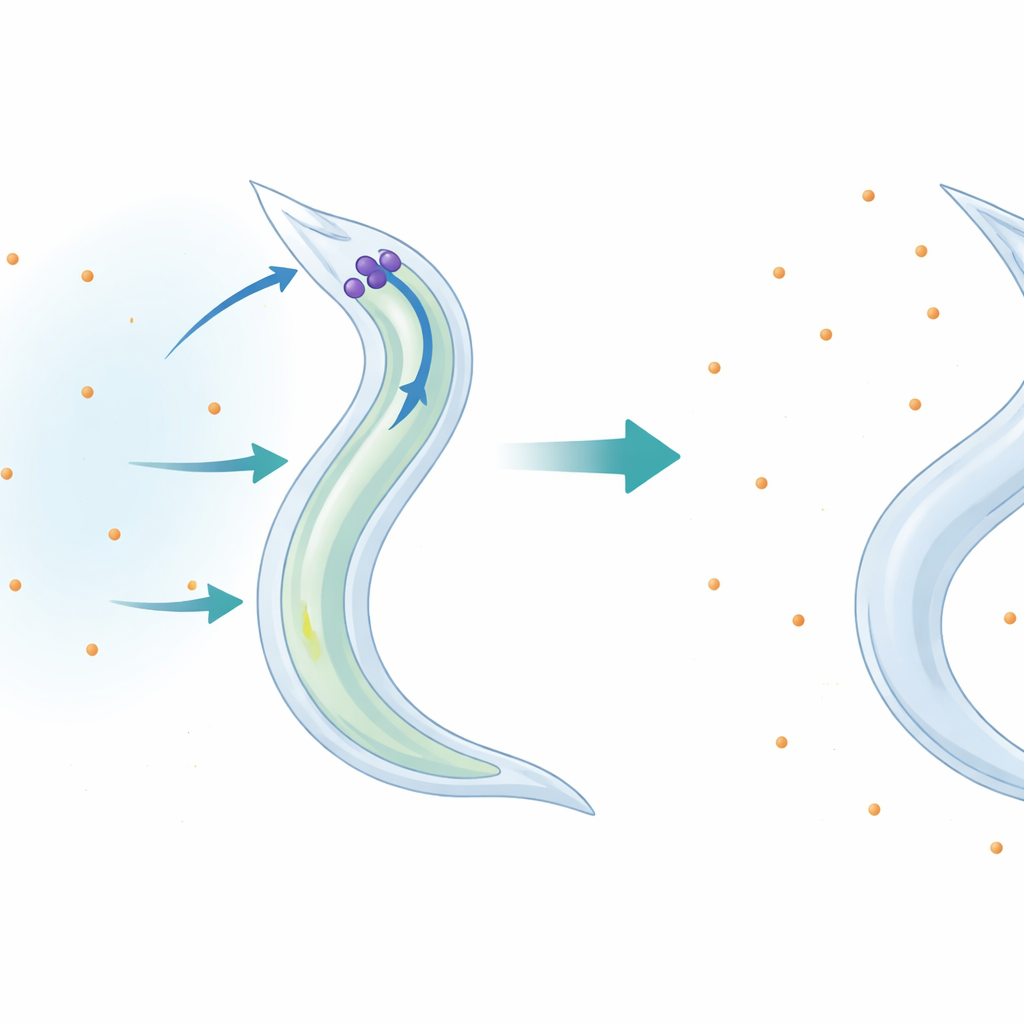
Potasyum Dengesine Penceresi Olan Küçük Bir Solucan
Araştırmacılar, diyetle gelen potasyum azaldığında neler olduğunu incelemek için mikroskobik solucan Caenorhabditis elegans’ı canlı bir model olarak kullandı. Erişkin solucanları, diğer tuzlar ve koşullar sabit tutulurken potasyum içermeyen veya farklı miktarlarda potasyum içeren kontrollü sıvı çözeltilere yerleştirdiler. İşleyen bir p38 sinyal yoluna sahip solucanlar, p38’in ana bileşenlerinden yoksun mutant solucanlara göre potasyum fakir koşullarda çok daha uzun süre hayatta kaldı. Potasyum klorür eklenmesi hassas mutantları kurtarırken sodyum veya kalsiyum tuzları kurtaramadı. Bu, sorunun genel bir “tuz stresi” değil, potasyum kaybıyla başa çıkamama olduğuna işaret etti.
Hayatta Kalma Genlerini Açan Bir Stres Yolağı
p38’in solucanların potasyum kıtlığına dayanmasına nasıl yardımcı olduğunu anlamak için ekip, bu yolaktaki tüm protein zincirini; üst akış sensörü (TIR-1) ile bir kinaz kaskadı (NSY-1, SEK-1, PMK-1) ve gen aktivitesini kontrol eden ATF-7 adlı transkripsiyon faktörüne kadar inceledi. Bu parçaların herhangi biri devre dışı bırakıldığında, solucanlar potasyum eksikliği altında hızla öldü; oysa birçok diğer iyi bilinen ömür ve stres genleri bu kadar kritik değildi. Genetik ekranlar ATF-7’yi merkezi bir oyuncu olarak gösterdi: ATF-7 “baskılayıcı” formda kilitlendiğinde hayatta kalma daha da kötüleşti; bu da p38’in ATF-7’yi değiştirerek potasyona karşı koruyucu belirli genleri açması ve zararlı baskıyı kapatması gerektiğini gösteriyor.
Derimsi Tabakada Bir Potasyum Pompası
Normal, yüksek-potasyum ve düşük-potasyum koşullarındaki solucanlarda gen aktivitesini karşılaştırarak, yazarlar yalnızca potasyum kıt olduğunda açılan yüzlerce gen buldular. Bunların çoğu tipik bağışıklık ve stres yanıtı genleriydi, ancak öne çıkan bir gen vardı: membranlar arasına potasyum taşıyan P-tipi ATPaz pompası CATP-3. CATP-3 eksikliği olan solucanlar, eksiklik durumunda p38 mutantlarına çok benziyordu: kas spazmları, vücut büzülmesi ve iç dokuların yırtılması gelişti ve dış potasyum birkaç milimolden azaldığında hızla öldüler. Floresan etiketlemeyle ekip, CATP-3’ün esas olarak hipodermiste — solucanın kasları ve iç organları saran deri benzeri dış hücre tabakasında — üretildiğini gösterdi. Yalnızca bu tabakada CATP-3’ü geri getirmek hayatta kalmayı kurtarmaya yetti; kas veya belirli nöronlarda ifade edilmesi ise yetmedi. Bu, hipodermisin tüm vücuda potasyum alımı için kilit bir geçit işlevi gördüğünü ima ediyor.
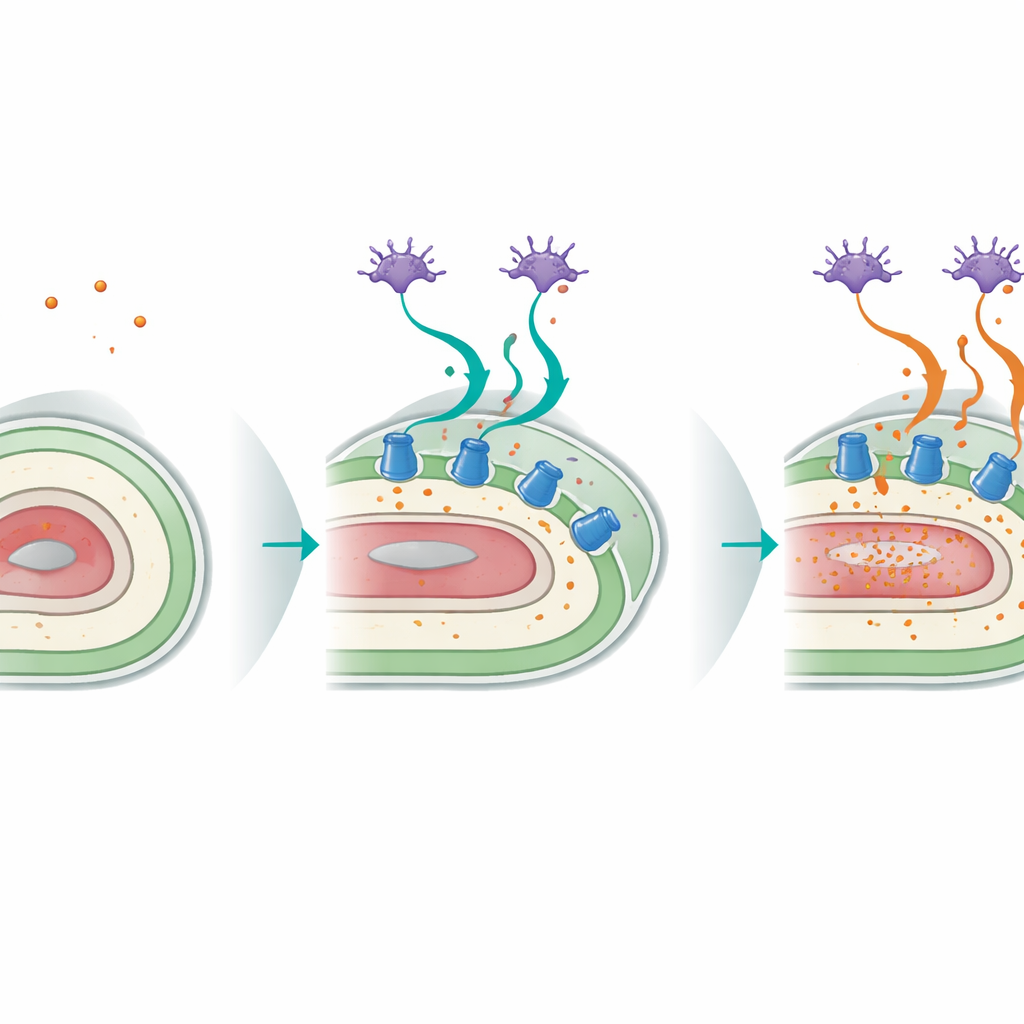
Algılayan Nöronlar ile Vücut Yüzeyi Arasında Karşılıklı Konuşma
Çalışma ayrıca solucanın duyusal nöronları ile hipodermisi arasında çarpıcı bir diyalog ortaya koydu. ASI olarak bilinen özel baş nöronları, normalde yiyecek ve diğer çevresel ipuçlarını algılar; potasyum kaybına verilen yanıtta p38 sinyallemesine güveniyorlar. p38 yalnızca ASI nöronlarında restorasyon edildiğinde, aksi halde mutant olan solucanlarda düşük potasyum altındaki hayatta kalma belirgin şekilde iyileşti ve hipodermisteki hayati CATP-3 pompası yeniden uyarıldı. Dokuya özgü gen susturma deneyleri, nöronlarda ve hipodermiste p38 fonksiyonunun hem gerekli hem de iç içe geçmiş olduğunu gösterdi: nöronlar besin tehdidini algılarken, deri benzeri doku koruyucu programı uygulayarak potasyum pompalarını devreye sokuyor. Bu dokular arası devre yaşla birlikte daha az etkili oluyor; CATP-3 ifadesi ve potasyum eksikliğiyle uyarılması her ikisi de azalıyor.
Solucanlardan Kaslara ve Mayaya Kadar Korunmuş Bir Strateji
Bu mantığın solucanların ötesine geçip geçmediğini test etmek için yazarlar fare kas hücreleri ve tomurcuklanan maya modellerine yöneldi. Kültürdeki fare miyoblastlarında hücrelerin kas lifi haline olgunlaşması için hem p38 aktivitesi hem de potasyum gerekliydi. Farklılaşma sırasında p38’e bağımlı genler, uyarılabilir dokularda iyon gradyanlarını koruyan Atp1a2 gibi belirli Na⁺/K⁺ pompa alt birimlerini içeriyordu. Mayada ise p38-benzeri kinaz Hog1 ve transkripsiyon faktörü Sko1, sodyum ve potasyum ihracını yöneten P-tipi ATPaz genlerini (ENA ailesi) düzenledi ve değişen tuz koşullarında hücre boyutunu etkiledi. Bu sistemler arasında ortak tema şuydu: p38-tipi bir stres yolakları, koşullar değiştiğinde potasyum dengesini stabilize etmek için enerji harcayan iyon pompalarının üretimini ayarlıyor.
Sağlık ve Yaşlanma İçin Anlamı
Basitçe ifade etmek gerekirse, bu çalışma potasyum dengesinin izole hücrelerin pasif iyon sızıntılarıyla değil, vücut çapında erken uyarı ağı tarafından korunduğunu gösteriyor. Bir stres sensörü (p38), çevresel algı nöronlarından gelen sinyalleri dinliyor ve sonra deri benzeri bariyere vücuda potasyumu geri çekecek daha fazla moleküler “pompa” kurmasını emrediyor; böylece kıtlık sırasında kaslar ve sinirler çökmekten korunuyor. Benzer kontrol sistemleri memeli kaslarında ve mayada da işliyor ve yaşla zayıflıyor. Bu devrenin nasıl çöktüğünü veya nasıl yeniden canlandırılabileceğini anlamak, nihayetinde hipokalemi, kas erimesi ve insanlarda yaşa bağlı gerilemeyle başa çıkma stratejilerine ışık tutabilir.
Atıf: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Anahtar kelimeler: potasyum homeostazı, p38 MAPK, Caenorhabditis elegans, iyon pompaları, yaşlanma