Clear Sky Science · nl
p38 MAPK orkestreert cross‑tissue kaliumhomeostase voor overleving
Waarom dit belangrijk is voor alledaagse gezondheid
Kalium is een eenvoudig mineraal dat op voedseletiketten voorkomt, maar te weinig ervan in het lichaam kan spierkrampen, hartproblemen en zelfs levensbedreigende situaties veroorzaken. Deze studie toont aan dat dieren niet één cel tegelijk met kaliumtekort omgaan. In plaats daarvan gebruiken ze een lichaamwijd alarm‑en‑reactiesysteem, gecoördineerd door een stress‑detecterend pad genaamd p38, om kaliumwaarden in balans te houden en overleving te waarborgen. Omdat dit systeem deels bewaard is van kleine wormen tot zoogdieren, wijst het op nieuwe manieren om menselijke aandoeningen gerelateerd aan laag kalium en veroudering te begrijpen.
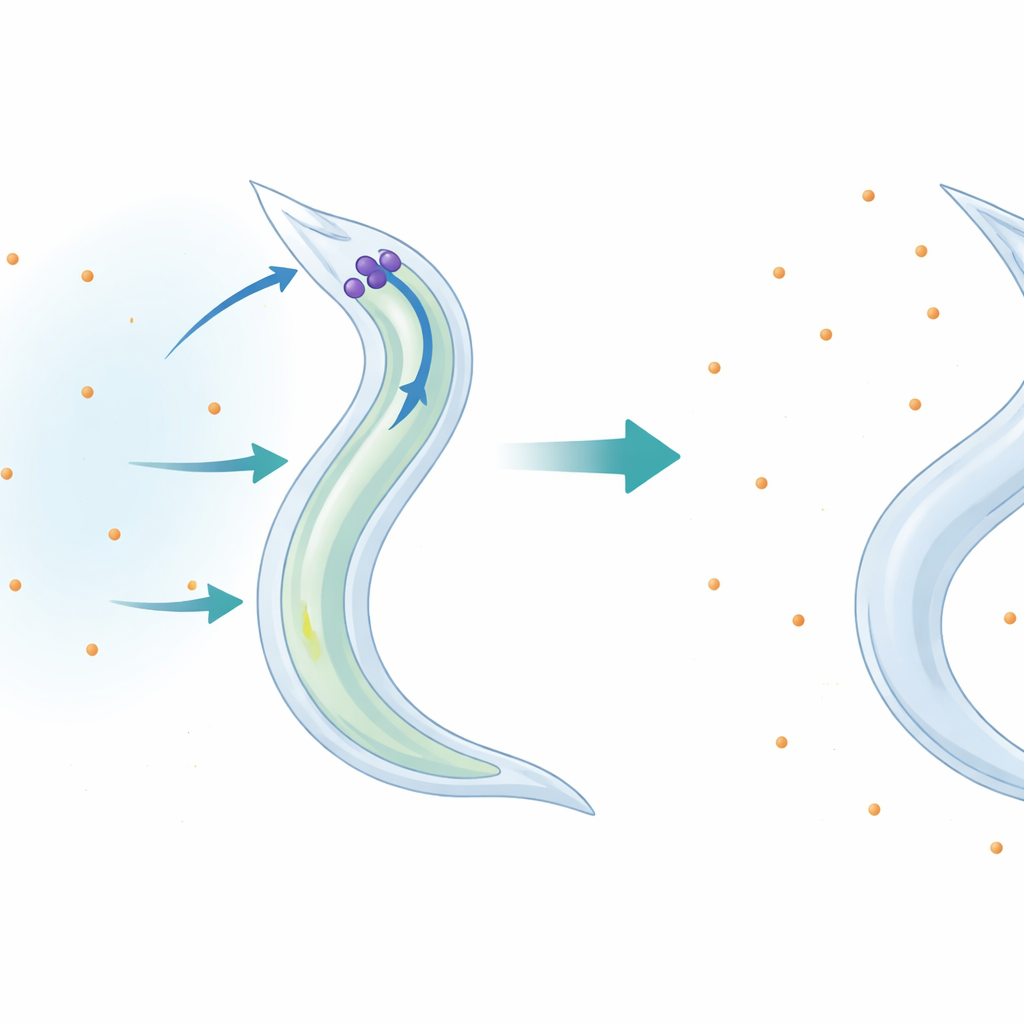
Een kleine worm als venster op kaliumbalans
De onderzoekers gebruikten de microscopische worm Caenorhabditis elegans als levend proefveld om te onderzoeken wat er gebeurt wanneer dieetkalium schaars is. Ze plaatsten volwassen wormen in zorgvuldig gecontroleerde vloeibare oplossingen die ofwel geen kalium bevatten of verschillende hoeveelheden daarvan, terwijl andere zouten en omstandigheden constant werden gehouden. Wormen met een werkend p38‑signaalpad overleefden kaliumarme omstandigheden veel langer dan mutante wormen die belangrijke p38‑componenten misten. Toediening van kaliumchloride redde de kwetsbare mutanten, terwijl natrium‑ of calciumsalzen dat niet deden. Dit toonde aan dat het probleem geen algemene “zoutstress” was, maar een specifieke onmogelijkheid om met kaliumverlies om te gaan.
Een stresspad dat overlevingsgenen inschakelt
Om te begrijpen hoe p38 wormen helpt kaliumtekort te doorstaan, ontleedde het team de volledige keten van eiwitten in dit pad, van een upstream sensor (TIR‑1) via een kinasecascade (NSY‑1, SEK‑1, PMK‑1) naar een transcriptiefactor genaamd ATF‑7, die genactiviteit reguleert. Wanneer een van deze schakels uitgeschakeld was, stierven wormen snel onder kaliumtekort, zelfs al waren veel andere bekende levensduur‑ en stressgenen veel minder kritisch. Genetische screens wezen ATF‑7 aan als een centraal speler: wanneer ATF‑7 in zijn "repressor"‑vorm vastgezet was, verslechterde de overleving nog verder, wat aangeeft dat p38 ATF‑7 moet modificeren om specifieke beschermende genen aan te zetten en schadelijke repressie uit te schakelen tijdens kaliumstress.
Een kaliumpomp in de huid‑achtige laag
Door genactiviteit te vergelijken in wormen onder normale, hoog‑kalium en laag‑kalium omstandigheden, vonden de auteurs honderden genen die alleen aangingen wanneer kalium schaars was. Veel daarvan waren typische immuun‑ en stressresponsgenen, maar één viel op: een P‑type ATPasepomp genaamd CATP‑3, gespecialiseerd in het verplaatsen van kalium over membranen. Wormen zonder CATP‑3 leken sterk op p38‑mutanten bij tekort: ze ontwikkelden spierkrampen, inkrimping van het lichaam en gescheurde inwendige weefsels, en stierven snel wanneer extern kalium onder een paar millimol daalde. Met behulp van fluorescerende tags toonden de onderzoekers aan dat CATP‑3 voornamelijk wordt geproduceerd in de hypodermis — het huidachtige buitenblad van de worm dat spieren en inwendige organen omsluit. Het herstellen van CATP‑3 alleen in deze laag was voldoende om de overleving te redden, terwijl expressie in spier of bepaalde neuronen dat niet deed, wat suggereert dat de hypodermis fungeert als sleutelpoort voor kaliumopname in het hele lichaam.
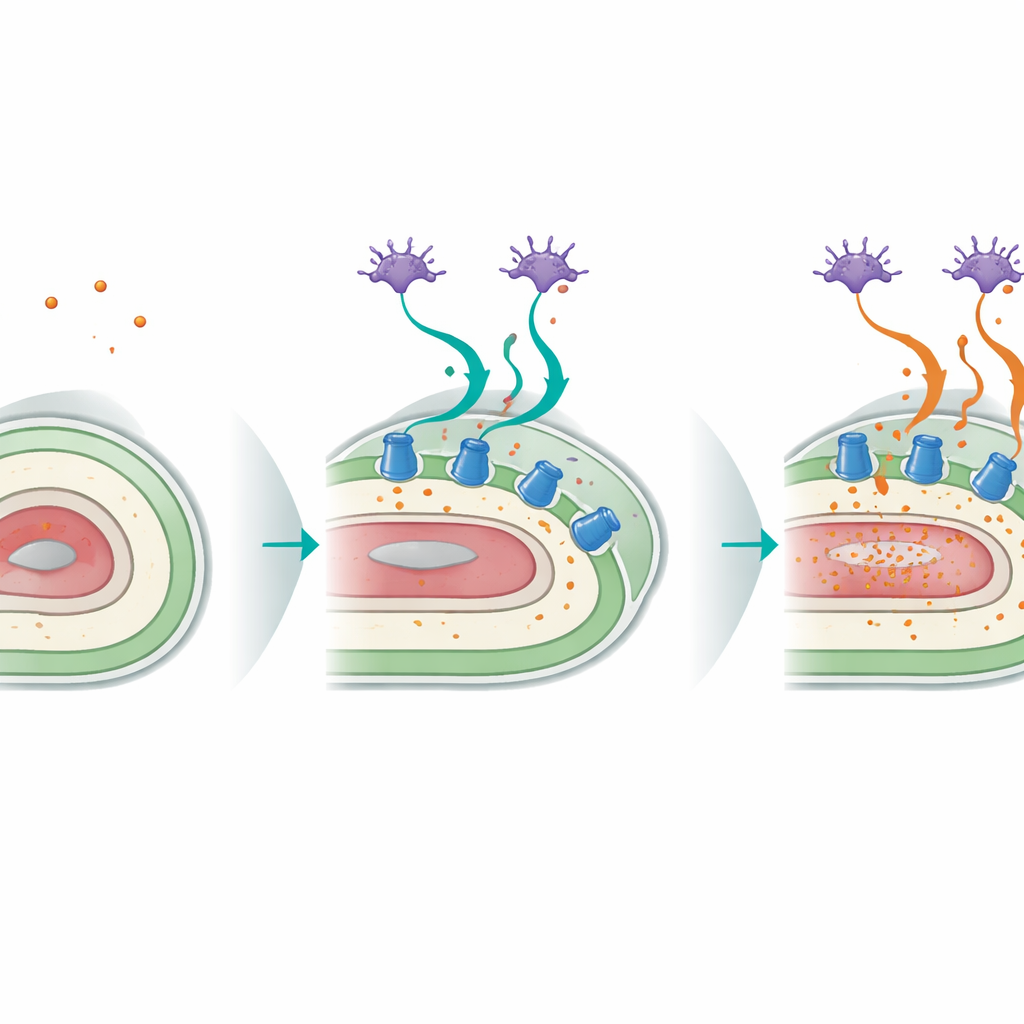
Communicatie tussen sensorische neuronen en het lichaamsoppervlak
De studie onthulde ook een opvallende dialoog tussen de sensorische neuronen van de worm en zijn hypodermis. Speciale kopneuronen, bekend als ASI, die normaal voedsel en andere omgevingssignalen detecteren, vertrouwen op p38‑signalering om de reactie op kaliumverlies mee te orkestreren. Toen p38 alleen in ASI‑neuronen van anderszins mutante wormen werd hersteld, verbeterde de overleving bij laag kalium sterk en werd de cruciale CATP‑3‑pomp in de hypodermis opnieuw geïnduceerd. Weefsel‑specifieke genstilleg‑experimenten toonden aan dat p38‑functie in neuronen en in de hypodermis zowel noodzakelijk als onderling verbonden is: neuronen detecteren de voedingsdreiging, terwijl het huidachtige weefsel het beschermende programma uitvoert door het opvoeren van kaliumpompen. Dit cross‑tissue circuit wordt minder effectief met de leeftijd, doordat de expressie van CATP‑3 en de inductie ervan door kaliumtekort beide afnemen.
Een geconserveerde strategie van wormen tot spieren en gist
Om te testen of deze logica verder gaat dan wormen, richtten de auteurs zich op muisspiercellen en gisteencellen. In gekweekte muismyoblasten waren p38‑activiteit en kalium beiden vereist voor de cellen om te rijpen tot samentrekkende spiervezels. Tijdens differentiatie behoorden p38‑afhankelijke genen tot specifieke Na⁺/K⁺‑pompondereenheden, zoals Atp1a2, die helpen ionengradiënten te behouden in prikkelbare weefsels. In gist reguleerden de p38‑achtige kinase Hog1 en de transcriptiefactor Sko1 P‑type ATPasegenen (ENA‑familie) die natrium‑ en kaliumexport beheren, en beïnvloedden ze de celgrootte onder variërende zoutomstandigheden. Over deze systemen heen kwam een geconserveerd thema naar voren: een p38‑achtig stresspad past de productie aan van energieverslindende ionpompen om kaliumbalans te stabiliseren wanneer de omstandigheden veranderen.
Wat dit betekent voor gezondheid en veroudering
In begrijpelijke termen laat dit werk zien dat kaliumbalans wordt bewaakt door een lichaamwijd vroegwaarschuwingsnetwerk, in plaats van door geïsoleerde cellen die passief ionen laten weglekken. Een stresssensor (p38) luistert naar signalen van omgevings‑sensorische neuronen en beveelt vervolgens aan de huidachtige barrière om meer moleculaire "pompen" te installeren die kalium terug het lichaam in trekken, zodat spieren en zenuwen niet falen tijdens tekorten. Vergelijkbare controlesystemen lijken te functioneren in zoogdierenspier en in gist, en verzwakken met de leeftijd. Begrijpen hoe deze schakeling faalt of kan worden nieuw leven ingeblazen, zou uiteindelijk strategieën kunnen informeren om hypokaliëmie, spierverlies en leeftijdsgerelateerde achteruitgang bij mensen te beheersen.
Bronvermelding: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Trefwoorden: kaliumhomeostase, p38 MAPK, Caenorhabditis elegans, ionpompen, veroudering