Clear Sky Science · fr
p38 MAPK orchestre l’homéostasie potassique intertissulaire pour la survie
Pourquoi cela compte pour la santé quotidienne
Le potassium est un minéral simple que l’on retrouve sur les étiquettes alimentaires, et pourtant une carence peut provoquer des spasmes musculaires, des problèmes cardiaques et même mettre la vie en danger. Cette étude montre que les animaux ne gèrent pas les pénuries de potassium cellule par cellule. Ils utilisent plutôt un système d’alerte et de réponse à l’échelle du corps, coordonné par une voie détectrice de stress appelée p38, pour maintenir l’équilibre potassique et préserver la survie. Parce que ce système est en partie conservé des petits vers aux mammifères, il suggère de nouvelles pistes pour comprendre les troubles humains liés à l’hypokaliémie et au vieillissement.
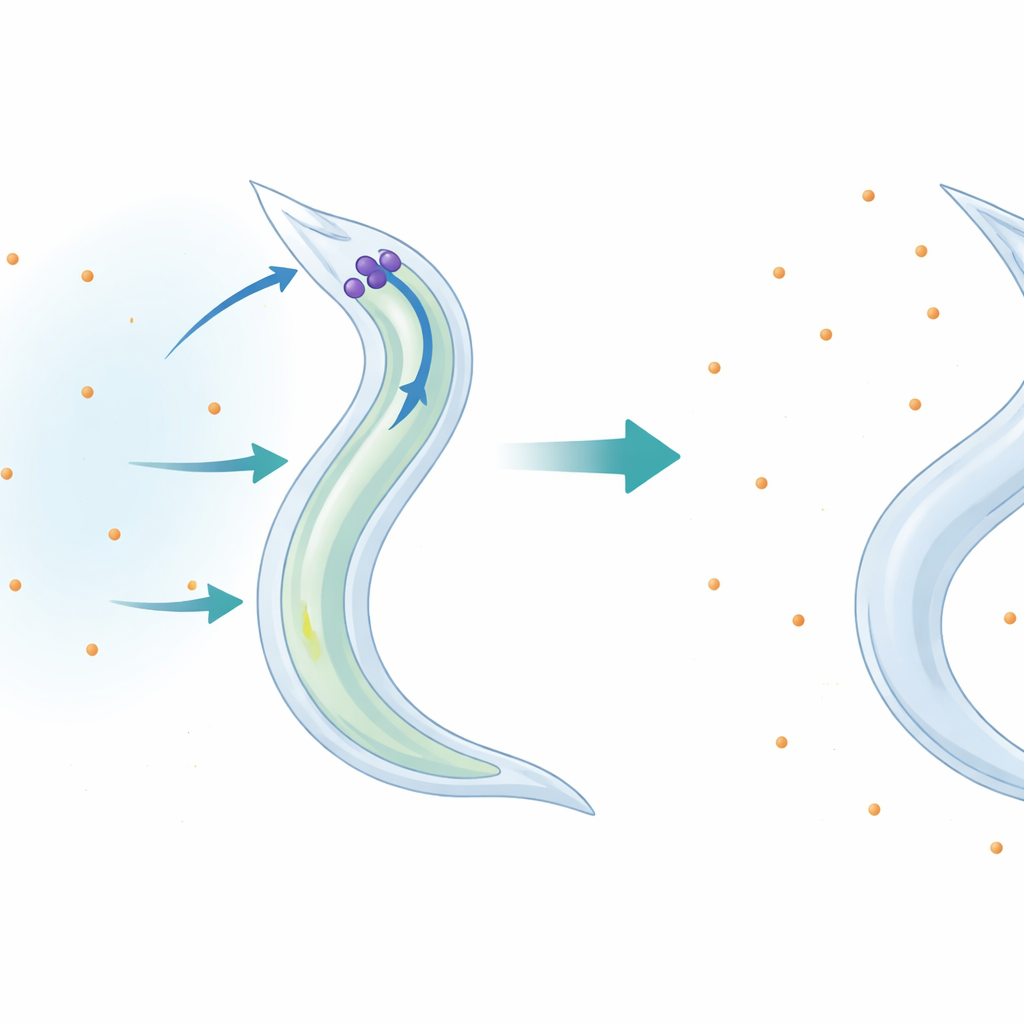
Un petit ver comme fenêtre sur l’équilibre potassique
Les chercheurs ont utilisé le ver microscopique Caenorhabditis elegans comme modèle vivant pour étudier ce qui se passe lorsque l’apport alimentaire en potassium diminue. Ils ont placé des vers adultes dans des solutions liquides soigneusement contrôlées, dépourvues de potassium ou contenant différentes concentrations, en maintenant constants les autres sels et conditions. Les vers avec une voie de signalisation p38 fonctionnelle ont survécu beaucoup plus longtemps en conditions de faible potassium que les mutants dépourvus de composants clés de p38. L’ajout de chlorure de potassium a sauvé les mutants fragiles, alors que des sels de sodium ou de calcium n’ont pas eu cet effet. Cela montre que le problème n’était pas un « stress salin » générique mais une incapacité spécifique à faire face à la perte de potassium.
Une voie de stress qui active des gènes de survie
Pour comprendre comment p38 aide les vers à résister à la pénurie de potassium, l’équipe a disséqué la chaîne complète de protéines de cette voie, depuis un détecteur en amont (TIR-1) via une cascade de kinases (NSY-1, SEK-1, PMK-1) jusqu’à un facteur de transcription appelé ATF-7, qui contrôle l’activité génétique. Lorsque l’un de ces éléments était désactivé, les vers mouraient rapidement en situation de carence potassique, alors que de nombreux autres gènes connus pour la longévité ou la réponse au stress étaient beaucoup moins critiques. Des criblages génétiques ont identifié ATF-7 comme un acteur central : lorsque ATF-7 était verrouillé sous sa forme « répresseur », la survie était encore pire, indiquant que p38 doit modifier ATF-7 pour activer certains gènes protecteurs et lever des répressions nuisibles pendant le stress potassique.
Une pompe à potassium dans la couche semblable à la peau
En comparant l’activité génique des vers en conditions normales, riches ou pauvres en potassium, les auteurs ont trouvé des centaines de gènes qui s’exprimaient uniquement lorsque le potassium faisait défaut. Beaucoup étaient des gènes typiques de la réponse immunitaire et du stress, mais un gène a émergé : une ATPase de type P nommée CATP-3, spécialisée dans le transport du potassium à travers les membranes. Les vers dépourvus de CATP-3 ressemblaient beaucoup aux mutants p38 en carence : ils développaient des spasmes musculaires, un rétrécissement corporel et des ruptures de tissus internes, et mouraient rapidement lorsque le potassium extérieur tombait en dessous de quelques millimoles. Grâce à des balises fluorescentes, l’équipe a montré que CATP-3 est principalement produite dans l’hypoderme — la couche extérieure semblable à la peau qui enveloppe les muscles et les organes internes. Restaurer CATP-3 uniquement dans cette couche suffisait à sauver la survie, tandis que son expression dans les muscles ou certains neurones ne le faisait pas, ce qui implique que l’hypoderme agit comme un passage clé pour l’entrée du potassium dans tout le corps.
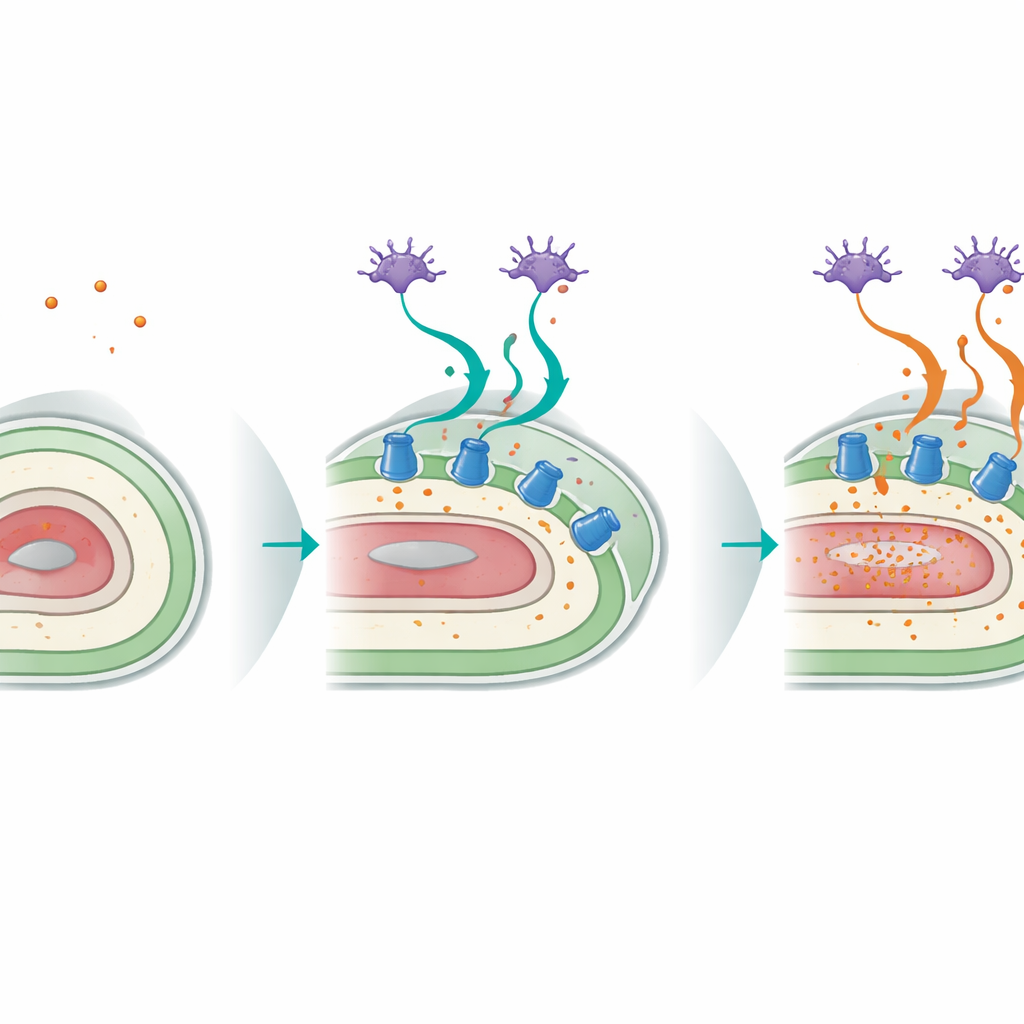
Dialogue entre neurones sensoriels et surface corporelle
L’étude a aussi mis au jour un dialogue saisissant entre les neurones sensoriels du ver et son hypoderme. Des neurones spéciaux de la tête, appelés ASI, qui détectent normalement la nourriture et d’autres indices environnementaux, dépendent de la signalisation p38 pour orchestrer la réponse à la perte de potassium. Lorsque p38 était restauré uniquement dans les neurones ASI de vers par ailleurs mutants, la survie en basse teneur en potassium s’améliorait nettement, et la pompe CATP-3 essentielle dans l’hypoderme était ré-induite. Des expériences de silencement génique tissulaire ont montré que la fonction de p38 dans les neurones et dans l’hypoderme est à la fois nécessaire et interconnectée : les neurones détectent la menace nutritionnelle, tandis que le tissu semblable à la peau exécute le programme protecteur en augmentant les pompes à potassium. Ce circuit intertissulaire devient moins efficace avec l’âge, l’expression de CATP-3 et son induction par la carence potassique diminuant toutes deux.
Une stratégie conservée du ver aux muscles et aux levures
Pour vérifier si cette logique s’applique au-delà des vers, les auteurs se sont tournés vers les cellules musculaires de souris et la levure de boulanger. Dans des myoblastes de souris en culture, l’activité p38 et la présence de potassium étaient toutes deux nécessaires pour que les cellules mûrissent en fibres musculaires contractiles. Lors de la différenciation, des gènes dépendants de p38 incluaient des sous-unités spécifiques de la pompe Na⁺/K⁺, telles qu’Atp1a2, qui aident à maintenir les gradients ioniques dans les tissus excitable. Chez la levure, la kinase de type p38 Hog1 et le facteur de transcription Sko1 régulaient des gènes d’ATPases de type P (famille ENA) qui gèrent l’exportation du sodium et du potassium, et influençaient la taille cellulaire selon les conditions salines. À travers ces systèmes, un thème conservé apparaît : une voie de stress de type p38 ajuste la production de pompes ioniques énergivores pour stabiliser l’équilibre potassique lorsque les conditions changent.
Ce que cela signifie pour la santé et le vieillissement
En termes accessibles, ce travail montre que l’équilibre potassique est protégé par un réseau d’alerte précoce à l’échelle du corps, plutôt que par des cellules isolées laissant simplement fuir des ions. Un capteur de stress (p38) écoute les signaux des neurones détectant l’environnement, puis ordonne à la barrière semblable à la peau d’installer davantage de « pompes » moléculaires qui réintroduisent le potassium dans l’organisme, empêchant muscles et nerfs de défaillir lors des pénuries. Des systèmes de contrôle similaires semblent opéreraient dans le muscle des mammifères et chez la levure, et ils s’affaiblissent avec l’âge. Comprendre comment ce circuit faillit ou peut être revigoré pourrait, à terme, éclairer des stratégies pour gérer l’hypokaliémie, la fonte musculaire et le déclin lié à l’âge chez l’humain.
Citation: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Mots-clés: homéostasie du potassium, p38 MAPK, Caenorhabditis elegans, pompes ioniques, vieillissement