Clear Sky Science · sv
p38 MAPK orkestrerar tvärvävnadigt kaliumbalans för överlevnad
Varför detta betyder något för vardaglig hälsa
Kalium är ett enkelt mineral som syns på näringsdeklarationer, men för lite av det i kroppen kan utlösa muskelspasmer, hjärtproblem och till och med bli livshotande. Denna studie visar att djur inte hanterar kaliumbrist cell för cell. I stället använder de ett kroppsomfattande larmsystem, koordinerat av en stresskänslig signalväg kallad p38, för att hålla kaliumnivåerna i balans och bevara överlevnad. Eftersom detta system delvis är bevarat från små maskar till däggdjur ger det ledtrådar till nya sätt att förstå mänskliga sjukdomar som kopplas till låg kaliumhalt och åldrande.
En liten mask som fönster mot kaliumbalans
Forskarna använde den mikroskopiska masken Caenorhabditis elegans som ett levande testfält för att undersöka vad som händer när dietärt kalium blir knapp. De placerade vuxna maskar i noggrant kontrollerade vätskelösningar som antingen saknade kalium eller innehöll olika mängder av det, samtidigt som andra salter och villkor hölls konstanta. Maskar med en fungerande p38-signalväg överlevde kaliumfattiga förhållanden betydligt längre än mutanta maskar som saknade viktiga p38-komponenter. Tillsats av kaliumklorid räddade de känsliga mutanterna, medan natrium- eller kalciumsalter inte kunde göra det. Detta visade att problemet inte var generisk ”saltstress” utan en specifik oförmåga att hantera kaliumförlust.
En stressväg som slår på överlevnadsgener
För att förstå hur p38 hjälper maskar att stå emot kaliumbrist dissekerade teamet hela kedjan av proteiner i denna väg, från en uppströms sensor (TIR-1) genom en kinas-kaskad (NSY-1, SEK-1, PMK-1) ner till en transkriptionsfaktor kallad ATF-7, som styr genaktivitet. När någon av dessa delar stängdes av dog maskarna snabbt vid kaliumbrist, även om många andra välkända långlivnads- och stressgener var mycket mindre kritiska. Genetiska screeningar pekade ut ATF-7 som en central aktör: när ATF-7 låstes i sin ”repressor”-form blev överlevnaden ännu sämre, vilket indikerar att p38 måste modifiera ATF-7 för att slå på särskilda skyddsgener och stänga av skadlig repression under kaliumstress.
En kaliumpump i hudliknande lagret
Genom att jämföra genaktivitet i maskar under normala, högkalium- och lågkaliumförhållanden fann författarna hundratals gener som aktiverades endast när kalium var knapp. Många av dessa var typiska immunsystem- och stressresponsgener, men en stack ut: en P-typ ATPaspump kallad CATP-3, specialiserad för att flytta kalium över membran. Maskar utan CATP-3 liknade p38-mutanter under brist: de utvecklade muskelspasmer, kroppssammansnörning och ruptur av inre vävnader, och dog snabbt när det yttre kaliumet föll under några millimolar. Med hjälp av fluorescerande taggar visade teamet att CATP-3 främst produceras i hypodermis — maskens hudliknande yttre cellskikt som omsluter muskler och inre organ. Återställande av CATP-3 endast i detta lager var tillräckligt för att rädda överlevnad, medan uttryck i muskel eller vissa neuroner inte var det, vilket tyder på att hypodermis agerar som en nyckelport för kaliumupptag till hela kroppen.
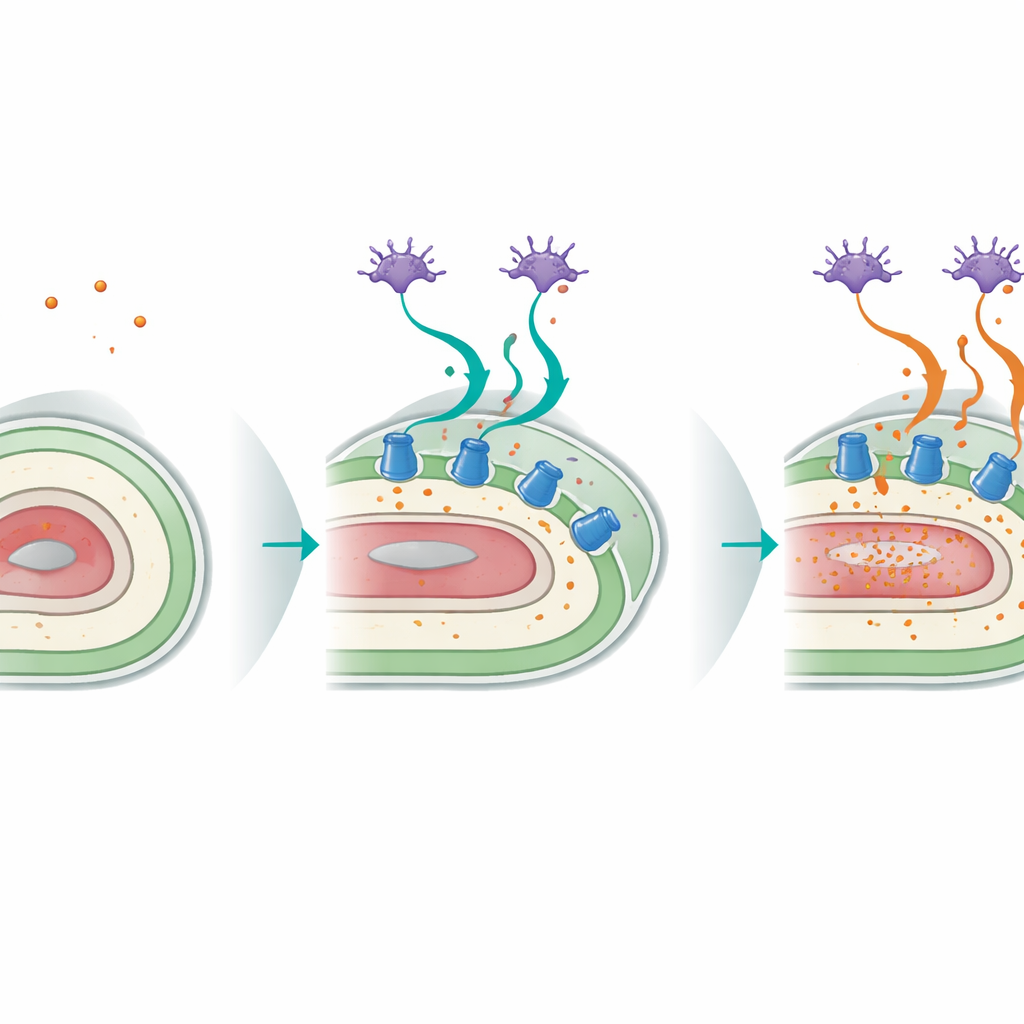
Tvärvävnadigt samtal mellan sensoriska neuroner och kroppens yta
Studien avslöjade också en påtaglig dialog mellan maskens sensoriska neuroner och dess hypodermis. Särskilda huvudneuroner kända som ASI, som normalt känner av mat och andra miljöledtrådar, är beroende av p38-signalering för att hjälpa till att orkestrera responsen på kaliumförlust. När p38 återställdes endast i ASI-neuroner hos annars mutanta maskar förbättrades överlevnaden under lågkalium avsevärt, och den avgörande CATP-3-pumpen i hypodermis inducerades igen. Vävnadsspecifika gen-silencings-experiment visade att p38-funktion i neuroner och i hypodermis både är nödvändig och sammanflätad: neuronerna känner av näringshotet, medan det hudliknande vävnadsskiktet utför det skyddande programmet genom att öka produktionen av kaliumpumpar. Denna tvärvävnadscircuit blir mindre effektiv med åldern, eftersom uttrycket av CATP-3 och dess induktion av kaliumbrist båda avtar.
En bevarad strategi från maskar till muskler och jäst
För att testa om denna logik sträcker sig bortom maskar vände författarna sig till musmuskulaturceller och jäst. I odlade musmyoblaster krävdes både p38-aktivitet och kalium för att cellerna skulle mogna till kontraherande muskelfibrer. Under differentiering ingick p38-beroende gener specifika Na⁺/K⁺-pumpsubenheter, såsom Atp1a2, som hjälper till att upprätthålla jongradienter i exciterbara vävnader. I jäst reglerade den p38-liknande kinasen Hog1 och transkriptionsfaktorn Sko1 P-typ ATPasgener (ENA-familjen) som hanterar natrium- och kaliumutflöde, och påverkade cellstorlek vid varierande saltförhållanden. I dessa system framträdde ett bevarat tema: en p38-typ stressväg justerar produktionen av energikrävande jonpumpar för att stabilisera kaliumbalansen när förhållandena förändras.
Vad detta betyder för hälsa och åldrande
Enkelt uttryckt visar detta arbete att kaliumbalans skyddas av ett kroppsomfattande tidigt varningsnät, snarare än av isolerade celler som passivt läcker joner. En stressensor (p38) lyssnar på signaler från miljökännande neuroner och beordrar sedan det hudliknande barriärskiktet att installera fler molekylära ”pumpar” som drar in kalium i kroppen igen, så att muskler och nerver inte kollapsar vid brist. Liknande kontrollsystem verkar finnas i däggdjursmuskulatur och i jäst, och de försvagas med åldern. Att förstå hur denna krets brister eller kan återaktiveras kan så småningom ge underlag för strategier att hantera hypokalemi, muskelförtvining och åldersrelaterad försämring hos människor.
Citering: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Nyckelord: kaliumhomeostas, p38 MAPK, Caenorhabditis elegans, jonpumpar, åldrande