Clear Sky Science · de
p38 MAPK orchestriert gewebsübergreifende Kalium‑Homöostase zum Überleben
Warum das für die Alltagsgesundheit wichtig ist
Kalium ist ein einfacher Mineralstoff, der auf Nährwertangaben auftaucht — zu wenig davon im Körper kann jedoch Muskelkrämpfe, Herzprobleme und sogar lebensbedrohliche Zustände auslösen. Diese Studie zeigt, dass Tiere Kaliummangel nicht Zelle für Zelle bewältigen. Stattdessen verwenden sie ein körperweites Alarm‑und‑Antwort‑System, das von einem Stress‑Erkennungsweg namens p38 koordiniert wird, um Kaliumspiegel auszugleichen und das Überleben zu sichern. Weil dieses System teilweise von winzigen Würmern bis zu Säugetieren konserviert ist, deutet es auf neue Ansätze hin, menschliche Erkrankungen im Zusammenhang mit niedrigem Kalium und dem Altern besser zu verstehen.
Ein winziger Wurm als Fenster in die Kalium‑Balance
Die Forscher nutzten den mikroskopischen Wurm Caenorhabditis elegans als lebendes Modell, um zu untersuchen, was passiert, wenn die diätetische Kaliumzufuhr knapp wird. Sie setzten adulte Würmer in kontrollierte Flüssigkeitslösungen, die entweder kein Kalium oder unterschiedliche Mengen davon enthielten, während andere Salze und Bedingungen konstant gehalten wurden. Würmer mit intaktem p38‑Signalweg überlebten kaliumarme Bedingungen deutlich länger als Mutanten, denen wesentliche p38‑Komponenten fehlten. Die Zugabe von Kaliumchlorid rettete die empfindlichen Mutanten, Natrium‑ oder Calciumsalze konnten das nicht. Das zeigte, dass es sich nicht um generischen „Salzstress“ handelte, sondern um eine spezifische Unfähigkeit, mit Kaliumverlust umzugehen.
Ein Stressweg, der Überlebensgene einschaltet
Um zu verstehen, wie p38 Würmern hilft, Kaliumknappheit zu überstehen, zerlegten die Autoren die komplette Proteinkette dieses Wegs — vom upstream Sensor (TIR‑1) über eine Kinasenkaskade (NSY‑1, SEK‑1, PMK‑1) bis zu einem Transkriptionsfaktor namens ATF‑7, der die Genaktivität steuert. Wenn ein Glied dieser Kette ausgeschaltet war, starben die Würmer unter Kaliumdefizienz schnell, obwohl viele andere bekannte Langlebigkeits‑ und Stressgene weit weniger kritisch waren. Genetische Screens identifizierten ATF‑7 als zentralen Akteur: Befand sich ATF‑7 in seiner „Repressor“‑Form, verschlechterte sich das Überleben weiter, was darauf hindeutet, dass p38 ATF‑7 modifizieren muss, um spezifische schützende Gene einzuschalten und schädliche Repressionen während des Kaliumstresses zu lösen.
Eine Kaliumpumpe in der hautähnlichen Schicht
Durch den Vergleich der Genaktivität bei Würmern unter normalen, hohen und niedrigen Kaliumverhältnissen fanden die Autoren Hunderte von Genen, die nur bei Kaliumknappheit hochreguliert wurden. Viele davon waren typische Immun‑ und Stressantwortgene, doch ein Gen ragte heraus: eine P‑Typ ATPase‑Pumpe namens CATP‑3, spezialisiert auf den Transport von Kalium über Membranen. Würmer ohne CATP‑3 ähnelten unter Mangelzuständen stark den p38‑Mutanten: Sie entwickelten Muskelkrämpfe, Körper‑Schrumpfung und Rupturen innerer Gewebe und starben schnell, wenn das äußere Kalium unter wenige Millimol fiel. Mit fluoreszenten Markern zeigten die Autoren, dass CATP‑3 hauptsächlich in der Hypodermis produziert wird — der hautähnlichen äußeren Zellschicht des Wurms, die Muskeln und innere Organe umhüllt. Die Wiederherstellung von CATP‑3 nur in dieser Schicht reichte aus, um das Überleben zu retten, während seine Expression in Muskelzellen oder bestimmten Neuronen das nicht tat. Das legt nahe, dass die Hypodermis als entscheidendes Tor für die Kaliumaufnahme in den gesamten Körper fungiert.
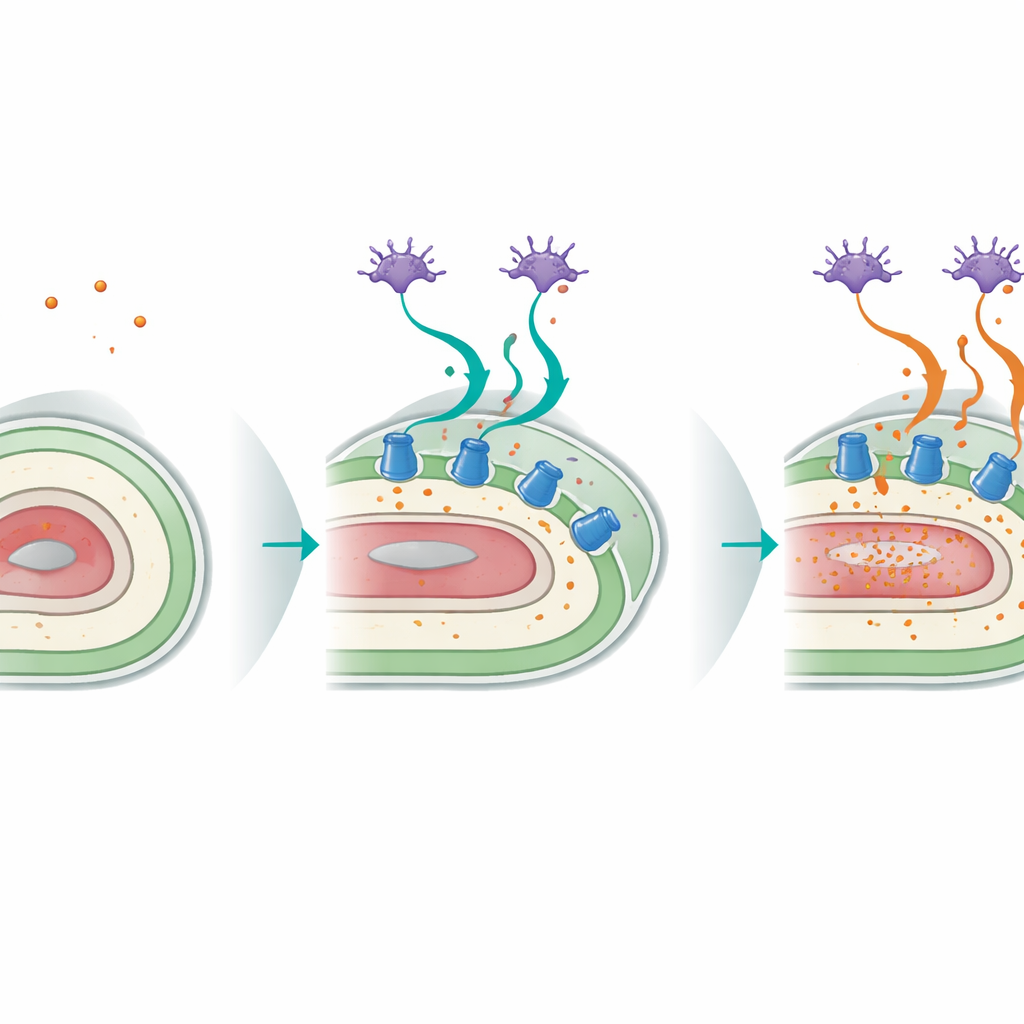
Dialog zwischen sensorischen Neuronen und der Körperoberfläche
Die Studie deckte außerdem einen markanten Dialog zwischen den sensorischen Neuronen des Wurms und seiner Hypodermis auf. Spezielle Kopfneuronen, bekannt als ASI, die normalerweise Nahrung und Umweltreize wahrnehmen, sind auf p38‑Signalgebung angewiesen, um die Reaktion auf Kaliumverlust mitzuorganisieren. Wenn p38 nur in den ASI‑Neuronen sonst mutanter Würmer wiederhergestellt wurde, verbessertes sich das Überleben bei niedrigem Kalium deutlich, und die entscheidende CATP‑3‑Pumpe in der Hypodermis wurde erneut induziert. Gewebespezifische Genstilllegungs‑Experimente zeigten, dass p38‑Funktion sowohl in Neuronen als auch in der Hypodermis notwendig und miteinander verknüpft ist: Neuronen erkennen die Nährstoffbedrohung, während das hautähnliche Gewebe das Schutzprogramm ausführt, indem es Kaliumpumpen hochfährt. Dieser gewebsübergreifende Schaltkreis wird mit dem Alter weniger wirksam, da die Expression von CATP‑3 und seine Induktion durch Kaliummangel abnehmen.
Eine konservierte Strategie von Würmern bis zu Muskeln und Hefe
Um zu prüfen, ob diese Logik über Würmer hinaus gilt, untersuchten die Autoren Mausmuskelzellen und Bäckerhefe. In kultivierten Mausmyoblasten waren sowohl p38‑Aktivität als auch Kalium erforderlich, damit sich die Zellen zu kontrahierenden Muskelfasern differenzieren. Während der Differenzierung gehörten p38‑abhängige Gene zu spezifischen Na⁺/K⁺‑Pump‑Untereinheiten, wie Atp1a2, die helfen, Ionen‑Gradienten in erregbaren Geweben aufrechtzuerhalten. In Hefe regulierten die p38‑ähnliche Kinase Hog1 und der Transkriptionsfaktor Sko1 P‑Typ ATPase‑Gene (ENA‑Familie), die Natrium‑ und Kaliumexport steuern, und beeinflussten die Zellgröße unter variierenden Salzbedingungen. In all diesen Systemen zeigte sich ein konserviertes Muster: Ein p38‑artiger Stressweg passt die Produktion energieintensiver Ionenpumpen an, um die Kaliumbalance bei veränderten Bedingungen zu stabilisieren.
Was das für Gesundheit und Altern bedeutet
Anschaulich zeigt diese Arbeit, dass die Kaliumbalance von einem körperweiten Frühwarnnetz bewacht wird, statt von isolierten Zellen, die passiv Ionen verlieren. Ein Stresssensor (p38) hört auf Signale von umweltwahrnehmenden Neuronen und befiehlt dann der hautähnlichen Barriere, mehr molekulare „Pumpen“ zu installieren, die Kalium wieder in den Körper holen, damit Muskeln und Nerven bei Mangel nicht versagen. Ähnliche Kontrollsysteme scheinen in Säugetiermuskeln und in Hefe zu wirken, und sie schwächen mit dem Alter ab. Zu verstehen, wie diese Schaltkreise versagen oder reaktiviert werden können, könnte langfristig helfen, Hypokaliämie, Muskelschwund und altersbedingten Leistungsabfall beim Menschen zu behandeln.
Zitation: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Schlüsselwörter: Kalium‑Homöostase, p38 MAPK, Caenorhabditis elegans, Ionenpumpen, Altern