Clear Sky Science · pl
p38 MAPK orkiestruje międzypowierzchniową homeostazę potasu dla przeżycia
Dlaczego to ma znaczenie dla codziennego zdrowia
Potas to prosty minerał często podawany na etykietach żywności, ale jego niedobór w organizmie może wywołać skurcze mięśni, problemy z sercem, a nawet zagrażać życiu. Badanie pokazuje, że zwierzęta nie radzą sobie z niedoborem potasu w pojedynczych komórkach — stosują zamiast tego ogólnoustrojowy system alarmowo‑odpowiedziowy, koordynowany przez szlak wykrywający stres zwany p38, który utrzymuje równowagę potasową i wspiera przeżycie. Ponieważ elementy tego systemu są częściowo zachowane od maleńkich nicieni po ssaki, wyniki sugerują nowe perspektywy dla zrozumienia ludzkich zaburzeń związanych z niskim poziomem potasu i procesami starzenia.
Malutki robak jako okno na równowagę potasową
Naukowcy użyli mikroskopijnego nicienia Caenorhabditis elegans jako żywego modelu, by zbadać, co się dzieje przy niskiej zawartości potasu w diecie. Dorosłe robaki umieszczono w precyzyjnie kontrolowanych roztworach płynnych pozbawionych potasu lub zawierających jego różne stężenia, przy zachowaniu stałych pozostałych soli i warunków. Robaki z działającym szlakiem sygnałowym p38 przeżywały dłużej w warunkach ubogich w potas niż mutanty pozbawione kluczowych składników p38. Dodanie chlorku potasu ratowało wrażliwe mutanty, podczas gdy sole sodu lub wapnia tego nie robiły. Pokazało to, że problem nie był ogólnym „stresem solnym”, lecz specyficzną niezdolnością do radzenia sobie z utratą potasu.
Szlak stresowy włączający geny przeżyciowe
Aby zrozumieć, jak p38 pomaga robakom znosić niedobór potasu, zespół rozłożył na części cały łańcuch białek w tym szlaku — od czujnika nadrzędnego (TIR‑1) przez kaskadę kinaz (NSY‑1, SEK‑1, PMK‑1) aż po czynnik transkrypcyjny ATF‑7, który kontroluje aktywność genów. Gdy którakolwiek z tych części była unieszkodliwiona, robaki szybko ginęły przy deficycie potasu, mimo że wiele innych dobrze znanych genów związanych z długowiecznością i stresem okazywało się mniej krytycznych. Badania genetyczne wskazały ATF‑7 jako centralnego gracza: gdy ATF‑7 utknął w formie „represora”, przeżywalność była jeszcze gorsza, co sugeruje, że p38 musi modyfikować ATF‑7, by włączyć konkretne geny ochronne i zdjąć szkodliwą represję podczas stresu potasowego.
Pompa potasowa w warstwie przypominającej skórę
Porównując aktywność genów u robaków w normalnych, wysokopotasowych i niskopotasowych warunkach, autorzy znaleźli setki genów włączanych wyłącznie przy niedoborze potasu. Wiele z nich to typowe geny odpornościowe i odpowiedzi na stres, ale jeden wyróżniał się szczególnie: pompa P‑typowa ATPaza nazwana CATP‑3, wyspecjalizowana w transporcie potasu przez błony. Robaki pozbawione CATP‑3 przypominały mutanta p38 przy deficycie: miały skurcze mięśni, kurczenie ciała i pękające tkanki wewnętrzne, a przy spadku zewnętrznego potasu poniżej kilku milimoli ginęły szybko. Dzięki znacznikom fluorescencyjnym zespół wykazał, że CATP‑3 jest głównie produkowany w hipodermie — zewnętrznej, skóropodobnej warstwie komórek, która otacza mięśnie i narządy wewnętrzne. Przywrócenie CATP‑3 tylko w tej warstwie wystarczyło, by uratować przeżycie, natomiast ekspresja w mięśniach lub niektórych neuronach tego nie czyniła, co sugeruje, że hipoderma działa jako kluczowa brama dla pobierania potasu do całego ciała.
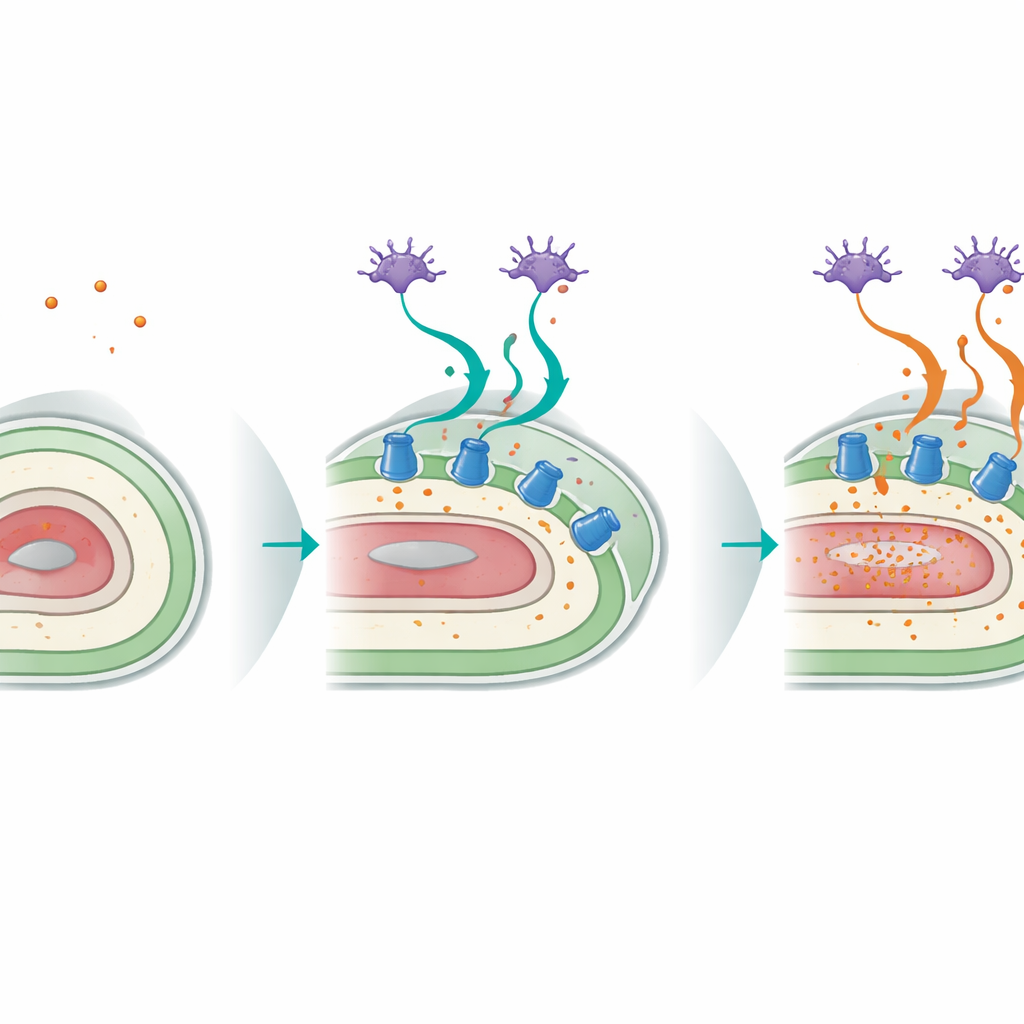
Dialog między neuronami czuciowymi a powierzchnią ciała
Badanie ujawniło również uderzający dialog między neuronami sensorycznymi robaka a jego hipodermą. Specjalne neurony głowy znane jako ASI, które zwykle wykrywają pokarm i inne sygnały środowiskowe, polegają na sygnalizacji p38, by pomóc zorganizować odpowiedź na utratę potasu. Gdy p38 przywrócono jedynie w neuronach ASI u mutantów, przeżywalność przy niskim potasie poprawiła się znacząco, a kluczowa pompa CATP‑3 w hipodermie została ponownie włączona. Eksperymenty z uciszaniem genów w konkretnych tkankach wykazały, że funkcja p38 w neuronach i w hipodermie jest zarówno niezbędna, jak i współzależna: neurony wykrywają zagrożenie związane z niedoborem, podczas gdy tkanka skórnopodobna realizuje program ochronny przez zwiększenie liczby pomp potasowych. Ten międzytkankowy obwód staje się mniej skuteczny z wiekiem, ponieważ ekspresja CATP‑3 i jej indukcja przez niedobór potasu maleją.
Zachowana strategia od nicieni po mięśnie i drożdże
Aby sprawdzić, czy ta logika wykracza poza nicienie, autorzy zwrócili się do komórek mięśni mysich i drożdży pączkujących. W hodowlach myoblastów mysich aktywność p38 i obecność potasu były konieczne, aby komórki dojrzały do kurczących się włókien mięśniowych. Podczas różnicowania geny zależne od p38 obejmowały specyficzne podjednostki pompy Na⁺/K⁺, takie jak Atp1a2, które pomagają utrzymać gradienty jonowe w tkankach pobudliwych. U drożdży kinaza podobna do p38 — Hog1 — i czynnik transkrypcyjny Sko1 regulowały geny ATPaz typu P (rodzina ENA) zarządzające eksportem sodu i potasu oraz wpływały na rozmiar komórek w zmieniających się warunkach solnych. W tych systemach wyłonił się wspólny motyw: szlak stresowy typu p38 dopasowuje produkcję energochłonnych pomp jonowych, aby ustabilizować równowagę potasową, gdy warunki ulegają zmianie.
Co to oznacza dla zdrowia i starzenia się
Mówiąc prosto, praca ta pokazuje, że równowagę potasu strzeże ogólnoustrojowa sieć wczesnego ostrzegania, a nie izolowane komórki biernie tracące jony. Czujnik stresu (p38) nasłuchuje sygnałów od neuronów odbierających bodźce środowiskowe, a następnie nakazuje barierze przypominającej skórę zainstalowanie większej liczby molekularnych „pomp”, które wtłaczają potas z powrotem do organizmu, chroniąc mięśnie i nerwy przed niewydolnością w czasie niedoborów. Podobne mechanizmy wydają się działać w mięśniach ssaków i u drożdży, a ich wydajność słabnie z wiekiem. Zrozumienie, jak ten obwód zawodzi lub jak można go pobudzić, może w przyszłości pomóc w opracowaniu strategii leczenia hipokaliemii, zaniku mięśni i związanych z wiekiem spadków funkcji u ludzi.
Cytowanie: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Słowa kluczowe: homeostaza potasu, p38 MAPK, Caenorhabditis elegans, pompy jonowe, starzenie się