Clear Sky Science · it
p38 MAPK orchestra l'omeostasi del potassio tra i tessuti per la sopravvivenza
Perché questo è importante per la salute quotidiana
Il potassio è un minerale semplice che trovi indicato sulle etichette degli alimenti, eppure la sua carenza nell’organismo può scatenare crampi muscolari, problemi cardiaci e perfino risultare pericolosa per la vita. Questo studio mostra che gli animali non affrontano la carenza di potassio cellula per cellula. Piuttosto, utilizzano un sistema di allarme e risposta a livello dell’intero organismo, coordinato da una via di segnalazione sensibile allo stress chiamata p38, per mantenere l’equilibrio del potassio e preservare la sopravvivenza. Poiché parte di questo sistema è conservata da piccoli vermi fino ai mammiferi, lo studio suggerisce nuove prospettive per comprendere i disturbi umani legati all’ipokaliemia e all’invecchiamento.
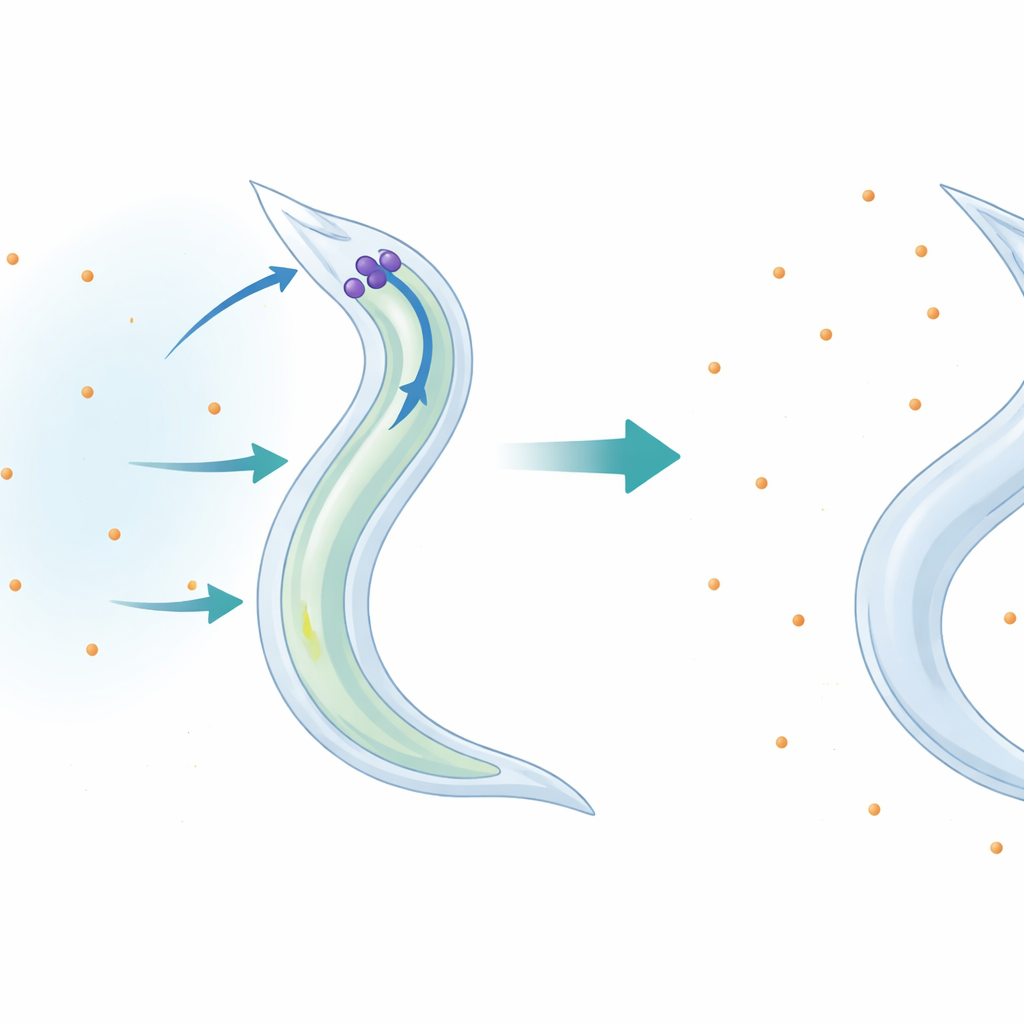
Un minuscolo verme come finestra sull’equilibrio del potassio
I ricercatori hanno impiegato il microscopico verme Caenorhabditis elegans come banco di prova vivo per esplorare cosa accade quando l’apporto dietetico di potassio diminuisce. Hanno posto vermi adulti in soluzioni liquide controllate che erano prive di potassio oppure ne contenevano quantità differenziate, mantenendo costanti altri sali e condizioni. I vermi con una via di segnalazione p38 funzionante sopravvissero molto più a lungo in condizioni povere di potassio rispetto ai vermi mutanti privi di componenti chiave della p38. L’aggiunta di cloruro di potassio salvava i mutanti fragili, mentre sali di sodio o di calcio non erano efficaci. Ciò dimostrò che il problema non era un generico “stress da sali”, ma un’incapacità specifica di fronteggiare la perdita di potassio.
Una via di stress che attiva geni protettivi
Per capire come p38 aiuti i vermi a resistere alla scarsità di potassio, il gruppo ha analizzato l’intera catena proteica di questa via, da un sensore a monte (TIR-1) attraverso una cascata di chinasi (NSY-1, SEK-1, PMK-1) fino a un fattore di trascrizione chiamato ATF-7, che regola l’attività genica. Quando una qualsiasi di queste componenti veniva disattivata, i vermi morivano rapidamente sotto carenza di potassio, nonostante molti altri noti geni di longevità e risposta allo stress fossero molto meno critici. Screening genetici identificarono ATF-7 come un attore centrale: quando ATF-7 era bloccato nella sua forma “repressiva”, la sopravvivenza peggiorava ulteriormente, indicando che p38 deve modificare ATF-7 per attivare specifici geni protettivi e disattivare repressioni dannose durante lo stress da potassio.
Una pompa di potassio nello strato simile alla pelle
Confrontando l’attività genica nei vermi in condizioni normali, ad alto contenuto di potassio e a basso contenuto di potassio, gli autori hanno trovato centinaia di geni che si attivavano solo quando il potassio era scarso. Molti di questi erano tipici geni di risposta immunitaria e allo stress, ma uno spiccava: una ATPasi di tipo P chiamata CATP-3, specializzata nel trasporto del potassio attraverso le membrane. I vermi privi di CATP-3 assomigliavano molto ai mutanti p38 sotto carenza: sviluppavano spasmi muscolari, restringimento del corpo e rottura di tessuti interni, e morivano rapidamente quando il potassio esterno scendeva sotto pochi millimoli. Mediante tag fluorescenti, il gruppo dimostrò che CATP-3 è prodotto principalmente nell’ipoderma — lo strato esterno di cellule simile alla pelle che avvolge muscoli e organi interni del verme. Ripristinare CATP-3 solo in questo strato era sufficiente a salvare la sopravvivenza, mentre la sua espressione nei muscoli o in certi neuroni non lo era, suggerendo che l’ipoderma agisca come un passaggio chiave per l’assorbimento del potassio nell’intero organismo.
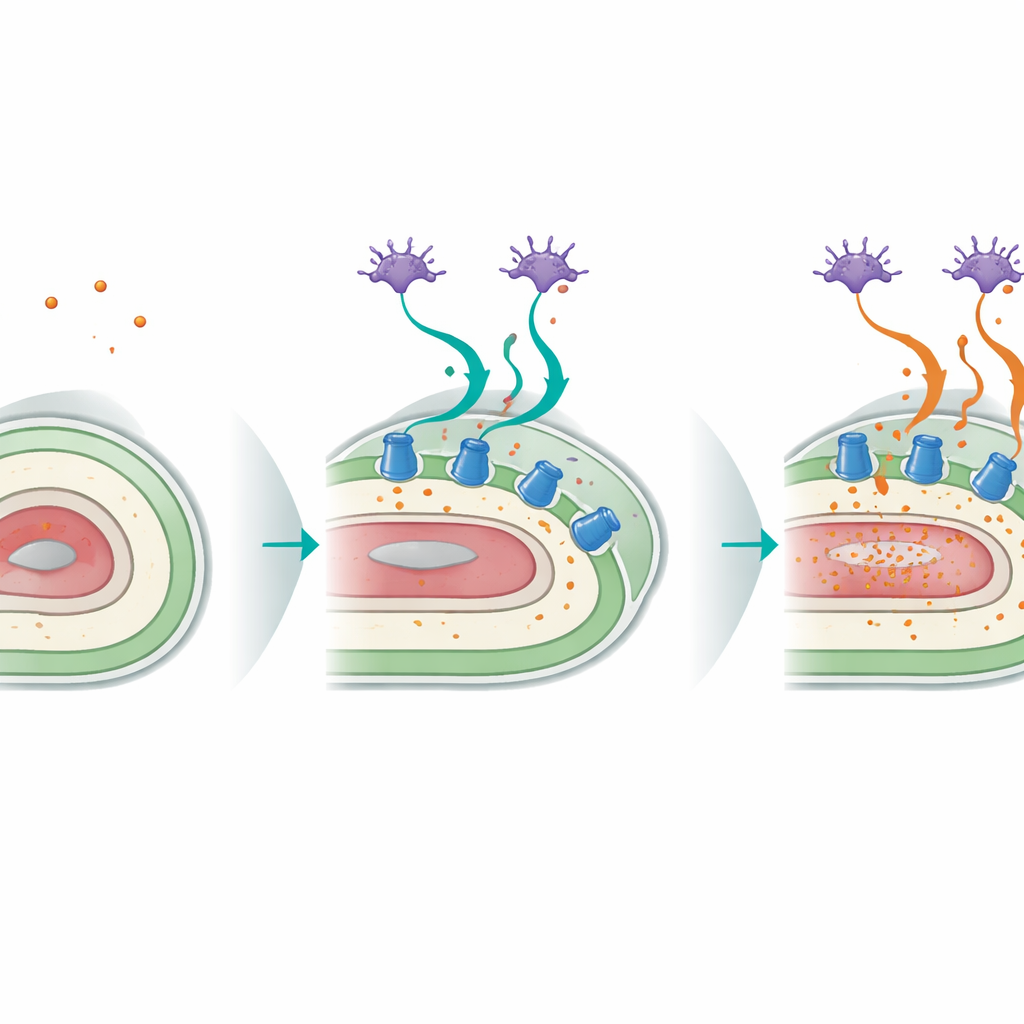
Dialogo tra neuroni sensoriali e superficie corporea
Lo studio ha inoltre rivelato un notevole dialogo tra i neuroni sensoriali del verme e il suo ipoderma. Neuroni speciali nella testa, noti come ASI, che normalmente rilevano cibo e altri segnali ambientali, si affidano alla segnalazione p38 per orchestrare la risposta alla perdita di potassio. Quando p38 veniva ripristinata solo nei neuroni ASI di vermi altrimenti mutanti, la sopravvivenza sotto basso potassio migliorava marcatamente e la cruciale pompa CATP-3 nell’ipoderma veniva riindotta. Esperimenti di silenziamento genico tessuto-specifico dimostrarono che la funzione di p38 nei neuroni e nell’ipoderma è sia necessaria sia interconnessa: i neuroni percepiscono la minaccia nutritiva, mentre il tessuto simile alla pelle esegue il programma protettivo aumentando le pompe del potassio. Questo circuito inter-tessuti diventa meno efficace con l’età, poiché l’espressione di CATP-3 e la sua induzione da carenza di potassio diminuiscono.
Una strategia conservata dai vermi ai muscoli e ai lieviti
Per verificare se questa logica si estende oltre i vermi, gli autori si sono rivolti a cellule muscolari di topo e al lievito. In mioblasti murini in coltura, l’attività di p38 e il potassio erano entrambi necessari perché le cellule maturassero in fibre muscolari contrattili. Durante la differenziazione, i geni dipendenti da p38 includevano subunità specifiche della pompa Na⁺/K⁺, come Atp1a2, che contribuiscono a mantenere i gradienti ionici nei tessuti eccitabili. Nel lievito, la chinasi simile a p38 Hog1 e il fattore di trascrizione Sko1 regolavano geni di ATPasi di tipo P (famiglia ENA) che gestiscono l’esportazione di sodio e potassio e influenzavano la dimensione cellulare in condizioni saline variabili. In questi sistemi emerse un tema conservato: una via di stress di tipo p38 modula la produzione di pompe ioniche energivore per stabilizzare l’equilibrio del potassio quando le condizioni cambiano.
Cosa significa per la salute e l’invecchiamento
In termini accessibili, questo lavoro mostra che l’equilibrio del potassio è custodito da una rete d’allerta precoce a livello corporeo, piuttosto che da singole cellule che lasciano passivamente fuoriuscire ioni. Un sensore di stress (p38) ascolta i segnali provenienti dai neuroni che percepiscono l’ambiente e poi ordina alla barriera simile alla pelle di installare più “pompe” molecolari che richiamano il potassio dentro l’organismo, evitando il cedimento di muscoli e nervi durante le carenze. Sistemi di controllo simili sembrano operare nei muscoli dei mammiferi e nei lieviti, e si indeboliscono con l’età. Capire come questo circuito fallisca o come possa essere rivitalizzato potrebbe, in futuro, aiutare a elaborare strategie per gestire l’ipokaliemia, la perdita muscolare e il declino legato all’età negli esseri umani.
Citazione: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
Parole chiave: omeostasi del potassio, p38 MAPK, Caenorhabditis elegans, pompe ioniche, invecchiamento