Clear Sky Science · ar
تنسق MAPK p38 توازن البوتاسيوم عبر الأنسجة للبقاء على قيد الحياة
لماذا يهم هذا للصحة اليومية
البوتاسيوم هو معدن بسيط تراه مدرجًا على ملصقات الطعام، ومع ذلك فإن نقصه في الجسم يمكن أن يسبب تشنجات عضلية ومشاكل قلبية وقد يكون مهددًا للحياة. تكشف هذه الدراسة أن الحيوانات لا تتعامل مع نقص البوتاسيوم خلية بخلية. بل تستخدم نظام إنذار واستجابة على مستوى الجسم، تنسقه مسار استشعار الإجهاد المسمى p38، للحفاظ على توازن البوتاسيوم وضمان البقاء. وبما أن جزءًا من هذا النظام محفوظ تطوريًا من الديدان الصغيرة حتى الثدييات، فإنه يشير إلى طرق جديدة لفهم اضطرابات البشر المرتبطة بنقص البوتاسيوم والشيخوخة.
دودة صغيرة كنافذة على توازن البوتاسيوم
استخدم الباحثون الدودة المجهرية Caenorhabditis elegans كنموذج حي لاستكشاف ما يحدث عند ضعف إمداد البوتاسيوم الغذائي. وضعوا ديدان البالغين في محاليل سائلة مراقبة بعناية تفتقر إما إلى البوتاسيوم أو تحتوي على كميات مختلفة منه، مع إبقاء الأملاح والظروف الأخرى ثابتة. نجت الديدان التي تمتلك مسار إشارة p38 وظيفيًا لفترات أطول بكثير في ظروف الفقر البوتاسيومي مقارنةً بالديدان الطافرة التي تفتقد مكونات p38 الأساسية. إن إضافة كلوريد البوتاسيوم أنقذت الطفرات الضعيفة، بينما لم تستطع أملاح الصوديوم أو الكالسيوم ذلك. هذا أوضح أن المشكلة ليست «إجهاد مَلحي» عام بل عجز محدد عن التعامل مع فقدان البوتاسيوم.
مسار إجهاد يشغّل جينات النجاة
لفهم كيف يساعد p38 الديدان على تحمل ندرة البوتاسيوم، حلّل الفريق سلسلة البروتينات في هذا المسار كاملةً، من جهاز استشعاري علوي (TIR-1) عبر الشلال الكينازي (NSY-1، SEK-1، PMK-1) وصولًا إلى عامل النسخ المسمى ATF-7 الذي يتحكم في نشاط الجينات. عندما تعطلت أي من هذه المكونات، ماتت الديدان بسرعة تحت نقص البوتاسيوم، رغم أن العديد من جينات طول العمر والإجهاد المعروفة الأخرى كانت أقل أهمية بكثير. حددت الفحوصات الجينية ATF-7 كلاعب مركزي: عندما اُغلِق ATF-7 في صورته «القامعة»، كانت النجاة أسوأ، مما يشير إلى أن p38 يجب أن يعدل ATF-7 ليشغّل جينات وقائية محددة ويوقف القمع الضار أثناء إجهاد البوتاسيوم.
مضخة بوتاسيوم في الطبقة الشبيهة بالجلد
من خلال مقارنة نشاط الجينات في الديدان تحت ظروف طبيعية، وارتفاع البوتاسيوم، ونقصه، وجد المؤلفون مئات الجينات التي تشتغل فقط عندما يكون البوتاسيوم نادرًا. كان العديد منها من جينات الاستجابة المناعية والجهازية للإجهاد، لكن أحدها تميّز: مضخة من نوع P-ATPase تسمى CATP-3، متخصصة في نقل البوتاسيوم عبر الغشاء. بدت الديدان التي تفتقد CATP-3 مشابهة جدًا لطلاب p38 تحت النقص: ظهرت لديها تشنجات عضلية، وانكماش الجسم، وتمزق في الأنسجة الداخلية، وماتت بسرعة عندما انخفض البوتاسيوم الخارجي إلى ما دون عدة ميليمولات. باستخدام وسوم فلورية، برهن الفريق أن CATP-3 يُنتَج بشكل رئيسي في الهيبوديرميس—الطبقة الخارجية الشبيهة بالجلد في الدودة التي تحيط بالعضلات والأعضاء الداخلية. كانت إعادة CATP-3 في هذه الطبقة وحدها كافية لاستعادة النجاة، في حين أن التعبير عنه في العضلات أو بعض الخلايا العصبية لم يكن كذلك، مما يوحي بأن الهيبوديرميس يعمل كبوابة رئيسية لامتصاص البوتاسيوم إلى الجسم بأكمله.
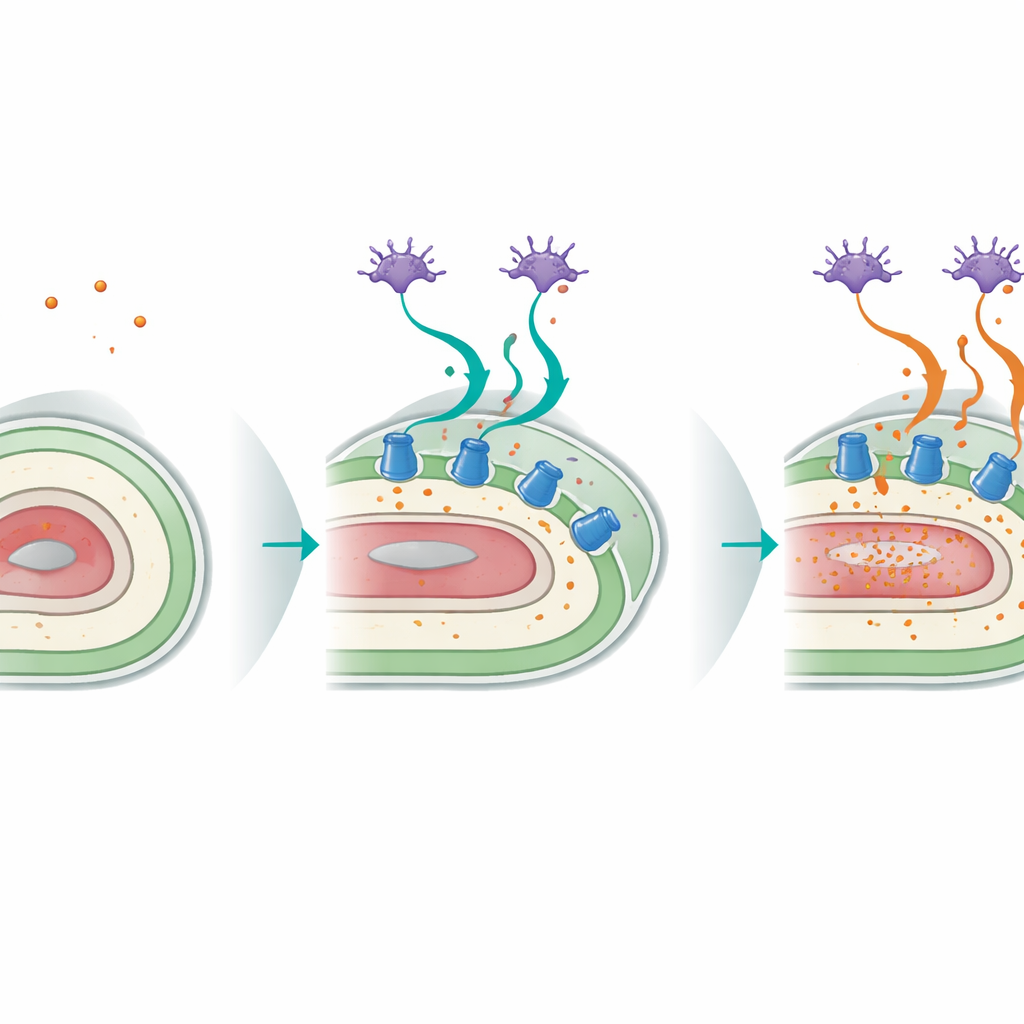
حوار بين الخلايا الحسّية وسطح الجسم
كشفت الدراسة أيضًا عن حوار لافت بين الخلايا العصبية الحسية للدودة وطبقتها الهيبوديرمية. تعتمد خلايا عصبية رأسية خاصة تعرف بـ ASI، والتي تكشف عادة عن الطعام وإشارات بيئية أخرى، على إشارة p38 للمساعدة في تنسيق الاستجابة لفقدان البوتاسيوم. عندما أعيد تشغيل p38 فقط في خلايا ASI العصبية لدى ديدان طافرة خلافًا لذلك، تحسنت النجاة تحت نقص البوتاسيوم بشكل ملحوظ، وأُعيد تحفيز المضخة الحيوية CATP-3 في الهيبوديرميس. أظهرت تجارب إسكات الجينات الخاصة بالنسج أن وظيفة p38 في الخلايا العصبية والهيبوديرميس ضرورية ومترابطة: تكشف الخلايا العصبية عن تهديد المغذيات، بينما تنفّذ الأنسجة الشبيهة بالجلد البرنامج الواقي عبر زيادة مضخات البوتاسيوم. يضعف هذا الدارة العبر‑نسيجية مع التقدم في العمر، حيث يتراجع تعبير CATP-3 وتحفيزه بفعل نقص البوتاسيوم.
استراتيجية محفوظة من الديدان إلى العضلات والخميرة
لاختبار ما إذا كان هذا المنطق يمتد إلى ما بعد الديدان، وجّه المؤلفون تجاربهم إلى خلايا عضلية فأرية وخميرة شعيرية. في خلايا العضلات الفأرية المنزرعة، كانت كل من فعالية p38 ومستوى البوتاسيوم مطلوبة لكي تنضج الخلايا إلى ألياف عضلية قابلة للانقباض. خلال التمايز، شملت الجينات المعتمدة على p38 رُكَبًا محددة من مضخة Na⁺/K⁺، مثل Atp1a2، التي تساعد في الحفاظ على تدرجات الأيونات في الأنسجة القابلة للاستثارة. في الخميرة، نَظّم كيناز شبيه بـ p38 يُدعى Hog1 وعامل النسخ Sko1 جينات مضخات من نوع P-ATPase (عائلة ENA) التي تدير تصدير الصوديوم والبوتاسيوم، وأثّروا على حجم الخلية تحت ظروف ملحية متغيرة. عبر هذه الأنظمة، ظهر نمط محفوظ: مسار إجهاد من نوع p38 يعدل إنتاج مضخات أيونية مستهلكة للطاقة لتثبيت توازن البوتاسيوم عندما تتغير الظروف.
ما الذي يعنيه هذا للصحة والشيخوخة
بعبارات يسهل فهمها، تُظهِر هذه الدراسة أن توازن البوتاسيوم يحرسه شبكة إنذار مبكر على مستوى الجسم، بدلًا من خلايا معزولة تتسرب أيوناتها سلبيًا. يستمع مجس إجهاد (p38) إلى إشارات من خلايا عصبية مستشعِرة بالبيئة ثم يأمر الحاجز الشبيه بالجلد بتركيب مزيد من «المضخات» الجزيئية التي تسحب البوتاسيوم مرة أخرى إلى الجسم، مما يمنع فشل العضلات والأعصاب عند النقص. تبدو أنظمة تحكم مماثلة عاملة في العضلات الثديية وفي الخميرة، وتضعف مع التقدم في العمر. قد يساهم فهم كيف يفشل هذا الدارة أو كيف يُعاد تنشيطها في نهاية المطاف في استراتيجيات لإدارة نقص بوتاسيوم الدم، وهزال العضلات، والتدهور المرتبط بالسن لدى البشر.
الاستشهاد: Huang, R., Hu, F., Li, Y. et al. p38 MAPK orchestrates cross-tissue potassium homeostasis for survival. Nat Commun 17, 3663 (2026). https://doi.org/10.1038/s41467-026-70641-7
الكلمات المفتاحية: توازن البوتاسيوم, MAPK p38, Caenorhabditis elegans, مضخات الأيونات, الشيخوخة