Clear Sky Science · tr
ATP11B‑YAP eksenini hedeflemek mitokondriyal işlevi onarır ve nöronal ferroptozi engelleyerek yaşa bağlı bilişsel gerilemeyi azaltır
Neden Yaşlanma Açısından Önemli
İnsanlar daha uzun yaşadıkça, birçok kişi yıl sayısını artırmaktan çok bu yılları zihinsel olarak keskin tutmaya önem veriyor. Bu çalışma, yaşlanan beynin neden hafıza kaybına ve Alzheimer gibi hastalıklara karşı savunmasız hale geldiğini inceliyor ve beyin hücrelerini yavaş, demir kaynaklı bir hasardan koruyan tek bir moleküler “anahtar” olan ATP11B’yi tanımlıyor. Bu anahtarın yaşla birlikte nasıl işlevini yitirdiğini anlayarak, araştırmacılar yaşa bağlı bilişsel gerilemeyi yavaşlatmaya ya da tersine çevirmeye yönelik olası bir yolu öne sürüyorlar.
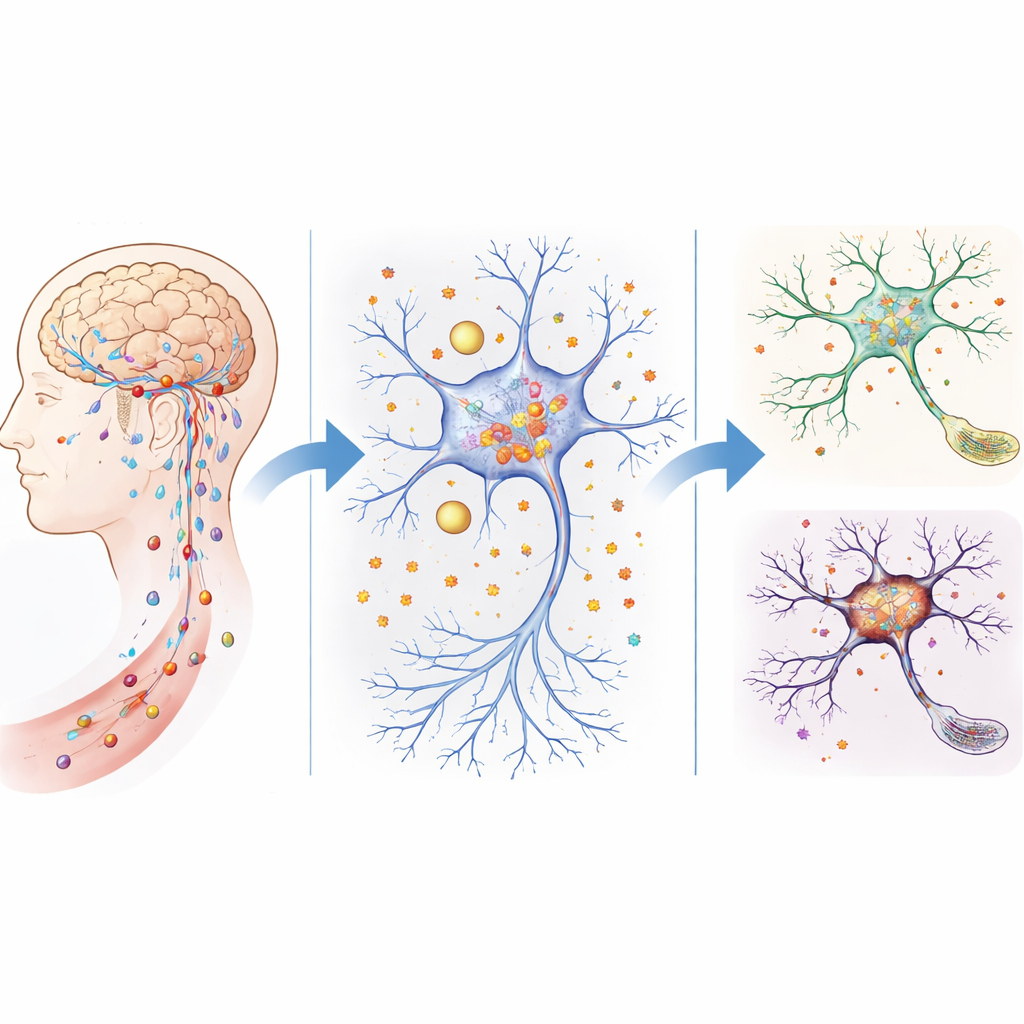
Yaşlanan Beyinde Sızan Savunmalar ve Demir Birikimi
Beyin normalde kan‑beyin bariyeri ve ilgili yapılar gibi sıkı bir filtre sistemiyle korunur; bu sistem kan dolaşımından neyin girdiğini dikkatle kontrol eder. Yaşlı farelerde ve ATP11B geninden yoksun farelerde bu bariyer daha sızdıran hale geliyor. Araştırmacılar, bu farelerin daha fazla küçük molekülün beyin dokusuna sızmasına izin verdiğini ve serbest demir düzeylerinin özellikle öğrenme ve hafıza için kritik olan hipokampusta belirgin şekilde yükseldiğini gösterdiler. Davranış testleri, ATP11B’siz farelerin daha hızlı yaşlandığını, sosyal etkileşimlerinin zayıfladığını, daha az kendinden emin hareket ettiklerini ve labirent ile hafıza görevlerinde daha kötü performans sergilediklerini; bunun insanlardaki yaşa bağlı bilişsel sorunları andırdığını ortaya koydu.
Destek Hücrelerin Demiri Kötü Yönetmesi
Tek hücre dizileme ve mekânsal haritalama kullanarak, araştırmacılar ATP11B kaybından en çok hangi beyin hücrelerinin etkilendiğini incelediler. Beynin sıvı dolu boşluklarını döşeyen ve sıvı ile beyin dokusu arasında besin ve iyon taşınmasına yardımcı olan ependimal hücrelere odaklandılar. ATP11B eksikliğine sahip farelerde ependimal hücre alt tiplerinin dengesi, metal iyon transportunu tercih eden hücrelere doğru kaydı ve bu hücrelerin hipokampusa daha yakın yer değiştirmiş gibi göründüğü gözlendi. Gen analizleri, bu değişikliğin yakınındaki nöronlara anormal demir akışını teşvik ettiğini düşündürdü. Bu bölgelerde demir yönetimi ve hafıza düzenlemesi belirteçleri değişmişti ve hücresel yaşlanmanın erken belirtileri önce ependimal hücrelerde, sonra nöronlarda ortaya çıktı; bu da destek hücrelerden kaynaklanan yanlış yönetilen demirin uzaktan nöron hasarına yol açabileceğini ima ediyor.
Demir, Bozulmuş Enerji Santralleri ve Yakıcı Bir Hücre Ölümü
Nöronların içinde aşırı demir, ferroptoz adı verilen bir zincir tepkisini tetikleyebilir—bu, hücre zarının yağ bileşenlerine yönelik oksidatif hasarla ilerleyen bir hücre ölümü türüdür. Yazarlar, insan kaynaklı sinir hücrelerinde ATP11B’yi baskılamanın serbest demiri artırdığını, demir depolama kapasitesini azalttığını ve ferroptoza ait belirteçleri yükselttiğini gösterdiler. Aynı zamanda hücrelerin mitokondrileri—enerji üreten küçük santraller—yapısal olarak bozuldu, membran potansiyellerini kaybetti ve daha az oksijen tüketti. Hücreler bunu telafi etmeye çalışarak şeker yakımını artırdı ve daha fazla laktat üretti, fakat bunun bedeli zarları daha fazla hasara uğratan reaktif moleküllerin artması oldu. Mitokondriler füzyon yerine parçalandı, temizleme süreçleri aşırı aktifleşti ve hücresel yaşlanma ile artan reaktif oksijen belirtileri ortaya çıktı; bunların hepsi nöronlar arasındaki elektriksel iletişimi zayıflattı.
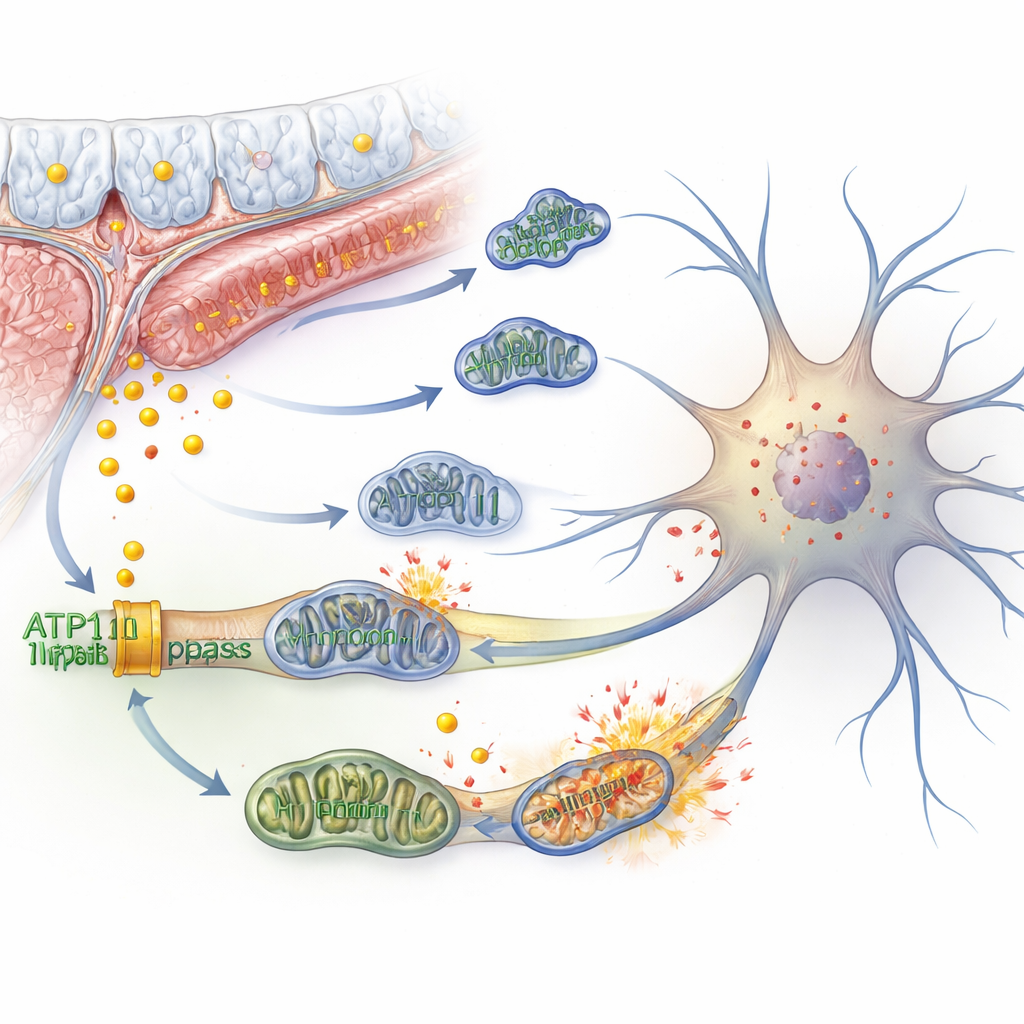
Çekirdekte Bir Moleküler Kontrol Ekseni
Çalışma, ATP11B’nin bu kadar çok aşağı akış olayı nasıl kontrol ettiğini daha derinlemesine sordu. Nöronlarda DNA’nın nasıl paketlendiğini ve okunduğunu inceleyerek, araştırmacılar ATP11B kaybının kromatini—DNA’yı saran maddeyi—belirli bölgelerde daha az erişilebilir hale getirdiğini buldular. Bu özellikle, normalde sağlıklı mitokondri fonksiyon genlerini korumaya yardımcı olan KLF4 adlı bir transkripsiyon faktörünün bağlanma bölgelerini etkiledi. Aynı zamanda Hippo olarak bilinen büyüme‑kontrol yolunun aktivitesi azaldı; bu da YAP adlı bir proteinin çekirdeğe girmesine ve ferroptoz ve yaşlanmayla ilişkili genleri açan bir kompleks oluşturmasına izin verdi. Stres altındaki mitokondrilerden kaynaklanan daha yüksek laktat da histonlar üzerindeki kimyasal işaretlere (histon laktilasyonu) katkıda bulunarak önemli pro‑yaşlanma ve pro‑ferroptoz genlerin ifadesini daha da artırdı. Birlikte, bu çekirdek değişiklikleri nöronları demir stresi ve mitokondriyal çöküşün kendi kendini güçlendiren bir döngüsüne kilitledi.
Anahtarı Yeniden Açmak
Cesaret verici olarak, hasar tamamen geri dönülemez değildi. Araştırmacılar yaşlı farelere viral vektör kullanarak ekstra ATP11B verdiğinde, birçok yaşa bağlı problem iyileşti. Tedavi edilen fareler daha uzun, daha stabil adımlarla yürüdü, dengeyi daha iyi korudu, yeni ortamları daha istekli keşfetti ve hafıza testlerinde anlamlı şekilde daha iyi performans gösterdi. Mikroskop altında nöronları daha uzun dallara ve daha karmaşık dikenlere (spine) sahipti; bunlar daha güçlü sinaptik bağlantılarla ilişkili yapısal özelliklerdir. Moleküler belirteçler demir kaynaklı lipid hasarı ve mitokondriyal stresin azaldığını gösterdi. Basitçe söylemek gerekirse, ATP11B’nin geri verilmesi demir yönetimini ve mitokondri sağlığını yeniden düzenlemeye yardımcı oldu, yaşlanan nöronları ölüme ve bilişsel gerilemeye iten baskıyı hafifletti.
Beyin Sağlığı İçin Ne Anlama Geliyor
Bir okuyucu için bu çalışma, beyin yaşlanmasının bir kısmının hücrelerin demiri, enerji üretimini ve gen kontrolünü nasıl dengelediğinin belirli bir şekilde çökmesine indirgenebileceğini öne sürüyor. ATP11B merkezi bir koordine edici görevi görüyor: kaybolduğunda demir sessizce birikir, beyin hücrelerinin enerji santralleri bozulur ve yıkıcı, paslanma benzeri bir süreç hafıza devrelerini yavaşça aşındırır. Farelerde ATP11B geri verildiğinde bu eğilimlerin çoğu tersine çevrilebiliyor. İnsanlar için güvenli tedavilere dönüştürmek, gen taşıma ve uzun vadeli testlerde büyük ilerlemeler gerektirecek olsa da, çalışma yaşlanan nüfusta düşünmeyi, hafızayı ve bağımsızlığı korumaya yönelik umut vadeden yeni bir hedefi öne çıkarıyor.
Atıf: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Anahtar kelimeler: beyin yaşlanması, demir yüklenmesi, mitokondriyal disfonksiyon, nöronal ferroptoz, bilişsel gerileme