Clear Sky Science · nl
Het richten op de ATP11B‑YAP‑as herstelt mitochondriale functie en remt neuronale ferroptose om leeftijdsgebonden cognitieve achteruitgang te verminderen
Waarom dit ertoe doet bij ouder worden
Nu mensen langer leven, bekommert men zich minder om extra levensjaren en meer om het behoud van mentale scherpte. Deze studie onderzoekt waarom de ouder wordende hersenen kwetsbaar worden voor geheugenverlies en ziekten zoals Alzheimer, en identificeert een enkele moleculaire "schakelaar"—ATP11B—die hersencellen helpt beschermen tegen een langzaam, door ijzer aangedreven type schade. Door te begrijpen hoe deze schakelaar met de leeftijd faalt, schetsen de onderzoekers een mogelijke nieuwe manier om leeftijdsgebonden cognitieve achteruitgang te vertragen of zelfs om te keren.
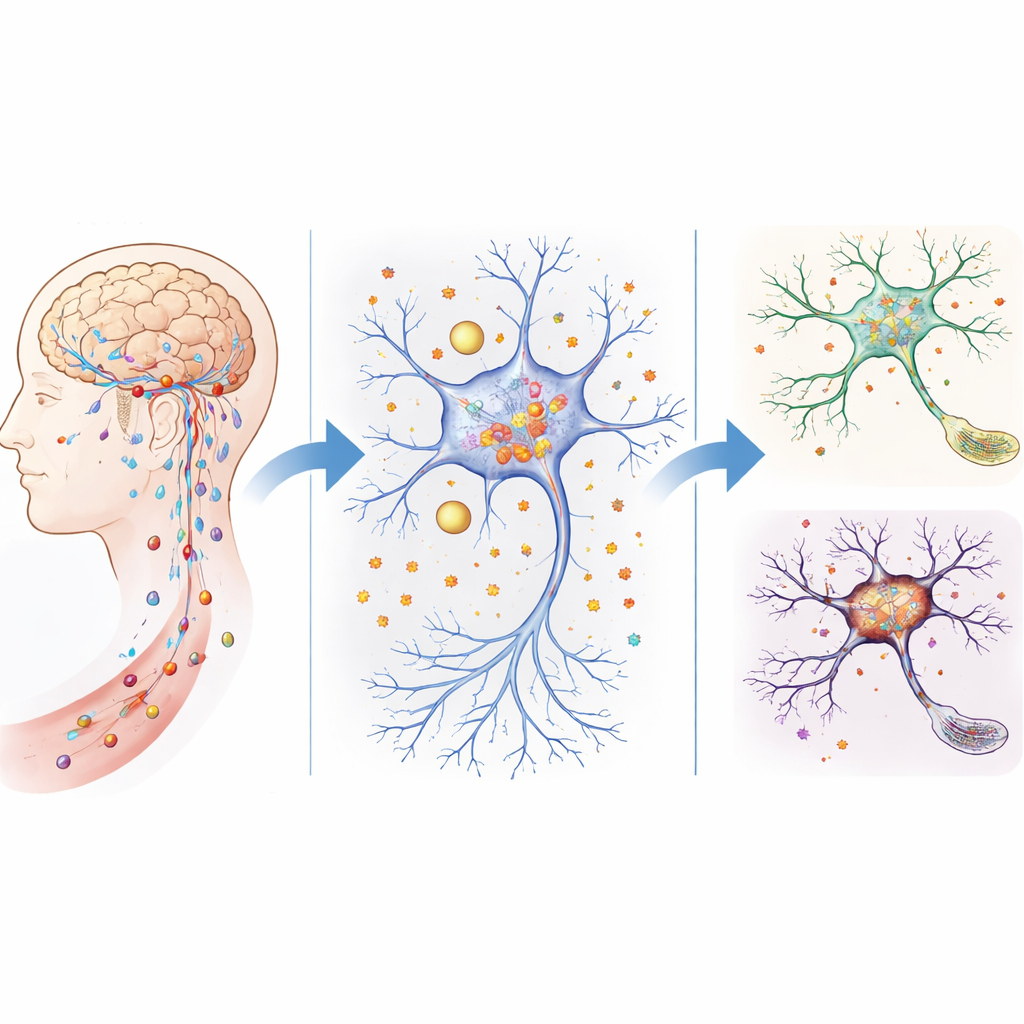
Lekke verdedigingen en ijzerophoping in het verouderende brein
De hersenen worden normaal beschermd door een strak filter systeem—de bloed‑hersenbarrière en verwante structuren—dat zorgvuldig controleert wat uit de bloedbaan binnenkomt. Bij oudere muizen, en bij muizen die genetisch geen ATP11B hebben, wordt deze barrière lekker. Het team toonde aan dat deze muizen meer kleine moleculen in hersenweefsel lieten sijpelen en dat de niveaus van vrij ijzer sterk toenamen in belangrijke regio’s, vooral de hippocampus, die cruciaal is voor leren en geheugen. Gedragstests lieten zien dat muizen zonder ATP11B sneller verouderden, slechtere sociale interactie toonden, minder zeker bewogen en slechter presteerden in doolhof‑ en geheugentaken, wat de leeftijdsgebonden cognitieve problemen bij mensen nabootst.
Hoe ondersteunende cellen slecht met ijzer omgaan
Met enkelcel‑sequencing en ruimtelijke afbakening onderzochten de onderzoekers welke hersencellen het meest getroffen waren door het verlies van ATP11B. Ze concentreerden zich op ependymcellen, die de met vloeistof gevulde ruimten van de hersenen bekleden en helpen bij het verplaatsen van voedingsstoffen en ionen tussen de vloeistof en het hersenweefsel. Bij muizen zonder ATP11B verschoof de balans van ependymcel‑subtypen naar die welke metalen ionentransport bevorderen, en deze cellen leken dichter naar de hippocampus te migreren. Genanalyse wees erop dat deze verandering abnormale ijzerlevering aan nabijgelegen neuronen stimuleerde. Merkers voor ijzerhuishouding en geheugenregulatie in deze regio’s waren veranderd, en vroege tekenen van cellulaire veroudering verschenen eerst in ependymcellen en daarna in neuronen, wat impliceert dat slecht beheerd ijzer vanuit ondersteunende cellen neuronale schade van een afstand kan veroorzaken.
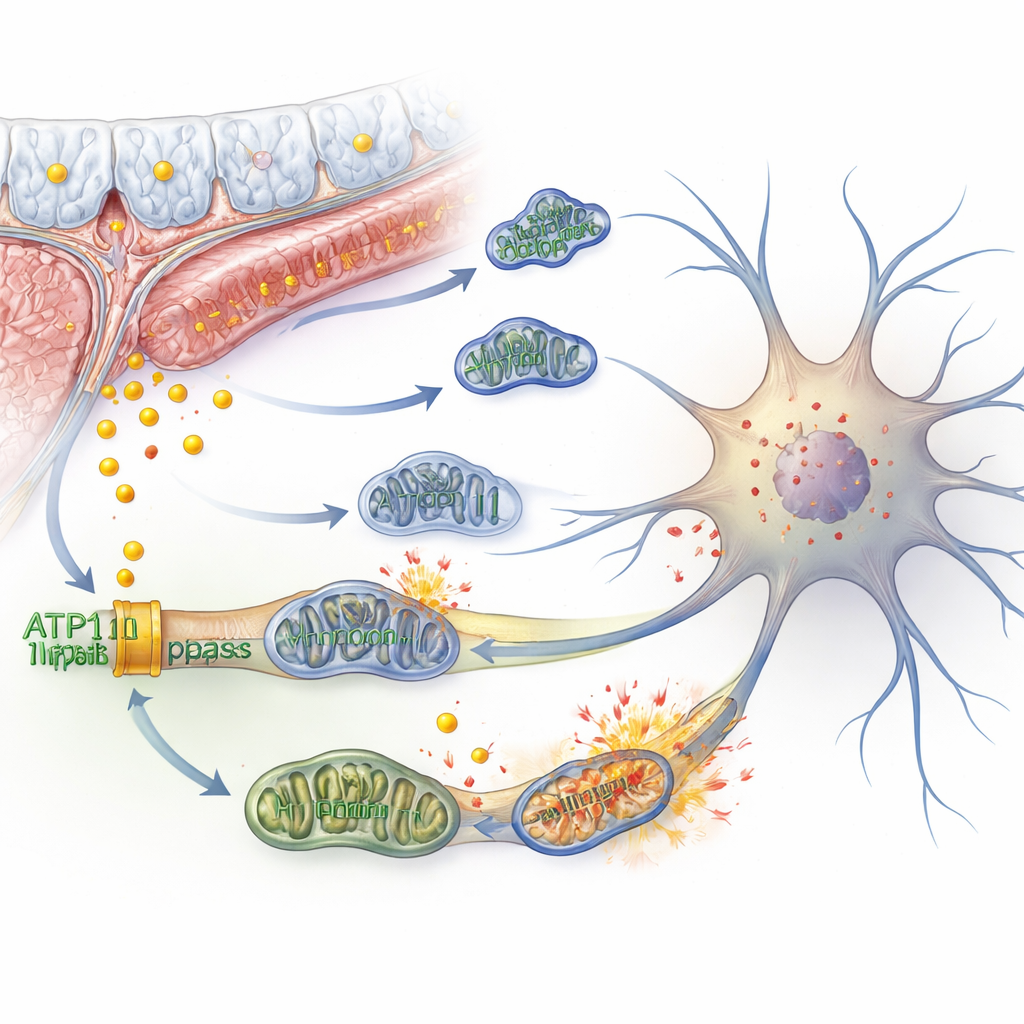
Ijzer, kapotte energiefabriekjes en een vurig celdoodproces
Binnen neuronen kan overtollig ijzer een kettingreactie veroorzaken die ferroptose heet—een vorm van celdood die wordt aangedreven door oxidatieve schade aan vetachtige componenten van het celmembraan. De auteurs toonden aan dat het onderdrukken van ATP11B in door mensen afgeleide zenuwcellen het vrije ijzer verhoogde, de ijzeropslagcapaciteit verlaagde en merkers van ferroptose versterkte. Tegelijkertijd werden de mitochondriën—de kleine energiefabriekjes die energie genereren—structureel vervormd, verloren ze hun membraanpotentiaal en verbruikten ze minder zuurstof. De cellen probeerden te compenseren door de suikerverbranding op te voeren en meer lactaat te produceren, maar dit ging gepaard met meer reactieve moleculen die membranen verder beschadigden. Mitochondriën fragmenteerden in plaats van te fuseren, opruimprocessen werden overactief en er verschenen tekenen van cellulaire veroudering en stijgende reactieve zuurstofniveaus, wat allemaal bijdroeg aan zwakkere elektrische signalering tussen neuronen.
Een moleculaire regelas in de kern
De studie ging dieper om te vragen hoe ATP11B zo veel downstream‑gebeurtenissen reguleert. Door te onderzoeken hoe DNA in neuronen wordt verpakt en afgelezen, vond het team dat verlies van ATP11B de toegankelijkheid van chromatine—het materiaal dat DNA omwikkelt—op specifieke locaties vermindert. Dit trof vooral bindingsplaatsen voor een transcriptiefactor genaamd KLF4, die normaal gesproken genen helpt te behouden die nodig zijn voor gezonde mitochondriale functie. Tegelijkertijd werd een groeiregulatiepad bekend als Hippo minder actief, waardoor een eiwit genaamd YAP de kern in kon bewegen en een complex vormde dat genen aktiveert die verband houden met ferroptose en veroudering. Hogere lactaatniveaus door gestreste mitochondriën voerden ook in chemische tags op histonen (histonlactylatie), wat de expressie van belangrijke pro‑veroudering en pro‑ferroptose genen verder versterkte. Samen verankerden deze kernveranderingen neuronen in een zichzelf versterkende cyclus van ijzerstress en mitochondriale uitval.
De schakelaar weer aanzetten
Hopelijk was de schade niet volledig onomkeerbaar. Toen de onderzoekers extra ATP11B toedienden aan oudere muizen met een viraal vector, verbeterden veel leeftijdsachtige problemen. Behandelde muizen liepen met langere, stabielere stappen, behielden beter hun evenwicht, verkenden nieuwe omgevingen makkelijker en presteerden significant beter in geheugentests. Onder de microscoop toonden hun neuronen langere takken en complexere spine‑structuren, kenmerken die gekoppeld zijn aan sterkere synaptische verbindingen. Moleculaire merkers wezen erop dat door ijzer veroorzaakte lipidedaad en mitochondriale stress waren verminderd. In eenvoudige bewoordingen hielp het herstel van ATP11B de ijzerhuishouding en mitochondriale gezondheid te resetten, waardoor de druk die verouderende neuronen richting celdood en cognitieve achteruitgang duwt, werd verminderd.
Wat dit betekent voor hersengezondheid
Voor een leek suggereert dit werk dat een deel van hersenveroudering mogelijk samen te vatten is als een specifieke storing in hoe cellen ijzer, energieproductie en gencontrole in balans houden. ATP11B fungeert als een centrale coördinator: wanneer het verloren gaat, hoopt ijzer zich stilletjes op, falen de energiefabriekjes van hersencellen en knaagt een destructief, roestachtig proces langzaam aan geheugenkringen. Wanneer ATP11B wordt hersteld, althans bij muizen, kunnen veel van deze trends worden omgekeerd. Het omzetten van dit inzicht in veilige therapieën voor mensen vergt wel grote vooruitgang in genafgifte en langdurige testen, maar de studie benadrukt een veelbelovend nieuw doelwit om denken, geheugen en zelfstandigheid bij een verouderende bevolking te behouden.
Bronvermelding: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Trefwoorden: hersenveroudering, ijzerstapeling, mitochondriale disfunctie, neurale ferroptose, cognitieve achteruitgang