Clear Sky Science · fr
La modulation de l’axe ATP11B–YAP répare la fonction mitochondriale et inhibe la ferroptose neuronale pour atténuer le déclin cognitif lié à l’âge
Pourquoi c’est important en vieillissant
À mesure que l’espérance de vie augmente, beaucoup se préoccupent moins d’ajouter des années à la vie que de conserver des capacités mentales intactes. Cette étude examine pourquoi le cerveau vieillissant devient vulnérable aux pertes de mémoire et à des maladies comme la maladie d’Alzheimer, et identifie un « interrupteur » moléculaire unique — nommé ATP11B — qui contribue à protéger les cellules cérébrales d’un type de dommage lent et alimenté par le fer. En comprenant comment cet interrupteur échoue avec l’âge, les chercheurs décrivent une voie potentielle pour ralentir, voire inverser, le déclin cognitif lié à l’âge.
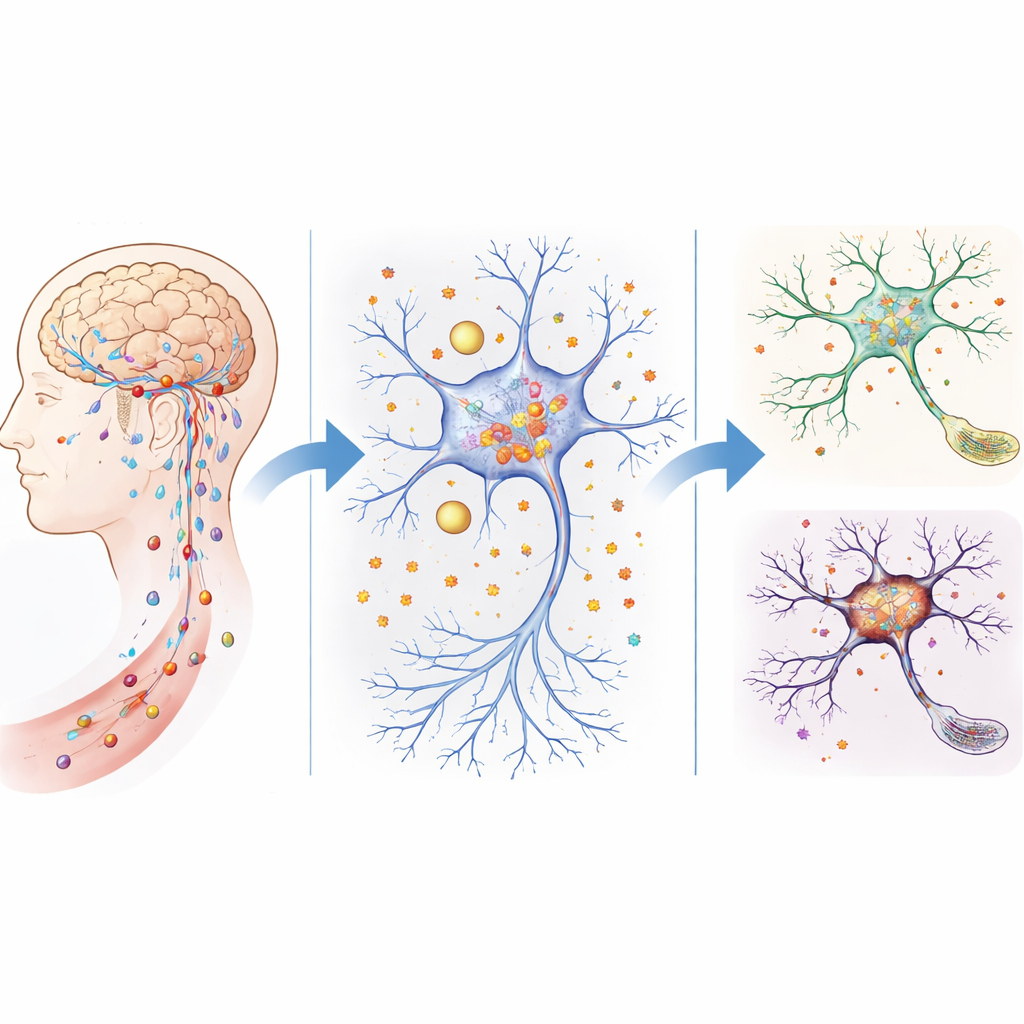
Des défenses poreuses et une accumulation de fer dans le cerveau vieillissant
Le cerveau est normalement protégé par un système de filtrage serré — la barrière hémato‑encéphalique et structures associées — qui contrôle soigneusement ce qui entre depuis la circulation sanguine. Chez des souris âgées, et chez des souris dépourvues d’ATP11B, cette barrière devient plus perméable. L’équipe a montré que ces souris laissaient davantage de petites molécules s’infiltrer dans le tissu cérébral, et les niveaux de fer libre augmentaient fortement dans des régions clés, en particulier l’hippocampe, essentiel pour l’apprentissage et la mémoire. Des tests comportementaux ont révélé que les souris sans ATP11B vieillissaient plus vite, présentaient une interaction sociale altérée, se déplaçaient avec moins d’assurance et obtenaient de moins bons résultats dans les labyrinthes et tâches mnésiques, reproduisant des problèmes cognitifs liés à l’âge chez l’humain.
Comment les cellules de soutien mal gèrent le fer
En utilisant le séquençage unicellulaire et la cartographie spatiale, les chercheurs ont examiné quelles cellules cérébrales étaient le plus affectées par la perte d’ATP11B. Ils se sont concentrés sur les cellules épendymaires, qui tapissent les cavités remplies de liquide du cerveau et aident à transporter nutriments et ions entre le liquide et le tissu cérébral. Chez les souris déficientes en ATP11B, l’équilibre des sous‑types de cellules épendymaires bascula vers celles favorisant le transport d’ions métalliques, et ces cellules semblaient migrer plus près de l’hippocampe. Les analyses génétiques suggéraient que ce changement favorisait une livraison anormale de fer aux neurones voisins. Les marqueurs de gestion du fer et de régulation de la mémoire dans ces régions étaient modifiés, et les premiers signes de vieillissement cellulaire apparurent d’abord dans les cellules épendymaires puis dans les neurones, ce qui laisse penser que le mauvais traitement du fer par les cellules de soutien peut endommager les neurones à distance.
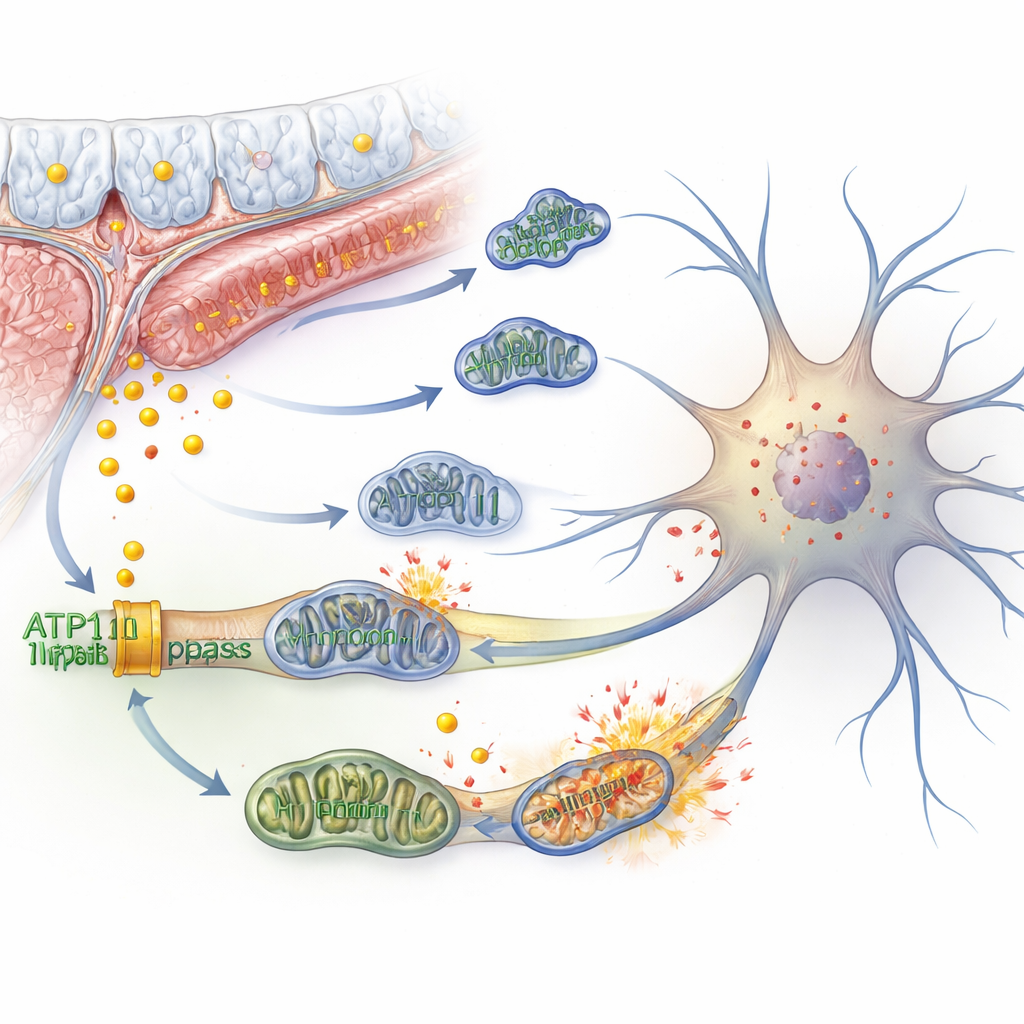
Fer, centrales électriques dégradées et une mort cellulaire enflammée
À l’intérieur des neurones, un excès de fer peut déclencher une réaction en chaîne appelée ferroptose — un type de mort cellulaire provoqué par des dommages oxydatifs aux composants lipidiques de la membrane. Les auteurs ont montré que l’inhibition d’ATP11B dans des cellules nerveuses d’origine humaine augmentait le fer libre, réduisait la capacité de stockage du fer et renforçait les marqueurs de la ferroptose. Parallèlement, les mitochondries des cellules — ces petites centrales qui génèrent l’énergie — se déformaient structurellement, perdaient leur potentiel de membrane et consommaient moins d’oxygène. Les cellules tentèrent de compenser en augmentant l’utilisation du sucre et la production de lactate, mais cela s’accompagna de plus de molécules réactives qui endommagèrent davantage les membranes. Les mitochondries se fragmentèrent au lieu de fusionner, les processus de nettoyage furent suractivés, et des signes de vieillissement cellulaire et d’augmentation des espèces réactives apparaissaient, contribuant à un affaiblissement de la transmission électrique entre neurones.
Un axe de contrôle moléculaire dans le noyau
L’étude est allée plus loin pour comprendre comment ATP11B contrôle tant d’événements en aval. En examinant la façon dont l’ADN est emballé et lu dans les neurones, l’équipe a constaté que la perte d’ATP11B rend la chromatine — le matériel qui enroule l’ADN — moins accessible à des sites spécifiques. Cela affectait particulièrement des régions de liaison pour un facteur de transcription appelé KLF4, qui aide normalement à maintenir des gènes favorables à la fonction mitochondriale saine. Parallèlement, une voie de contrôle de la croissance connue sous le nom de Hippo devenait moins active, permettant à une protéine nommée YAP de se déplacer dans le noyau et de former un complexe qui active des gènes liés à la ferroptose et au vieillissement. L’augmentation du lactate provenant de mitochondries stressées contribuait aussi à des marques chimiques sur les histones (lactylation des histones), renforçant encore l’expression de gènes clés pro‑vieillissement et pro‑ferroptose. Ensemble, ces modifications nucléaires enfermaient les neurones dans un cercle auto‑renforçant de stress ferreux et d’échec mitochondrial.
Rétablir l’interrupteur
De façon encourageante, les dégâts n’étaient pas entièrement irréversibles. Lorsque les chercheurs ont délivré un supplément d’ATP11B à de vieilles souris au moyen d’un vecteur viral, de nombreux problèmes liés à l’âge se sont améliorés. Les souris traitées marchaient avec des enjambées plus longues et plus stables, gardaient mieux l’équilibre, exploraient plus volontiers de nouveaux environnements et obtenaient des performances nettement supérieures aux tests de mémoire. Au microscope, leurs neurones montraient des branches plus longues et des épines plus complexes, des caractéristiques structurelles associées à des connexions synaptiques plus robustes. Les marqueurs moléculaires indiquaient que les dommages lipidiques induits par le fer et le stress mitochondrial étaient réduits. En termes simples, la restauration d’ATP11B permit de rééquilibrer la gestion du fer et la santé mitochondriale, diminuant la pression qui pousse les neurones vieillissants vers la mort et le déclin cognitif.
Ce que cela signifie pour la santé cérébrale
Pour un non‑spécialiste, ce travail suggère qu’une partie du vieillissement cérébral peut se résumer à une défaillance spécifique dans la façon dont les cellules gèrent le fer, la production d’énergie et le contrôle génétique. ATP11B agit comme un coordinateur central : lorsqu’il est perdu, le fer s’accumule discrètement, les centrales des cellules s’affaiblissent et un processus destructeur, semblable à la rouille, érode lentement les circuits de la mémoire. Lorsque l’ATP11B est restauré, du moins chez la souris, beaucoup de ces tendances peuvent être inversées. Transformer cette découverte en thérapies sûres pour l’humain exigera des avancées majeures en délivrance génique et des tests à long terme, mais l’étude met en lumière une nouvelle cible prometteuse pour préserver les capacités de réflexion, la mémoire et l’autonomie dans une population vieillissante.
Citation: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Mots-clés: vieillissement cérébral, surcharge en fer, dysfonction mitochondriale, ferroptose neuronale, déclin cognitif