Clear Sky Science · pt
Direcionar o eixo ATP11B-YAP repara a função mitocondrial e inibe a ferroptose neuronal para atenuar o declínio cognitivo relacionado à idade
Por que isso importa ao envelhecer
À medida que as pessoas vivem mais, muitos se preocupam menos em acrescentar anos à vida e mais em manter essas décadas com a mente afiada. Este estudo investiga por que o cérebro envelhecido se torna vulnerável à perda de memória e a doenças como Alzheimer, e identifica um único “interruptor” molecular — chamado ATP11B — que ajuda a proteger as células cerebrais de uma forma lenta de dano impulsionada pelo ferro. Ao entender como esse interruptor falha com a idade, os pesquisadores delineiam uma possível nova maneira de retardar ou até reverter o declínio cognitivo relacionado à idade.
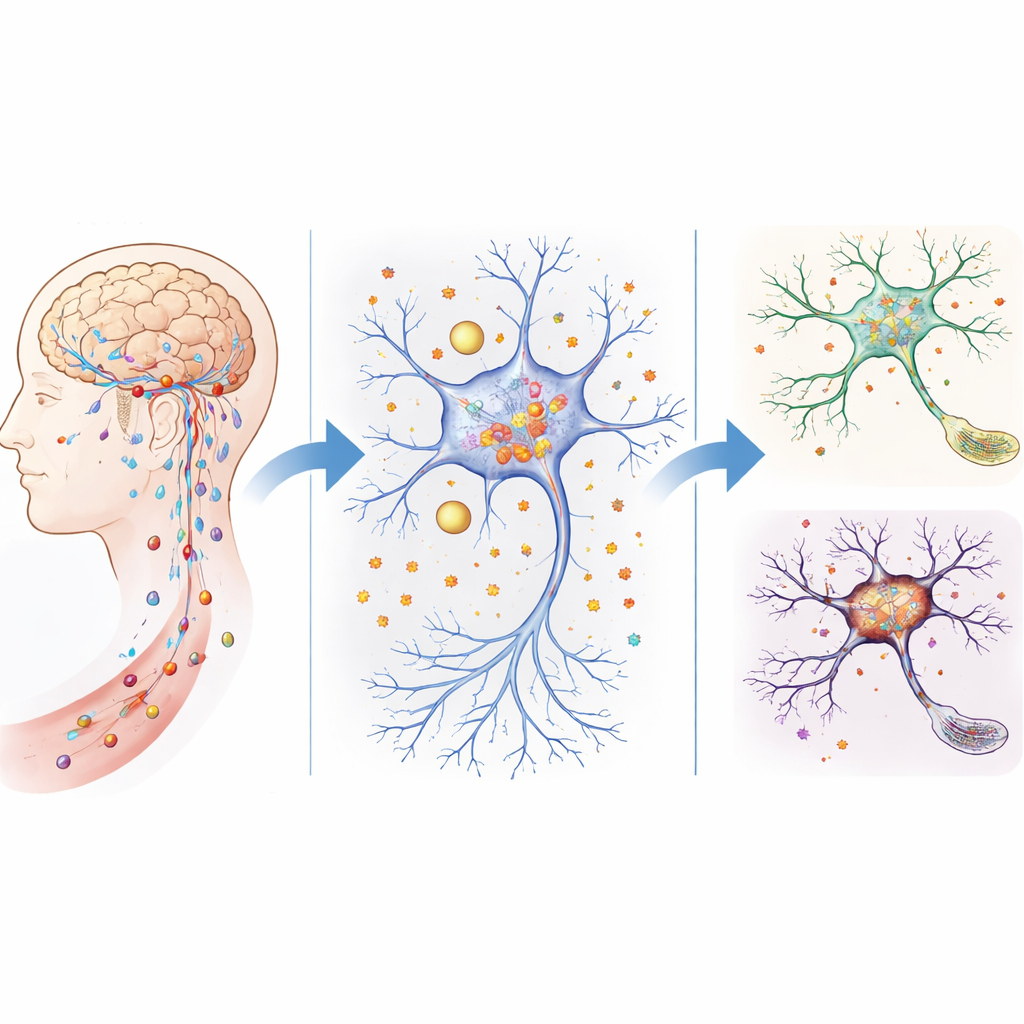
Defesas permeáveis e acúmulo de ferro no cérebro envelhecido
O cérebro é normalmente protegido por um sistema de filtro rigoroso — a barreira hematoencefálica e estruturas relacionadas — que controlam cuidadosamente o que entra a partir da corrente sanguínea. Em camundongos mais velhos, e em animais geneticamente sem ATP11B, essa barreira torna‑se mais permeável. A equipe mostrou que esses camundongos permitiam que mais pequenas moléculas penetrassem no tecido cerebral, e os níveis de ferro livre aumentaram fortemente em regiões-chave, especialmente o hipocampo, crucial para aprendizagem e memória. Testes comportamentais revelaram que camundongos sem ATP11B envelheciam mais rápido, apresentavam pior interação social, moviam‑se com menos confiança e tiveram desempenho inferior em labirintos e tarefas de memória, imitando problemas cognitivos relacionados à idade em humanos.
Como células de suporte gerenciam mal o ferro
Usando sequenciamento de célula única e mapeamento espacial, os pesquisadores examinaram quais células cerebrais foram mais afetadas pela perda de ATP11B. Eles focaram nas células ependimárias, que revestem os espaços preenchidos por fluido no cérebro e ajudam a transportar nutrientes e íons entre o líquido e o tecido cerebral. Em camundongos deficientes em ATP11B, o equilíbrio entre subtipos de células ependimárias mudou para formas que favorecem o transporte de íons metálicos, e essas células pareceram migrar mais perto do hipocampo. Análises genéticas sugeriram que essa mudança promoveu uma entrega anormal de ferro aos neurônios próximos. Marcadores de manejo de ferro e de regulação da memória nessas regiões foram alterados, e sinais precoces de envelhecimento celular surgiram primeiro nas células ependimárias e depois nos neurônios, o que sugere que o ferro mal gerido pelas células de suporte pode danificar os neurônios à distância.
Ferro, usinas de energia quebradas e uma morte celular inflamável
Dentro dos neurônios, o excesso de ferro pode desencadear uma reação em cadeia chamada ferroptose — um tipo de morte celular impulsionado por dano oxidativo aos componentes lipídicos da membrana. Os autores mostraram que reduzir ATP11B em células nervosas derivadas de humanos aumentou o ferro livre, reduziu a capacidade de armazenamento de ferro e elevou marcadores de ferroptose. Ao mesmo tempo, as mitocôndrias das células — as pequenas usinas que geram energia — ficaram estruturalmente distorcidas, perderam potencial de membrana e consumiram menos oxigênio. As células tentaram compensar aumentando a queima de glicose e produzindo mais lactato, mas isso veio acompanhado de mais moléculas reativas que danificaram ainda mais as membranas. As mitocôndrias fragmentaram em vez de se fundirem, os processos de limpeza foram hiperativados, e sinais de envelhecimento celular e aumento de espécies reativas de oxigênio apareceram, tudo contribuindo para sinais elétricos mais fracos entre os neurônios.
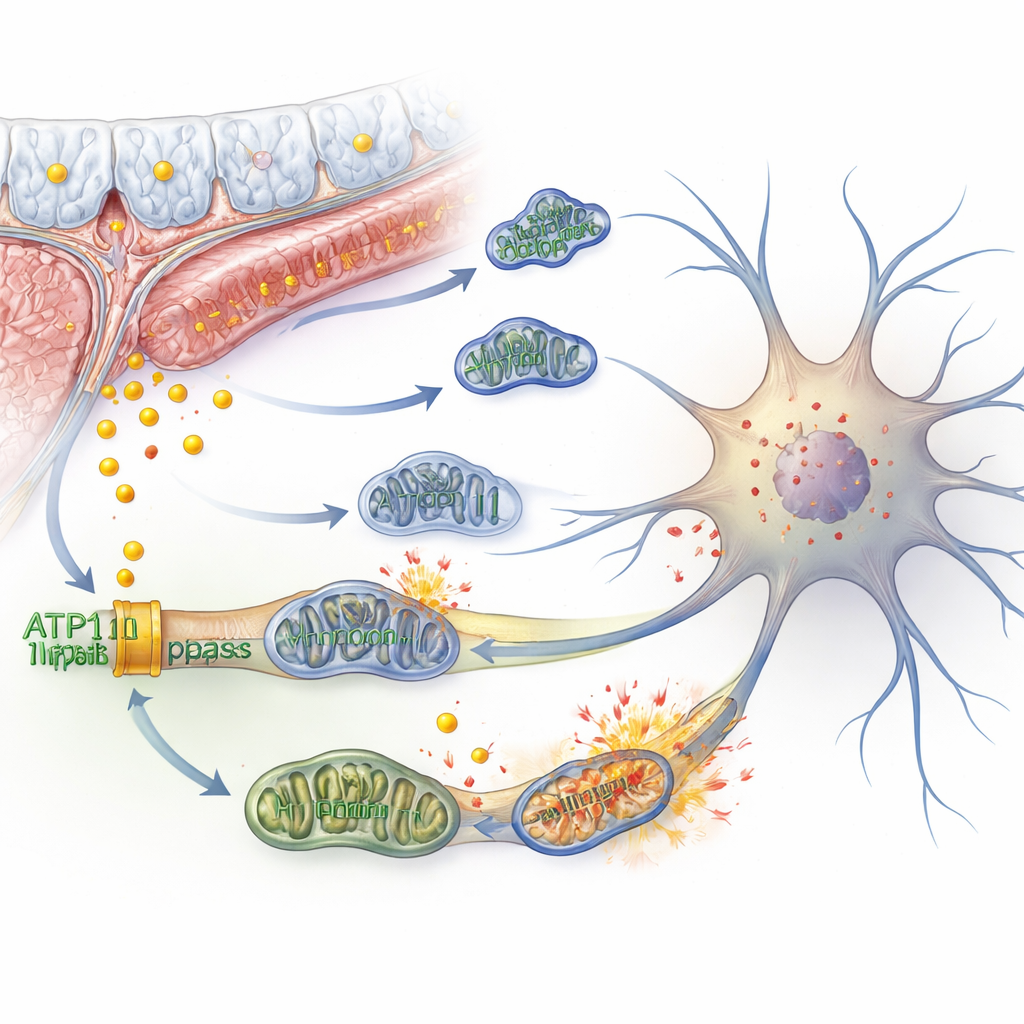
Um eixo de controle molecular no núcleo
O estudo avançou para perguntar como ATP11B controla tantos eventos a jusante. Ao examinar como o DNA é empacotado e lido nos neurônios, a equipe descobriu que a perda de ATP11B torna a cromatina — o material que envolve o DNA — menos acessível em sítios específicos. Isso afetou especialmente regiões de ligação de um fator de transcrição chamado KLF4, que normalmente ajuda a manter genes para a função mitocondrial saudável. Ao mesmo tempo, uma via de controle do crescimento conhecida como Hippo tornou‑se menos ativa, permitindo que uma proteína chamada YAP se movesse para o núcleo e formasse um complexo que ativa genes ligados à ferroptose e ao envelhecimento. O lactato mais alto proveniente das mitocôndrias estressadas também alimentou marcas químicas em histonas (lactilação de histonas), aumentando ainda mais a expressão de genes pró‑envelhecimento e pró‑ferroptose. Juntas, essas alterações nucleares aprisionaram os neurônios em um ciclo auto‑reforçador de estresse de ferro e falha mitocondrial.
Religando o interruptor
Animadoramente, o dano não foi totalmente irreversível. Quando os pesquisadores entregaram ATP11B adicional a camundongos idosos usando um vetor viral, muitos problemas relacionados à idade melhoraram. Os animais tratados caminharam com passos mais longos e estáveis, mantiveram melhor o equilíbrio, exploraram novos ambientes com mais prontidão e tiveram desempenho significativamente melhor em testes de memória. Ao microscópio, seus neurônios mostraram ramos mais longos e espinhas mais complexas, características estruturais associadas a conexões sinápticas mais fortes. Marcadores moleculares indicaram que o dano lipídico impulsionado pelo ferro e o estresse mitocondrial foram reduzidos. Em termos simples, restaurar ATP11B ajudou a reiniciar o manejo do ferro e a saúde mitocondrial, aliviando a pressão que empurra neurônios envelhecidos em direção à morte e ao declínio cognitivo.
O que isso significa para a saúde do cérebro
Para um público leigo, este trabalho sugere que parte do envelhecimento cerebral pode se resumir a uma falha específica em como as células equilibram ferro, produção de energia e controle gênico. ATP11B atua como um coordenador central: quando ele é perdido, o ferro se acumula silenciosamente, as usinas das células cerebrais falham e um processo destrutivo, parecido com a ferrugem, corrói lentamente os circuitos da memória. Quando o ATP11B é restaurado, ao menos em camundongos, muitas dessas tendências podem ser revertidas. Embora transformar essa descoberta em terapias seguras para pessoas exija avanços importantes na entrega gênica e testes de longo prazo, o estudo destaca um novo alvo promissor para preservar o raciocínio, a memória e a independência em uma população que envelhece.
Citação: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Palavras-chave: envelhecimento cerebral, acúmulo de ferro, disfunção mitocondrial, ferroptose neuronal, declínio cognitivo