Clear Sky Science · es
Apuntar al eje ATP11B-YAP restaura la función mitocondrial e inhibe la ferroptosis neuronal para atenuar el deterioro cognitivo relacionado con la edad
Por qué importa al envejecer
A medida que la gente vive más, muchos se preocupan menos por añadir años a la vida y más por mantener esas años con agudeza mental. Este estudio explora por qué el cerebro envejecido se vuelve vulnerable a la pérdida de memoria y a enfermedades como el Alzheimer, e identifica un único “interruptor” molecular —llamado ATP11B— que ayuda a proteger las células cerebrales de una forma de daño lenta impulsada por el hierro. Al comprender cómo este interruptor falla con la edad, los investigadores trazan una posible vía para ralentizar o incluso revertir el deterioro cognitivo relacionado con la edad.
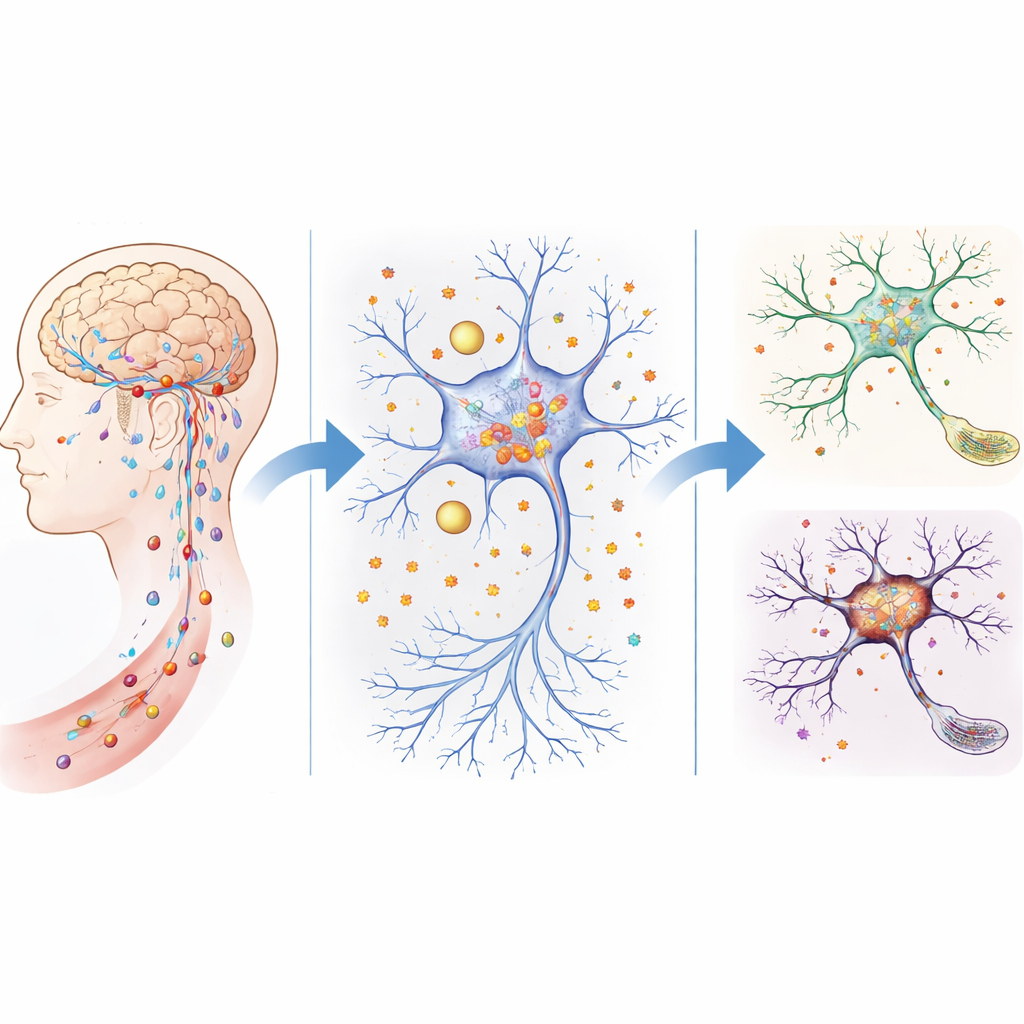
Defensas permeables y acumulación de hierro en el cerebro envejecido
Normalmente, el cerebro está protegido por un sistema de filtrado estricto —la barrera hematoencefálica y estructuras relacionadas— que controlan cuidadosamente lo que entra desde el torrente sanguíneo. En ratones envejecidos, y en ratones genéticamente carentes de ATP11B, esta barrera se vuelve más permeable. El equipo mostró que estos ratones permitían que más moléculas pequeñas se filtraran hacia el tejido cerebral, y los niveles de hierro libre aumentaron de forma marcada en regiones clave, especialmente el hipocampo, crucial para el aprendizaje y la memoria. Las pruebas de comportamiento revelaron que los ratones sin ATP11B envejecían antes, mostraban peor interacción social, se movían con menos confianza y obtenían peores resultados en laberintos y tareas de memoria, imitando los problemas cognitivos humanos relacionados con la edad.
Cómo las células de soporte gestionan mal el hierro
Mediante secuenciación a célula única y mapeo espacial, los investigadores examinaron qué células cerebrales se veían más afectadas por la pérdida de ATP11B. Se centraron en las células ependimarias, que recubren los espacios llenos de líquido del cerebro y ayudan a transportar nutrientes e iones entre el líquido y el tejido cerebral. En ratones deficientes en ATP11B, el equilibrio de subtipos de células ependimarias se desplazó hacia aquellas que favorecen el transporte de iones metálicos, y estas células parecían migrar más cerca del hipocampo. Los análisis genéticos sugirieron que este cambio promovía una entrega anómala de hierro a las neuronas cercanas. Los marcadores de manejo del hierro y de regulación de la memoria en estas regiones estaban alterados, y los signos tempranos de envejecimiento celular aparecieron primero en las células ependimarias y luego en las neuronas, lo que implica que el hierro mal gestionado desde las células de soporte puede causar daño neuronal a distancia.
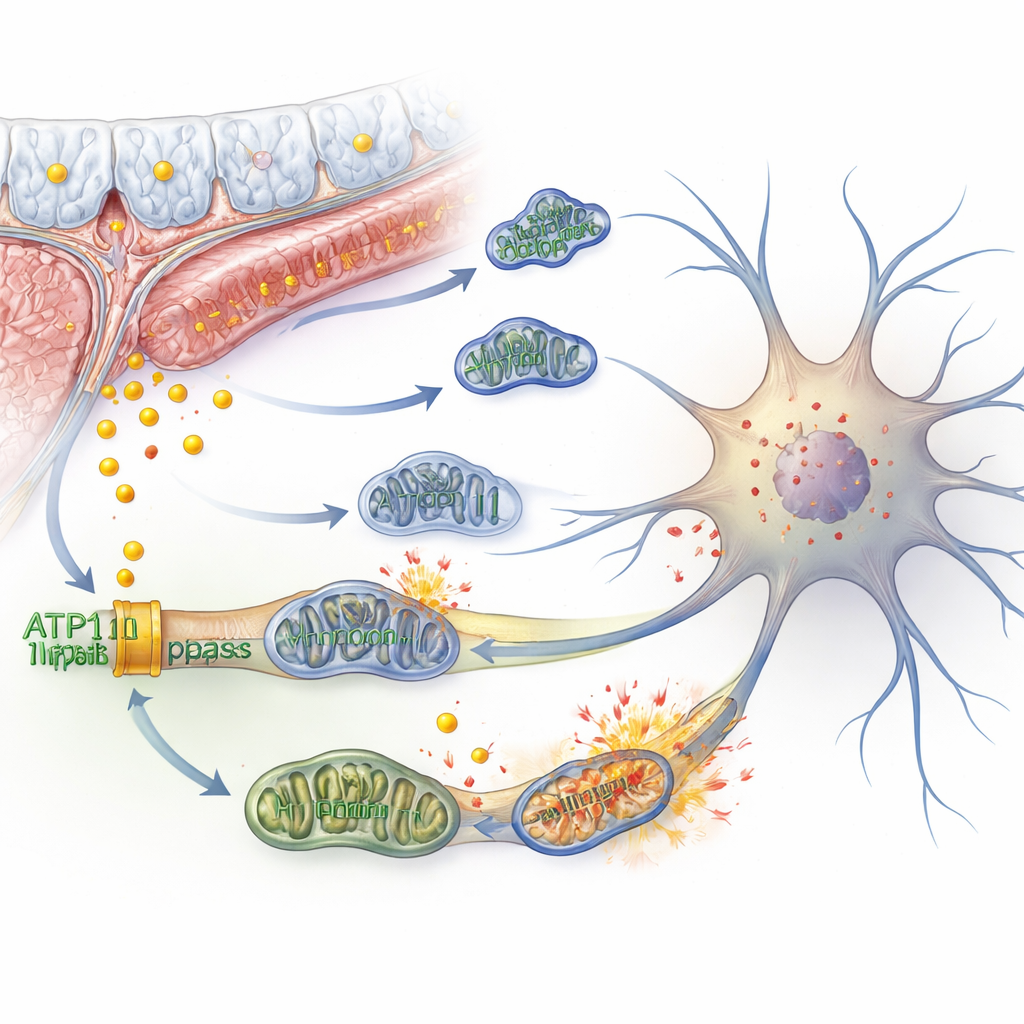
Hierro, centrales eléctricas rotas y una muerte celular abrasadora
Dentro de las neuronas, el exceso de hierro puede desencadenar una reacción en cadena llamada ferroptosis —un tipo de muerte celular impulsada por daño oxidativo a los componentes grasos de la membrana celular. Los autores demostraron que reducir ATP11B en células nerviosas derivadas de humanos aumentaba el hierro libre, reducía la capacidad de almacenamiento de hierro y elevaba marcadores de ferroptosis. Al mismo tiempo, las mitocondrias de las células —las pequeñas centrales que generan energía— se distorsionaron estructuralmente, perdieron su potencial de membrana y consumieron menos oxígeno. Las células intentaron compensar aumentando la quema de azúcares y produciendo más lactato, pero ello vino acompañado de más especies reactivas que dañaron aún más las membranas. Las mitocondrias se fragmentaron en lugar de fusionarse, los procesos de limpieza celular se sobreactivaron, y aparecieron signos de envejecimiento celular y aumento de especies reactivas, todo lo cual contribuyó a un debilitamiento de la señalización eléctrica entre neuronas.
Un eje de control molecular en el núcleo
El estudio profundizó para preguntar cómo ATP11B controla tantos eventos aguas abajo. Al examinar cómo se empaqueta y lee el ADN en las neuronas, el equipo encontró que la pérdida de ATP11B hace que la cromatina —el material que envuelve el ADN— sea menos accesible en sitios específicos. Esto afectó especialmente a las regiones de unión de un factor de transcripción llamado KLF4, que normalmente ayuda a mantener genes para la función mitocondrial saludable. Al mismo tiempo, una vía de control del crecimiento conocida como Hippo se volvió menos activa, permitiendo que una proteína llamada YAP se moviera al núcleo y formara un complejo que activa genes vinculados a la ferroptosis y al envejecimiento. El lactato elevado procedente de mitocondrias estresadas también contribuyó a marcas químicas en las histonas (lactalilación de histonas), potenciando aún más la expresión de genes clave pro‑envejecimiento y pro‑ferroptosis. En conjunto, estos cambios nucleares bloquearon a las neuronas en un ciclo auto‑reforzante de estrés por hierro y fallo mitocondrial.
Volver a encender el interruptor
De forma alentadora, el daño no fue totalmente irreversible. Cuando los investigadores administraron ATP11B adicional a ratones envejecidos usando un vector viral, muchos problemas propios de la edad mejoraron. Los ratones tratados caminaban con pasos más largos y estables, mantenían mejor el equilibrio, exploraban nuevos entornos con más facilidad y obtuvieron rendimientos significativamente mejores en pruebas de memoria. Al microscopio, sus neuronas mostraron dendritas más largas y espinas más complejas, rasgos estructurales vinculados a conexiones sinápticas más fuertes. Los marcadores moleculares indicaron que el daño lipídico impulsado por el hierro y el estrés mitocondrial se redujeron. En términos sencillos, restaurar ATP11B ayudó a reajustar el manejo del hierro y la salud mitocondrial, aliviando la presión que empuja a las neuronas envejecidas hacia la muerte y el declive cognitivo.
Qué significa esto para la salud cerebral
Para un lector no especialista, este trabajo sugiere que parte del envejecimiento cerebral puede reducirse a una falla específica en cómo las células gestionan el hierro, la producción de energía y el control génico. ATP11B actúa como un coordinador central: cuando se pierde, el hierro se acumula silenciosamente, las centrales celulares fallan y un proceso destructivo, similar a la oxidación, erosiona lentamente los circuitos de la memoria. Cuando ATP11B se restaura, al menos en ratones, muchas de estas tendencias pueden invertirse. Aunque convertir este hallazgo en terapias seguras para personas requerirá avances importantes en la entrega génica y pruebas a largo plazo, el estudio destaca un objetivo prometedor para preservar el pensamiento, la memoria y la independencia en una población envejecida.
Cita: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Palabras clave: envejecimiento cerebral, sobrecarga de hierro, disfunción mitocondrial, ferroptosis neuronal, declive cognitivo