Clear Sky Science · pl
Celowanie w oś ATP11B–YAP naprawia funkcję mitochondriów i hamuje ferroptozę neuronów, łagodząc związany z wiekiem spadek funkcji poznawczych
Dlaczego to ma znaczenie dla starzenia się
W miarę jak ludzie żyją dłużej, coraz mniej chodzi o samo dodawanie lat, a coraz więcej o zachowanie sprawności umysłowej. W tym badaniu zbadano, dlaczego starzejący się mózg staje się podatny na utratę pamięci i choroby takie jak choroba Alzheimera, oraz zidentyfikowano pojedynczy molekularny „przełącznik” — ATP11B — który pomaga chronić komórki mózgowe przed powolnym, napędzanym przez żelazo rodzajem uszkodzenia. Rozumiejąc, jak ten przełącznik zawodzi z wiekiem, badacze nakreślili możliwy nowy sposób spowolnienia, a nawet odwrócenia związanego z wiekiem spadku funkcji poznawczych.
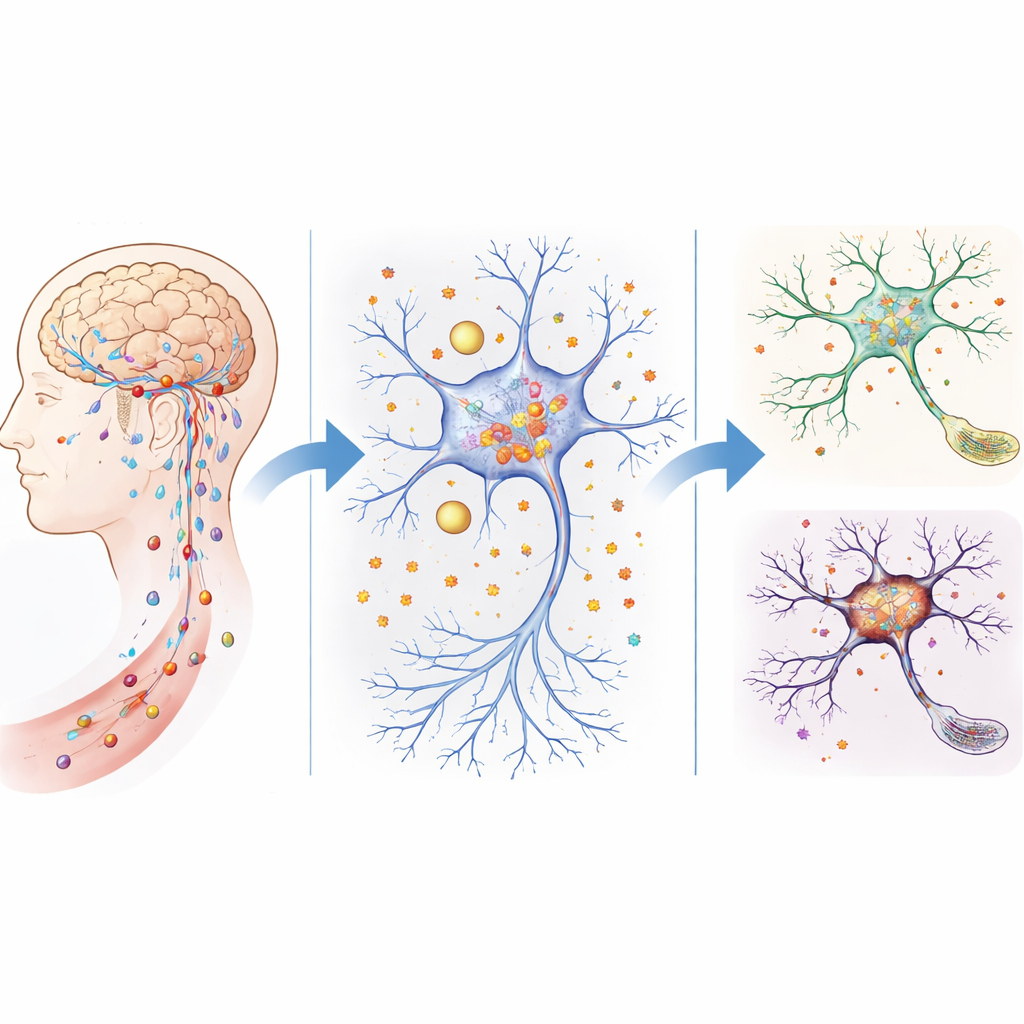
Nieszczelne bariery i gromadzenie żelaza w starzejącym się mózgu
Mózg zwykle chroniony jest przez ścisły system filtrów — barierę krew–mózg i pokrewne struktury — które kontrolują, co przedostaje się z krwiobiegu. U starszych myszy, a także u myszy pozbawionych genetycznie ATP11B, ta bariera staje się bardziej przepuszczalna. Zespół wykazał, że u tych myszy więcej małych cząsteczek przenika do tkanki mózgowej, a poziomy wolnego żelaza gwałtownie rosną w kluczowych obszarach, zwłaszcza w hipokampie, który jest istotny dla uczenia się i pamięci. Testy behawioralne wykazały, że myszy bez ATP11B starzały się szybciej, wykazywały gorsze interakcje społeczne, poruszały się mniej pewnie i wypadały gorzej w zadaniach labiryntowych i pamięciowych, naśladując ludzkie problemy poznawcze związane z wiekiem.
Jak komórki wspierające źle gospodarują żelazem
Wykorzystując sekwencjonowanie pojedynczych komórek i mapowanie przestrzenne, badacze sprawdzili, które komórki mózgowe były najbardziej dotknięte utratą ATP11B. Skupili się na komórkach ependymalnych, które wyściełają wypełnione płynem przestrzenie mózgu i pomagają transportować substancje odżywcze oraz jony między płynem a tkanką mózgową. U myszy z niedoborem ATP11B równowaga podtypów komórek ependymalnych przesunęła się w stronę tych sprzyjających transportowi jonów metali, a komórki te wydawały się przemieszczać bliżej hipokampa. Analizy genów sugerowały, że ta zmiana sprzyjała nieprawidłowej dostawie żelaza do pobliskich neuronów. Markery gospodarki żelazem i regulacji pamięci w tych obszarach były zmienione, a wczesne oznaki starzenia komórkowego pojawiały się najpierw w komórkach ependymalnych, a potem w neuronach, co sugeruje, że nieodpowiednio zarządzane żelazo z komórek wsparcia może z daleka napędzać uszkodzenie neuronów.
Żelazo, uszkodzone elektrownie i „ognista” śmierć komórki
W neuronach nadmiar żelaza może wywołać reakcję łańcuchową zwaną ferroptozą — rodzaj śmierci komórki napędzany oksydacyjnym uszkodzeniem lipidów błony komórkowej. Autorzy pokazali, że zmniejszenie ekspresji ATP11B w pochodnych ludzkich komórek nerwowych zwiększyło poziom wolnego żelaza, zmniejszyło zdolność magazynowania żelaza i nasiliło markery ferroptozy. Jednocześnie mitochondria komórek — maleńkie elektrownie produkujące energię — ulegały deformacji strukturalnej, traciły potencjał błonowy i konsumowały mniej tlenu. Komórki próbowały kompensować to zwiększeniem spalania cukrów i produkcji mleczanu, ale wiązało się to z wyższą ilością reaktywnych cząsteczek, które dodatkowo uszkadzały błony. Mitochondria fragmentowały się zamiast łączyć, procesy oczyszczania były nadmiernie aktywowane, pojawiały się oznaki starzenia komórkowego i wzrostu reaktywnych form tlenu — wszystko to przyczyniało się do osłabienia sygnalizacji elektrycznej między neuronami.
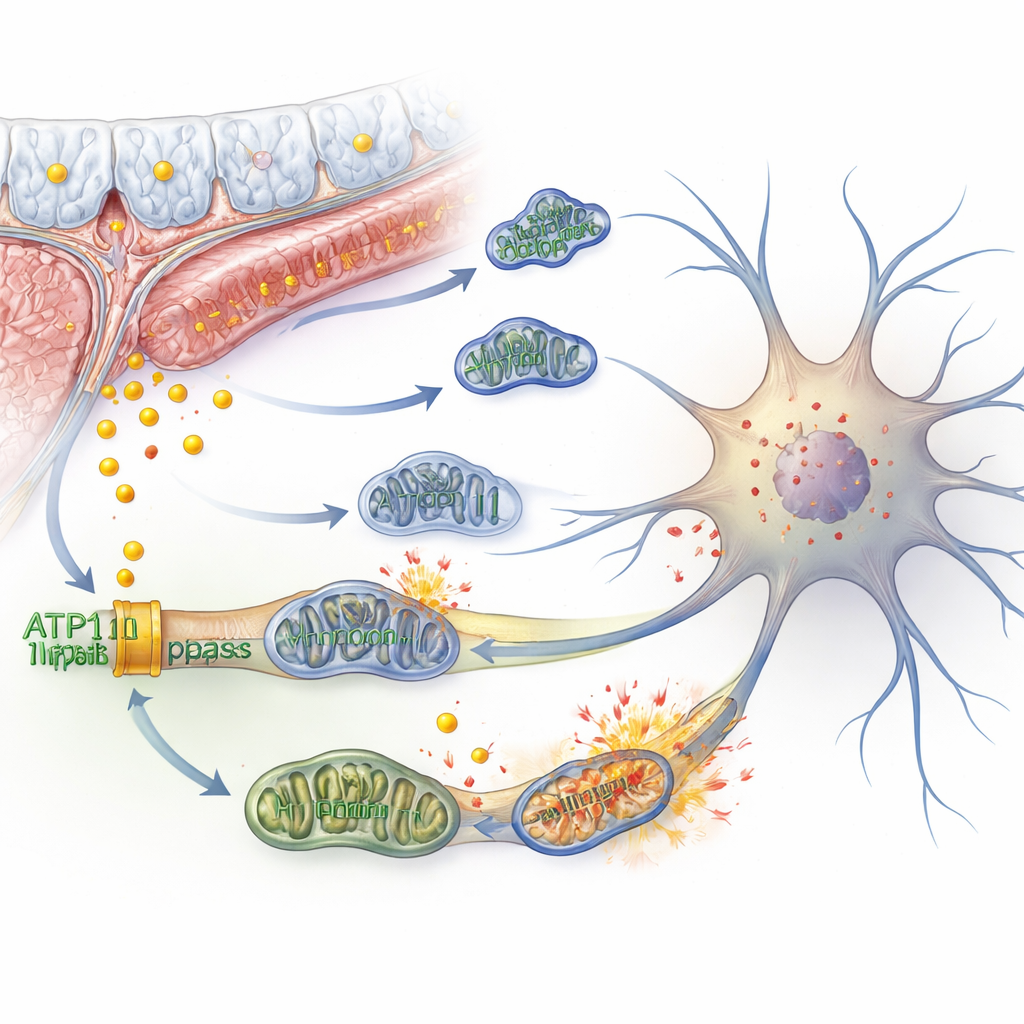
Molekularna oś kontrolna w jądrze
Badanie poszło dalej, by sprawdzić, jak ATP11B kontroluje tak wiele zdarzeń położonych „dookoła”. Analizując, jak DNA jest pakowane i odczytywane w neuronach, zespół stwierdził, że utrata ATP11B czyni chromatynę — materiał owijający DNA — mniej dostępną w określonych miejscach. Szczególnie dotyczyło to miejsc wiązania czynnika transkrypcyjnego KLF4, który normalnie pomaga utrzymać geny ważne dla zdrowej funkcji mitochondriów. Jednocześnie ścieżka kontroli wzrostu znana jako Hippo stawała się mniej aktywna, co pozwalało białku YAP przenikać do jądra i tworzyć kompleks uruchamiający geny powiązane z ferroptozą i starzeniem. Wyższy poziom mleczanu pochodzącego ze zestresowanych mitochondriów wpływał również na chemiczne znaczniki na histonach (laktylacja histonów), co dodatkowo zwiększało ekspresję kluczowych genów sprzyjających starzeniu i ferroptozie. Te jądrowe zmiany razem blokowały neurony w samonapędzającym się cyklu stresu żelazowego i upadku mitochondriów.
Włączenie przełącznika na nowo
Co zachęcające, uszkodzenia nie były całkowicie nieodwracalne. Kiedy badacze dostarczyli dodatkowe ATP11B do starszych myszy za pomocą wektora wirusowego, wiele problemów związanych z wiekiem uległo poprawie. Leczone myszy chodziły z dłuższymi, bardziej stabilnymi krokami, lepiej utrzymywały równowagę, chętniej eksplorowały nowe otoczenie i wypadły znacząco lepiej w testach pamięci. Pod mikroskopem ich neurony miały dłuższe odgałęzienia i bardziej złożone kolce dendrytyczne — cechy strukturalne powiązane z mocniejszymi połączeniami synaptycznymi. Markery molekularne wskazywały, że uszkodzenia lipidowe napędzane żelazem i stres mitochondrialny zostały zredukowane. Prościej mówiąc: przywrócenie ATP11B pomogło zresetować gospodarkę żelazem i zdrowie mitochondriów, zmniejszając presję, która popycha starzejące się neurony ku śmierci i utracie funkcji poznawczych.
Co to oznacza dla zdrowia mózgu
Dla osoby niebędącej specjalistą to badanie sugeruje, że część starzenia się mózgu może sprowadzać się do konkretnej awarii w tym, jak komórki gospodarują żelazem, produkcją energii i kontrolą genów. ATP11B działa jako centralny koordynator: gdy go brakuje, żelazo cicho się kumuluje, elektrownie komórkowe zawodzą, a destrukcyjny, „rdzewiejący” proces stopniowo niszczy obwody pamięciowe. Przywrócenie ATP11B, przynajmniej u myszy, może odwrócić wiele z tych tendencji. Przekształcenie tego odkrycia w bezpieczne terapie dla ludzi będzie wymagać znaczących postępów w dostarczaniu genów i długoterminowych testach, ale badanie wskazuje obiecujący nowy cel dla zachowania myślenia, pamięci i niezależności w starzejącej się populacji.
Cytowanie: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
Słowa kluczowe: starzenie się mózgu, nadmiar żelaza, dysfunkcja mitochondriów, neuronalna ferroptoza, spadek funkcji poznawczych