Clear Sky Science · ar
استهداف محور ATP11B–YAP يصلح وظيفة الميتوكوندريا ويثبط الفيروبتوز العصبي ليخفف التراجع المعرفي المرتبط بالعمر
لماذا هذا مهم مع التقدم في العمر
مع ازدياد مدة حياة الناس، يقل القلق لدى كثيرين بشأن مجرد زيادة السنوات ويزداد الاهتمام بالحفاظ على حدة الذهن. تستقصي هذه الدراسة سبب تعرّض الدماغ المسن لفقدان الذاكرة وأمراض مثل الزهايمر، وتحدد «مفتاحاً» جزيئياً واحداً — يدعى ATP11B — يساعد على حماية خلايا الدماغ من شكل بطيء من الضرر المدفوع بالحديد. من خلال فهم كيفية فشل هذا المفتاح مع التقدم في العمر، يحدد الباحثون طريقاً محتملاً لإبطاء أو حتى عكس التراجع المعرفي المرتبط بالعمر.
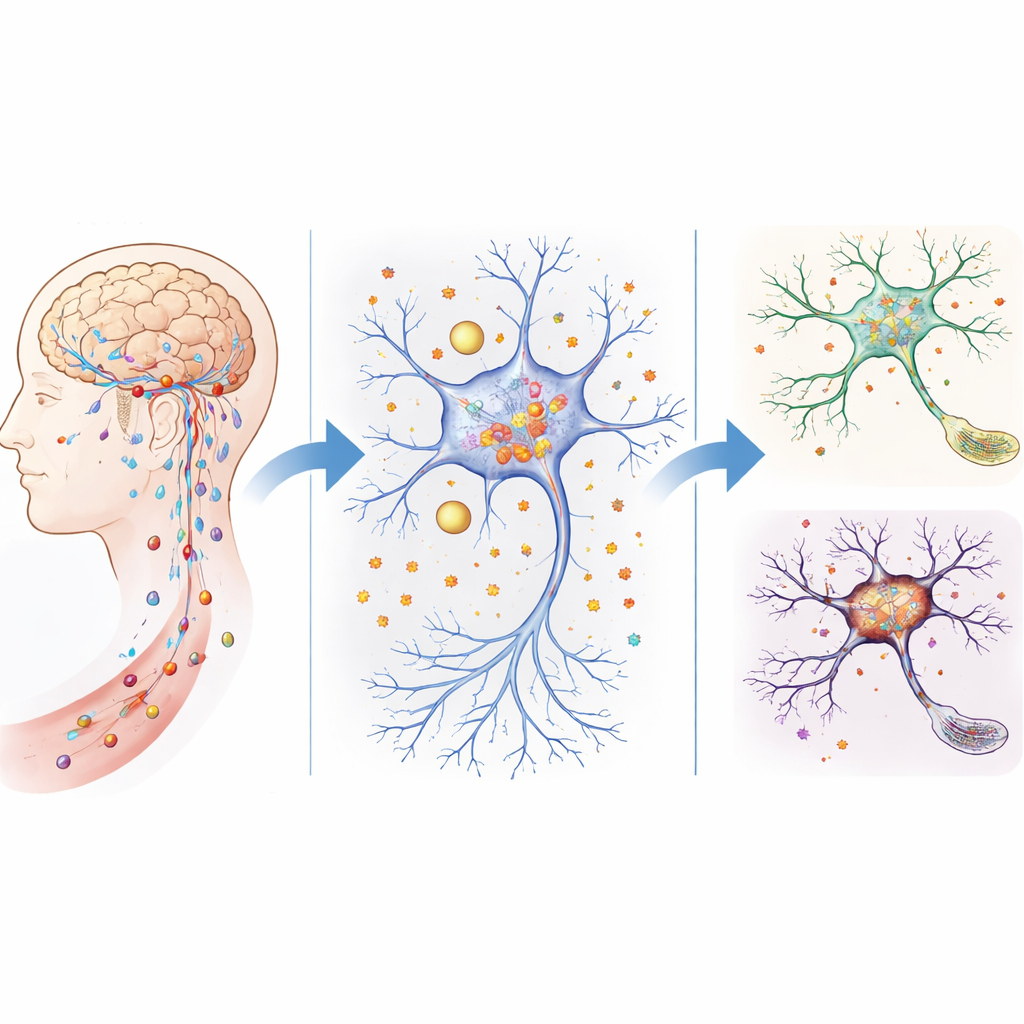
دفاعات متسربة وتراكم الحديد في الدماغ المسن
يُحاط الدماغ عادةً بنظام ترشيح محكم — الحاجز الدموي الدماغي وبُنى ذات صلة — تتحكم بعناية فيما يدخل من مجرى الدم. في الفئران المسنة، وفي الفئران التي تفتقر وراثياً إلى ATP11B، يصبح هذا الحاجز أكثر تسريباً. أظهرت الفريق أن هذه الفئران سمحت لتسرب المزيد من الجزيئات الصغيرة إلى نسيج المخ، وارتفعت مستويات الحديد الحر بشكل حاد في مناطق رئيسية، خاصة الحصين الذي يعد أساسياً للتعلم والذاكرة. كشفت اختبارات السلوك أن الفئران بدون ATP11B تقدمت في العمر أسرع، وأظهرت تفاعلات اجتماعية أضعف، وتحركت بثقة أقل، وأداء أدنى في المتاهات ومهمات الذاكرة، محاكاةً لمشكلات معرفية مرتبطة بالعمر لدى البشر.
كيف يسيء الخلايا الداعمة إدارة الحديد
باستخدام التسلسل الخلوي المفرد والتخطيط المكاني، فحص الباحثون أي خلايا الدماغ تأثرت أكثر بفقدان ATP11B. ركزوا على خلايا البطانة الظهارية (ependymal) التي تبطن الفراغات المملوءة بالسائل في الدماغ وتساعد على نقل المواد الغذائية والأيونات بين السائل ونسيج الدماغ. في الفئران الخالية من ATP11B، تحوّل التوازن بين أنواع هذه الخلايا نحو الأنواع التي تفضّل نقل أيونات المعادن، وبدا أن هذه الخلايا تهاجر أقرب إلى الحصين. أشارت تحليلات الجينات إلى أن هذا التغير عزز توصيل الحديد الشاذ إلى الخلايا العصبية المجاورة. تغيّرت مؤشرات التعامل مع الحديد وتنظيم الذاكرة في هذه المناطق، وظهرت علامات مبكرة للشيخوخة الخلوية أولاً في خلايا البطانة ثم في الخلايا العصبية، ما يوحي بأن سوء إدارة الحديد من الخلايا الداعمة قد يسبب تلف الخلايا العصبية عن بُعد.
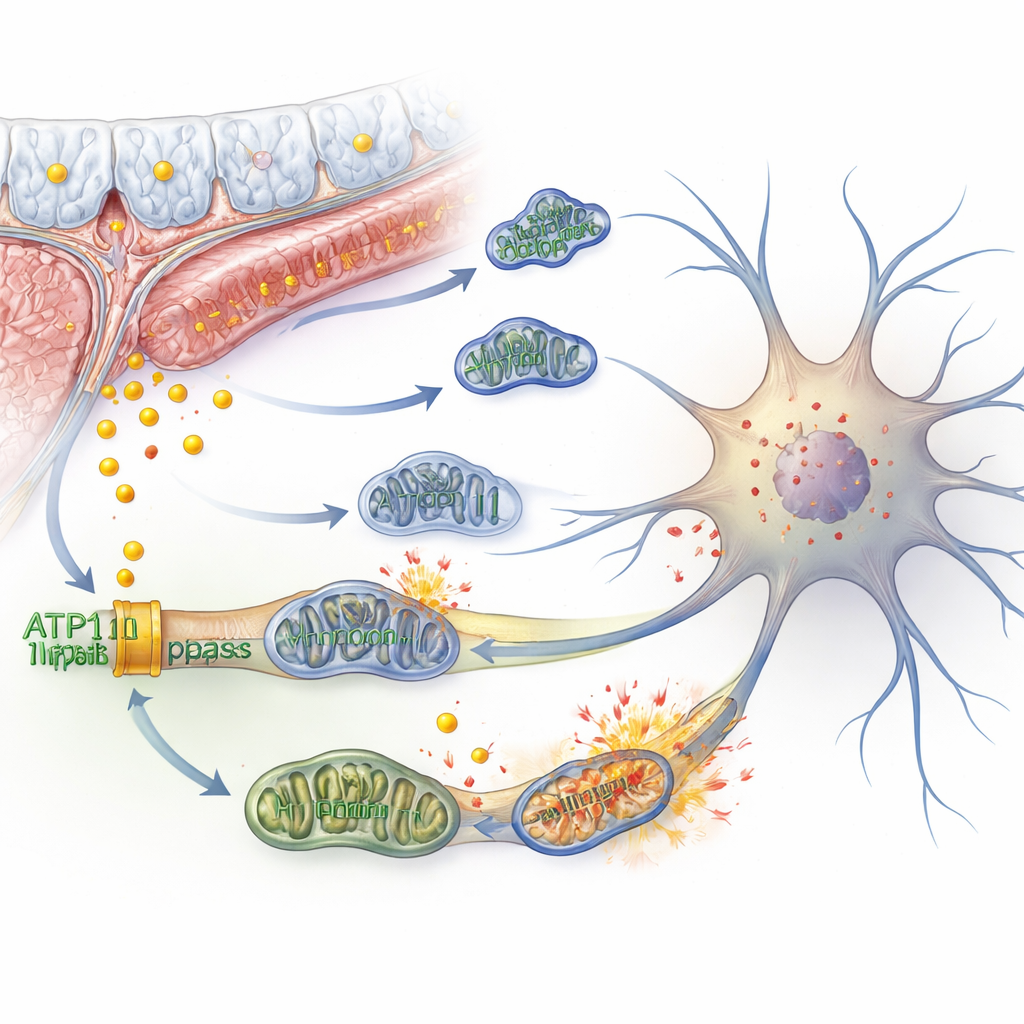
الحديد، محطات الطاقة المعطلة، وموت خلوي مشتعل
داخل الخلايا العصبية، يمكن للحديد الزائد أن يطلق سلسلة تفاعلات تسمى الفيروبتوز — نوع من موت الخلايا يقوده الضرر التأكسدي لمكونات الدهون في غشاء الخلية. أظهر المؤلفون أن تثبيط ATP11B في خلايا عصبية مشتقة من الإنسان زاد من الحديد الحر، وقلل قدرة التخزين الحديدي، وزاد مؤشرات الفيروبتوز. في الوقت نفسه، أصبحت الميتوكوندريا — مصانع الطاقة الصغيرة التي تولد الطاقة — مشوهة تركيبياً، فقدت فرق الجهد عبر أغشيتها، واستهلكت كمية أقل من الأكسجين. حاولت الخلايا التعويض بزيادة حرق السكر وإنتاج المزيد من اللاكتات، لكن هذا صاحبته جزيئات تفاعلية أكثر أضرت بالغشاء بشكل إضافي. تجزأت الميتوكوندريا بدلاً من أن تندمج، فُعّلت عمليات التنظيف بشكل مفرط، وظهرت علامات الشيخوخة الخلوية وارتفاع مستويات الأكسجة التفاعلية، وكل ذلك ساهم في ضعف الإشارة الكهربائية بين الخلايا العصبية.
محور تحكّم جزيئي في النواة
تعمقت الدراسة لسؤال كيف يتحكم ATP11B في هذا العدد الكبير من الأحداث اللاحقة. من خلال فحص كيفية تعبئة وقراءة الحمض النووي في الخلايا العصبية، وجد الفريق أن فقدان ATP11B يجعل الكروماتين — المادة التي تلفّ الحمض النووي — أقل إمكانية وصول في مواقع محددة. أثر هذا خصوصاً على مناطق ارتباط لعامل نسخ يدعى KLF4، الذي يساعد عادةً على الحفاظ على جينات وظيفة الميتوكوندريا الصحية. في الوقت نفسه، أصبح مسار التحكم بالنمو المعروف باسم Hippo أقل نشاطاً، مما أتاح لبروتين يسمى YAP الانتقال إلى النواة وتشكيل مركب يشغّل جينات مرتبطة بالفيروبتوز والشيخوخة. كما أن اللاكتات الأعلى الناتجة عن الميتوكوندريا المتوترة أدت إلى وسم كيميائي على الهياستونات (لاكتيلَيشن الهستون)، مما عزز تعبير جينات رئيسية معززة للشيخوخة والفيروبتوز. معاً، قفلت هذه التغييرات النووية الخلايا العصبية في دورة تغذية ذاتية من ضغط الحديد وفشل الميتوكوندريا.
إعادة تشغيل المفتاح
من المشجع أن الضرر لم يكن غير قابل للانعكاس تماماً. عندما أدخل الباحثون ATP11B إضافياً إلى فئران مسنة باستخدام ناقل فيروسي، تحسّنت كثير من المشكلات الشبيهة بالعمر. مشت الفئران المعالجة بخطوات أطول وأكثر ثباتاً، حافظت على توازن أفضل، استكشفت بيئات جديدة بشكل أكبر، وأدت أداءً أفضل بكثير في اختبارات الذاكرة. تحت المجهر، أظهرت خلاياهم العصبية تفرعات أطول وأشواكاً أكثر تعقيداً، وهي ميزات بنيوية مرتبطة باتصالات تشابكية أقوى. أشارت العلامات الجزيئية إلى أن الضرر الدهني المدفوع بالحديد وضغط الميتوكوندريا تقلصا. بمصطلحات بسيطة، ساعدت استعادة ATP11B على إعادة ضبط إدارة الحديد وصحة الميتوكوندريا، مما خفف الضغط الذي يدفع الخلايا العصبية المسنة نحو الموت والتراجع المعرفي.
ماذا يعني هذا لصحة الدماغ
للقارئ العام، توحي هذه الدراسة أن جزءاً من شيخوخة الدماغ قد يعود إلى فشل محدد في كيفية تلاعب الخلايا بالحديد وإنتاج الطاقة وتنظيم الجينات. يعمل ATP11B كمنسق مركزي: عندما يضيع، يتراكم الحديد بهدوء، تتعطل مصانع طاقة الخلايا، وعملية مدمرة تشبه الصدأ تآكل دوائر الذاكرة ببطء. عند استعادة ATP11B، على الأقل في الفئران، يمكن عكس كثير من هذه الاتجاهات. في حين أن تحويل هذه الرؤية إلى علاجات آمنة للبشر سيتطلب تقدماً كبيراً في توصيل الجينات واختبارات طويلة المدى، تبرز الدراسة هدفاً واعداً للحفاظ على التفكير والذاكرة والاستقلالية لدى السكان المسنين.
الاستشهاد: Qi, W., Liu, Q., Dong, N. et al. Targeting ATP11B-YAP axis repairs mitochondrial function and inhibits neuronal ferroptosis to attenuate age-related cognitive decline. Sig Transduct Target Ther 11, 141 (2026). https://doi.org/10.1038/s41392-026-02652-1
الكلمات المفتاحية: شيخوخة الدماغ, تراكم الحديد, خلل وظيفي في الميتوكوندريا, الفيروبتوز العصبي, تراجع إدراكي