Clear Sky Science · tr
Metabolik oksidoredüktazlar: kök hücrelikte epigenetik manzaraların merkezi düzenleyicileri
Hücre Yakıtı Hücre Kimliğini Nasıl Biçimlendirir
Vücudunuzdaki her hücre temel olarak aynı DNA’yı taşır, yine de nöronlar, kan hücreleri ve deri hücreleri tamamen farklı görünür ve davranır. Bu makale, hücrelerin yakıtı nasıl işlediği ile hangi hücre tipine dönüşeceklerini nasıl seçtikleri arasında şaşırtıcı bir bağı inceliyor. Enerji ve besinleri normalde işleyen bir enzim sınıfı olan oksidoredüktazların, hangi genlerin açık olacağını kontrol eden DNA ve proteinler üzerindeki kimyasal işaretleri yazıp silmeye de yardımcı olduğunu açıklıyor. Bu bağlantıyı anlamak, kök hücreler, yaşlanma ve hatta kanser hakkındaki düşüncelerimizi yeniden şekillendirebilir.
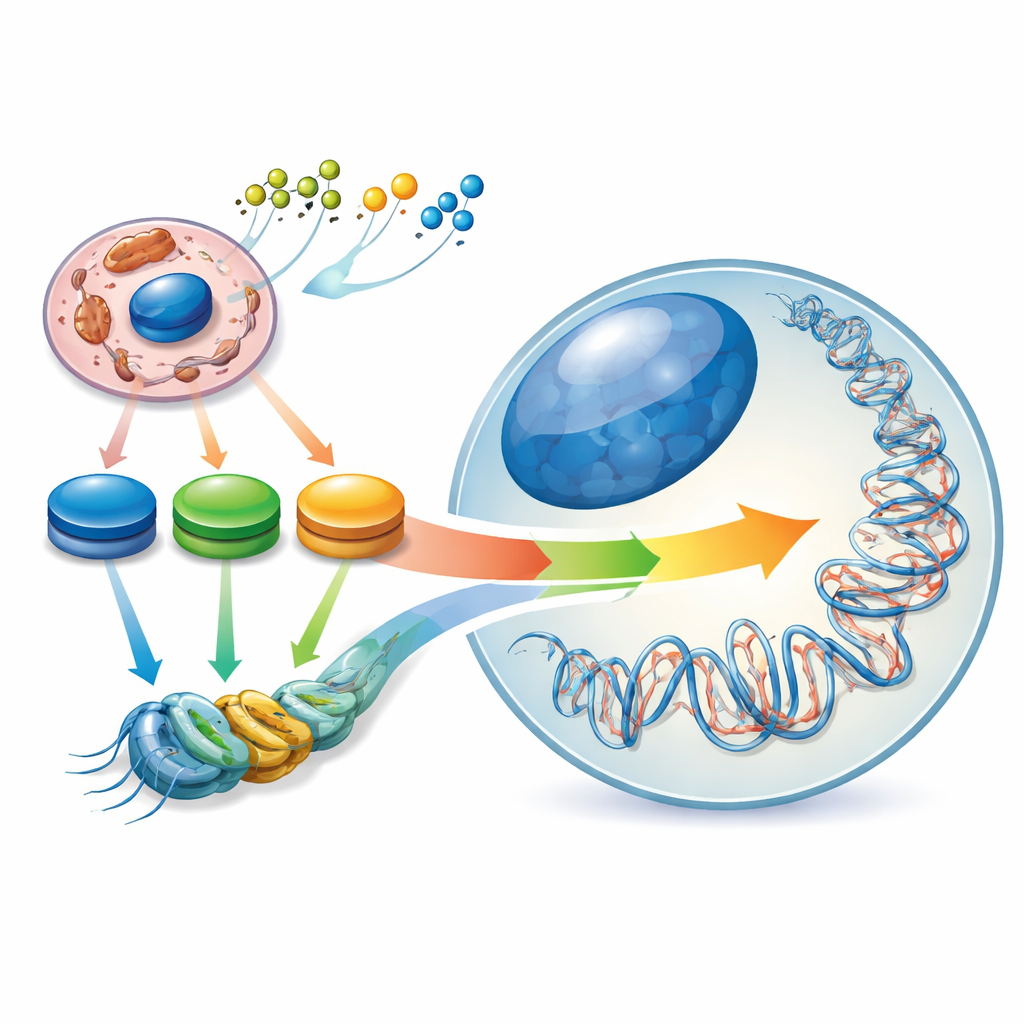
Genlerimizin İçindeki Gizli Manzara
Kök hücreler özeldir çünkü ya kendilerini yenileyebilirler ya da birçok farklı hücre tipine olgunlaşabilirler. Bu dengeyi, genler için birer karartma düğmesi gibi davranan DNA ve onun paketleyici proteinleri üzerindeki kimyasal etiketlerin desenlerinden oluşan içsel bir “epigenetik manzara” aracılığıyla yönetirler. Yazarlar bu manzarayı hücre içindeki bir “enerji konturu” tarafından şekillendirilen; asetil‑CoA, NAD⁺/NADH ve α‑ketoglutarat gibi ana metabolitlerin seviyelerindeki zirveler ve çukurlar olarak tanımlar. Bir kök hücre saf halden daha taahhütlü bir duruma geçtiğinde merkezi karbon metabolizması yeniden düzenlenir ve epigenetik manzara da onunla birlikte kayar. Dolayısıyla hücresel yakıt kullanımındaki değişiklikler yalnızca hücre kimliğinin bir sonucu değildir — aktif olarak onu belirlemeye yardımcı olurlar.
Yiyeceği Epigenetik Sinyallere Çeviren Enzimler
Oksidoredüktazlar, oksidasyon‑indirgeme reaksiyonlarını katalizleyen ve metabolizmanın kilit kavşaklarında bulunan enzimlerdir. Birçoğu, DNA ve histonları etiketleyen enzimler için hammadde veya kofaktör görevi gören “epigenetik metabolitler” üretir. Örneğin glikoliz ve TCA döngüsündeki dehidrogenazlar, histon asetilasyonu için asetil‑CoA, deasetilazları etkileyen NAD⁺/NADH ve NADPH ile DNA ve histon demetilazları için güç kaynağı olan α‑ketoglutaratı üretir. Bu metabolitlerin ne kadarının mevcut olduğunu kontrol ederek oksidoredüktazlar olası epigenetik değişikliklerin aralığını belirler. Farklı kök hücre durumları farklı metabolik karışımlara dayanır: saf pluripotent kök hücreler hem şekeri hem yağı kullanır, hazırlıklı (primed) pluripotent hücreler büyük ölçüde glikolize ve glutamine yönelir, birçok yetişkin kök hücre ise yağ asidi yıkımı ve oksidatif fosforilasyonu tercih eder.
DNA, RNA ve Histonların Doğrudan Düzenleyicileri
Bazı oksidoredüktazlar malzemeyi sağlamakla kalmaz, aynı zamanda epigenetik işaretleri doğrudan yeniden yazar. TET proteinleri ve JMJD demetilazlar gibi demir ve α‑ketoglutarat bağımlı enzimler DNA ve histonlardan metil gruplarını çıkararak hangi genlerin aktif olduğunu yeniden şekillendirir. İlgili enzimler ALKBH5 ve FTO, RNA üzerindeki metil işaretlerini siler ve mesajların ne kadar süre kaldığını ve ne kadar verimli çevrildiğini etkiler. Başka bir grup olan LSD1 ve LSD2, belirli histon lizinlerini demetilemek için flavin kofaktörü kullanır. Tüm bu enzimlerin metabolik kofaktörlere ve oksijene ihtiyaç duyması, aktivitelerinin hücrenin enerji ve redoks durumuna son derece duyarlı olmasını sağlar. Derleme, α‑ketoglutarat, süksinat veya kanserdeki mutant metabolitlerdeki değişimlerin açık, esnek kromatin ile sıkı kilitlenmiş, baskılanmış durumlar arasındaki dengeyi nasıl değiştirebileceğini gösterir.
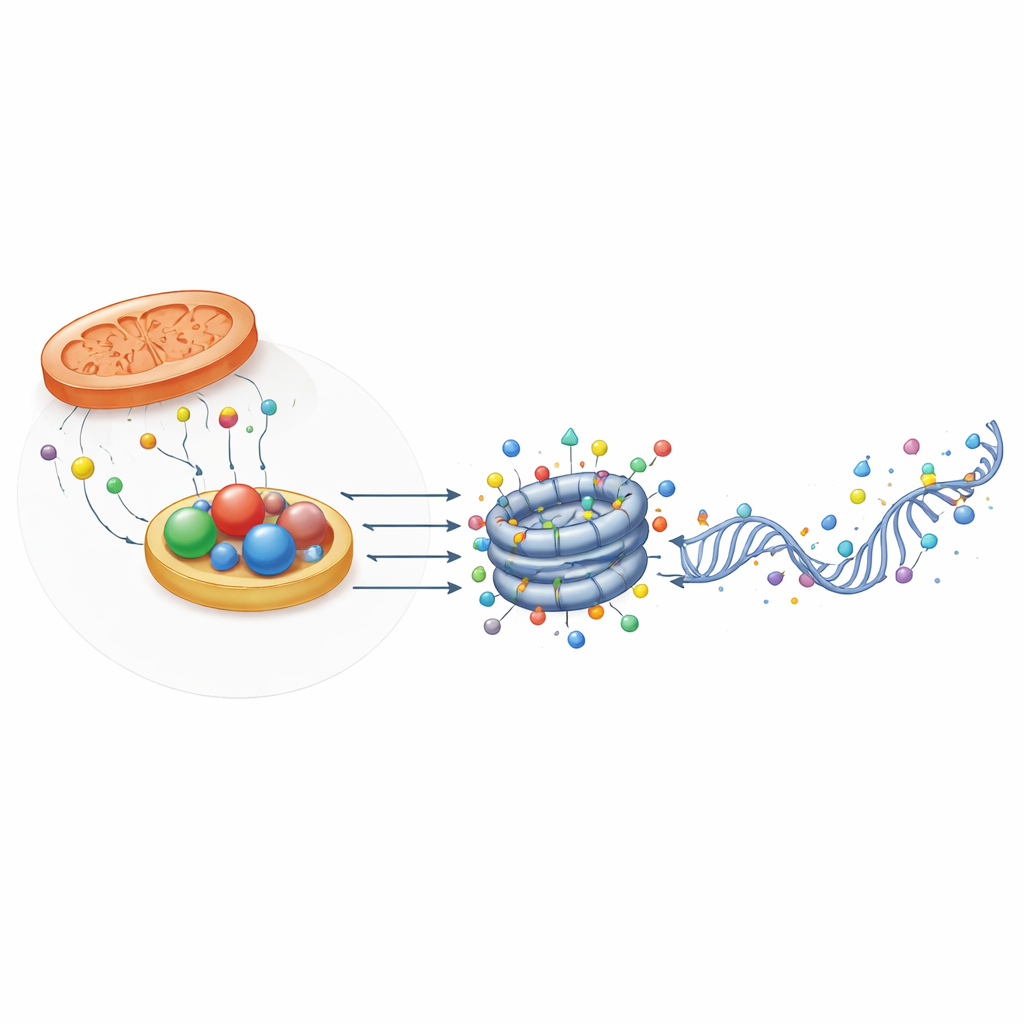
Redoks Durumunu Hisseden Yapısal Yardımcılar
İlginçtir ki, tüm oksidoredüktaz ilişkili proteinler enzim olarak davranmaz. CTBP ve NPAC/GLYR1 gibi bazıları NADH bağlayan yapısal katı koruyucu (fold) kalıntısını muhafaza eder ancak çok az veya hiç katalitik aktivite göstermez. Bunun yerine, belirli gen bölgelerinde transkripsiyon faktörleri ve kromatin düzenleyicilerini bir araya getiren çok birimli iskeletler oluştururlar. Bu yapıların oluşumu NAD(H) bağlanmasına bağlıdır; bu da onların hücrenin redoks durumunun fiziksel sensörleri olarak hareket edebileceği anlamına gelir. Fare embriyonik kök hücrelerinde CTBP2, farklılaşma sırasında pluripotensi genlerini kapatılmaya hazırlamak için asetil ve metil işaretlerini çıkaran kompleksleri çekerek yardımcı olurken, NPAC/GLYR1 LSD2 ve RNA polimeraz II ile birlikte transkripsiyonel uzama ve alternatif kesme‑birleştirmeyi koordine eder. Bu enzimsel olmayan roller, metabolizmanın gen kontrolünü etkilemesinde başka bir katman ekler.
Sağlık ve Hastalık Açısından Neden Önemli
Yazarlar sonuç olarak oksidoredüktazların metabolizmayı ve gen düzenlemesini üç düzeyde birleştirdiğini savunuyor: anahtar metabolitleri üretirler, DNA, RNA ve histonlardaki kimyasal işaretleri doğrudan silerler ve kromatin makinesini yeniden düzenleyen iskeletler olarak görev yaparlar. Bu işlevler birlikte hücrenin yakıt kullanımını hangi genlerin ifade edileceğine dair kalıcı yönergelere dönüştürür; böylece kök hücreliği korumaya ya da farklılaşmayı yönlendirmeye yardımcı olurlar. Bu çerçeve, metabolik mutasyonların hücreleri kanser benzeri durumlara nasıl yeniden programlayabildiğini ve besinleri veya metabolik enzimleri ayarlamanın kök hücre davranışını nasıl değiştirebileceğini açıklamaya yardımcı olur. Araştırmacılar bu bağlantıları daha ayrıntılı inceledikçe, oksidoredüktazlar hücrelerin enerji kullanımını yeniden düzenleyerek epigenetik manzarayı yeniden şekillendirmeyi hedefleyen rejeneratif tedaviler ve antikanser stratejiler için cazip hedefler olarak ortaya çıkıyor.
Atıf: Lee, HT., Roe, JS. & Youn, HD. Metabolic oxidoreductases: central regulators of the epigenetic landscapes in stemness. Exp Mol Med 58, 1017–1037 (2026). https://doi.org/10.1038/s12276-026-01687-2
Anahtar kelimeler: kök hücre metabolizması, epigenetik düzenleme, oksidoredüktaz enzimleri, kromatin yeniden şekillendirme, kanser kök hücreleri