Clear Sky Science · es
Oxidorreductasas metabólicas: reguladoras centrales de los paisajes epigenéticos en la pluripotencia
Cómo el combustible celular moldea la identidad celular
Cada célula de tu cuerpo contiene esencialmente el mismo ADN, sin embargo las neuronas, las células sanguíneas y las de la piel se ven y actúan de forma completamente distinta. Este artículo explora un vínculo sorprendente entre cómo las células procesan el combustible y cómo deciden en qué tipo de célula convertirse. Explica cómo una clase de enzimas llamadas oxidorreductasas, que normalmente gestionan la energía y los nutrientes, también ayudan a escribir y borrar las marcas químicas en el ADN y las proteínas que controlan qué genes se activan. Comprender esta conexión podría cambiar nuestra forma de pensar sobre las células madre, el envejecimiento e incluso el cáncer.
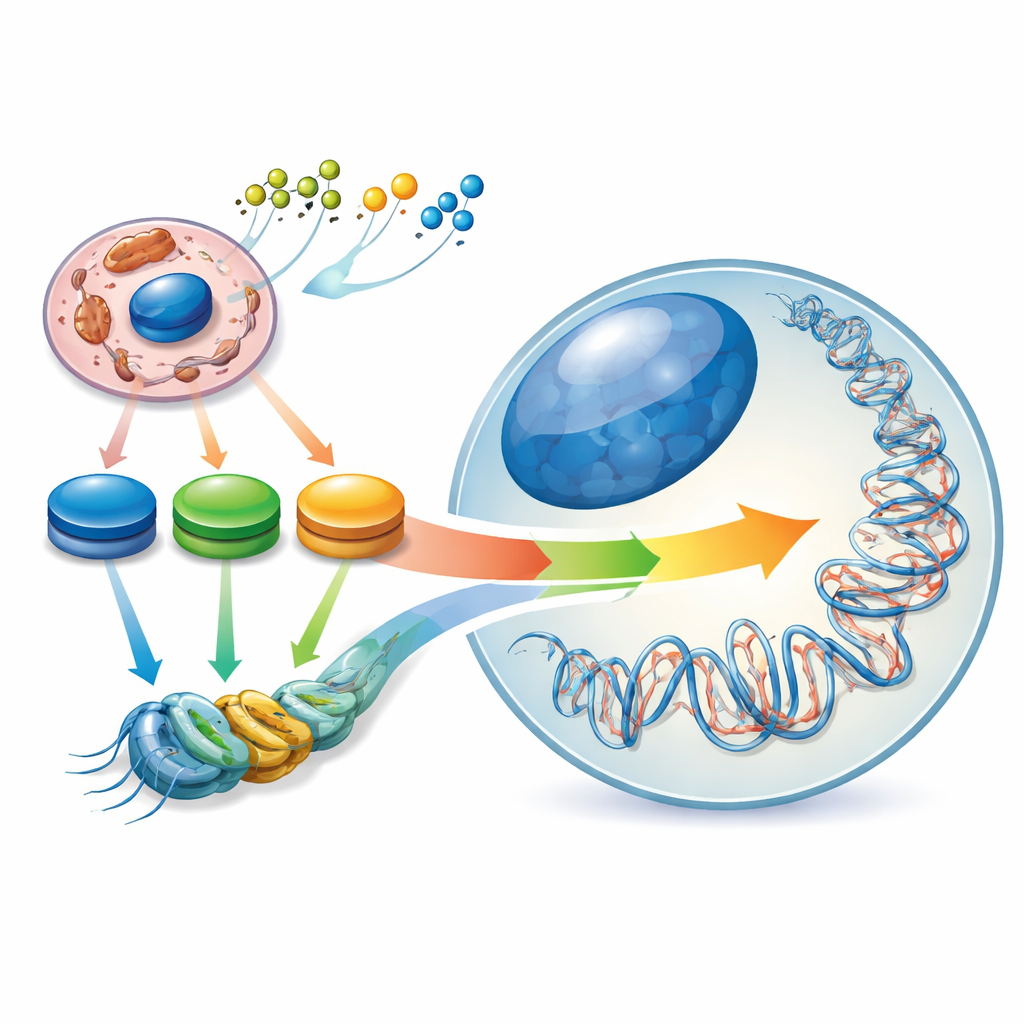
El paisaje oculto dentro de nuestros genes
Las células madre son especiales porque pueden renovarse o madurar en muchos tipos celulares diferentes. Manejan este equilibrio mediante un “paisaje epigenético” interno: patrones de etiquetas químicas en el ADN y sus proteínas de empaquetamiento que funcionan como reguladores de intensidad para los genes. Los autores describen este paisaje como modelado por una “curva energética” dentro de la célula: picos y valles en los niveles de moléculas metabólicas clave como acetil‑CoA, NAD⁺/NADH y α‑cetoglutarato. Cuando una célula madre pasa de un estado naïve a uno más comprometido, su metabolismo central del carbono se reconfigura y el paisaje epigenético cambia con él. Así, las variaciones en el uso del combustible celular no son solo consecuencias de la identidad celular: contribuyen activamente a determinarla.
Enzimas que convierten los alimentos en señales epigenéticas
Las oxidorreductasas son enzimas que catalizan reacciones de óxido‑reducción y ocupan puntos clave en el metabolismo. Muchas de ellas generan “metabolitos epigenéticos”, moléculas que sirven como materia prima o cofactores para enzimas que etiquetan el ADN y las histonas. Por ejemplo, deshidrogenasas en la glucólisis y el ciclo del TCA producen acetil‑CoA para la acetilación de histonas, NAD⁺/NADH y NADPH que influyen en las desacetilasas, y α‑cetoglutarato que alimenta a las desmetilasas de ADN e histonas. Al controlar cuánto de estos metabolitos está disponible, las oxidorreductasas determinan el rango de cambios epigenéticos posibles. Diferentes estados de las células madre dependen de mezclas metabólicas distintas: las células madre pluripotentes naïve utilizan tanto azúcar como grasa, las pluripotentes primed se apoyan en gran medida en la glucólisis y la glutamina, y muchas células madre adultas favorecen la degradación de ácidos grasos y la fosforilación oxidativa.
Editores directos de ADN, ARN e histonas
Algunas oxidorreductasas van más allá de suministrar ingredientes y reescriben directamente marcas epigenéticas. Enzimas dependientes de hierro y α‑cetoglutarato como las proteínas TET y las demetilasas JMJD eliminan grupos metilo del ADN y las histonas, remodelando qué genes están activos. Enzimas relacionadas, ALKBH5 y FTO, borran marcas metilo en el ARN, influyendo en la duración de los mensajes y en la eficiencia de su traducción. Otro grupo, LSD1 y LSD2, utiliza un cofactor flavínico para desmetilar lisinas específicas de histonas. Como todas estas enzimas requieren cofactores metabólicos y oxígeno, su actividad es exquisitamente sensible al estado energético y redox de la célula. La revisión muestra cómo cambios en α‑cetoglutarato, succinato o metabolitos mutantes en cáncer pueden inclinar la balanza entre una cromatina abierta y flexible y estados reprimidos y cerrados.
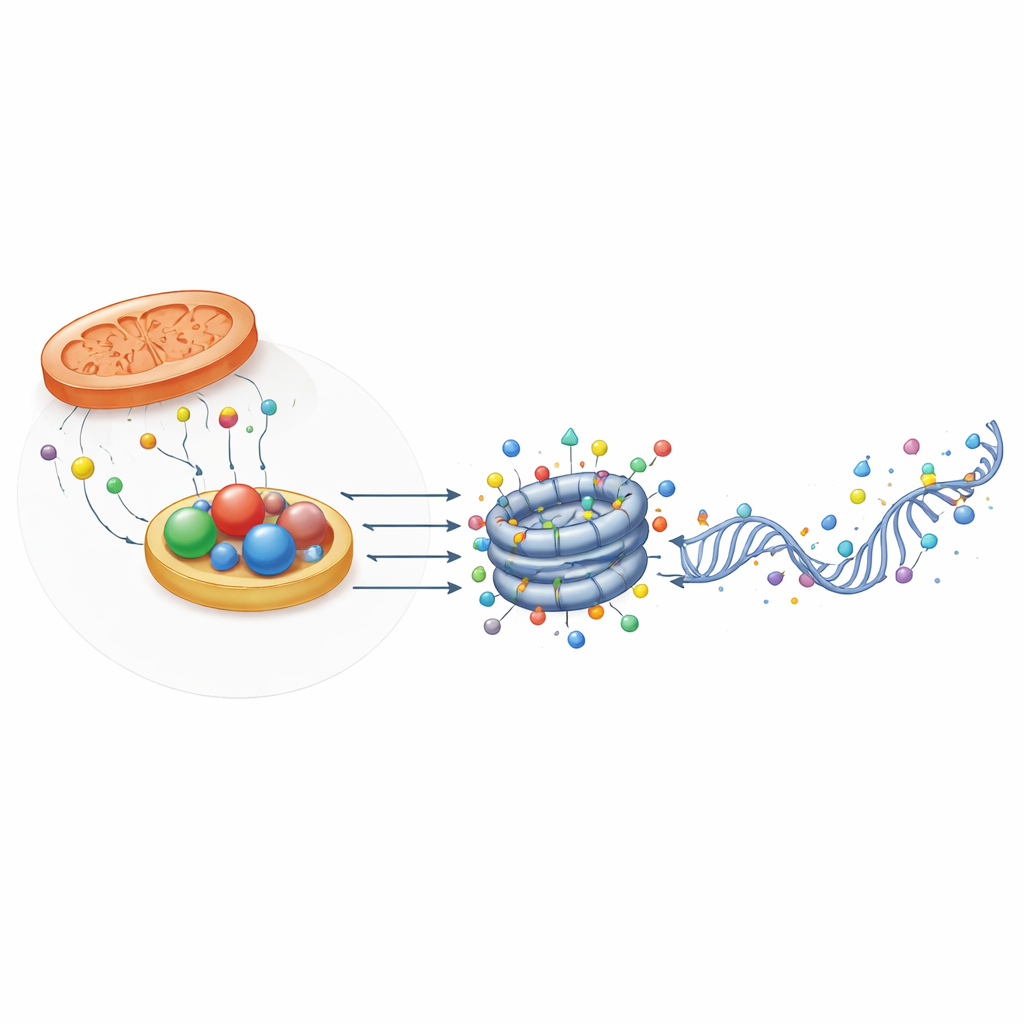
Ayudantes estructurales que detectan el estado redox
De manera intrigante, no todas las proteínas relacionadas con oxidorreductasas actúan como enzimas. Algunas, como CTBP y NPAC/GLYR1, conservan el dominio estructural que une NADH pero tienen poca o nula actividad catalítica. En lugar de eso, forman andamiajes multiproteicos que reúnen factores de transcripción y modificadores de la cromatina en regiones génicas específicas. Su ensamblaje depende de la unión a NAD(H), lo que significa que pueden actuar como sensores físicos del estado redox celular. En células madre embrionarias de ratón, CTBP2 ayuda a preparar los genes de pluripotencia para su apagado durante la diferenciación reclutando complejos que eliminan marcas de acetil y metilo, mientras que NPAC/GLYR1 se asocia con LSD2 y la ARN polimerasa II para coordinar la elongación transcripcional y el empalme alternativo. Estos roles no enzimáticos añaden otra capa por la que el metabolismo influye en el control génico.
Por qué esto importa para la salud y la enfermedad
Los autores concluyen que las oxidorreductasas integran metabolismo y regulación génica en tres niveles: generan metabolitos clave, borran directamente marcas químicas en el ADN, ARN e histonas, y actúan como andamiajes que reorganizan la maquinaria de la cromatina. En conjunto, estas funciones transforman el uso de combustible de una célula en instrucciones duraderas sobre qué genes expresar, ayudando a mantener la pluripotencia o a impulsar la diferenciación. Este marco ayuda a explicar por qué las mutaciones metabólicas pueden reprogramar células hacia estados similares al cáncer, y por qué ajustar nutrientes o enzimas metabólicas puede alterar el comportamiento de las células madre. A medida que los investigadores profundizan en estos enlaces, las oxidorreductasas emergen como dianas atractivas para terapias regenerativas y estrategias anticancerígenas que buscan remodelar el paisaje epigenético rehaciendo la gestión energética celular.
Cita: Lee, HT., Roe, JS. & Youn, HD. Metabolic oxidoreductases: central regulators of the epigenetic landscapes in stemness. Exp Mol Med 58, 1017–1037 (2026). https://doi.org/10.1038/s12276-026-01687-2
Palabras clave: metabolismo de células madre, regulación epigenética, enzimas oxidorreductasas, remodelado de la cromatina, células madre cancerosas