Clear Sky Science · ar
أكسيدoreدوكتازات الأيض: المنظمات المركزية للمشاهد فوق الجينية في الخلايا الجذعية
كيف يشكل وقود الخلية هوية الخلية
كل خلية في جسمك تحمل في الأساس نفس المادة الوراثية، ومع ذلك تبدو الخلايا العصبية وخلايا الدم وخلايا الجلد وتتصرف بشكل مختلف تمامًا. يستكشف هذا المقال رابطًا مفاجئًا بين كيفية معالجة الخلايا للوقود وكيفية تحديدها لنوع الخلية التي ستصبحها. يشرح كيف أن فئة من الإنزيمات تُسمى الأكسيدوالاختزالية، التي تتولى عادة التعامل مع الطاقة والمغذيات، تساعد أيضًا في كتابة وحذف العلامات الكيميائية على الحمض النووي والبروتينات التي تتحكم في تشغيل الجينات. قد يعيد فهم هذا الرابط تشكيل طريقة تفكيرنا بشأن الخلايا الجذعية والشيخوخة وحتى السرطان.
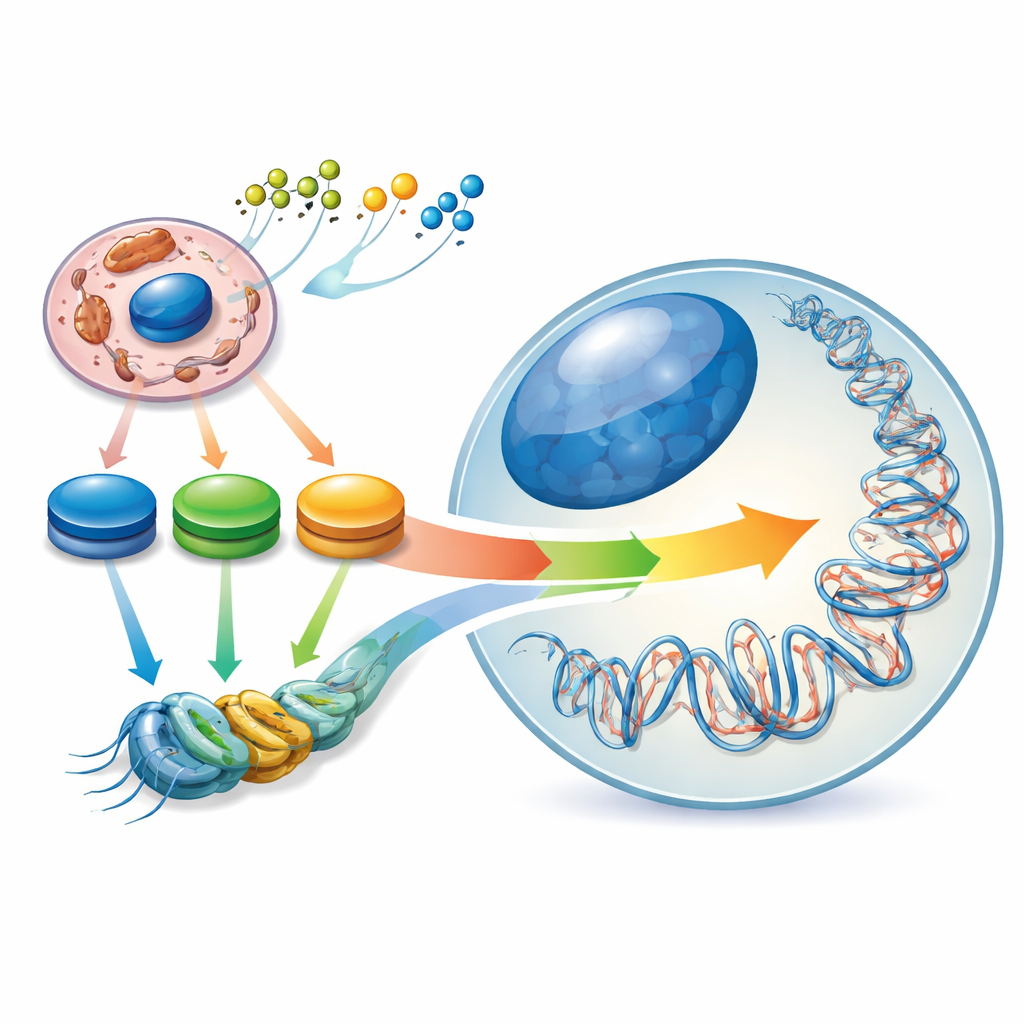
المشهد الخفي داخل جيناتنا
الخلايا الجذعية مميزة لأنها تستطيع إما أن تتجدد ذاتيًا أو تنضج إلى أنواع خلوية متعددة. تدير هذا التوازن من خلال "المشهد فوق الجيني" الداخلي — أنماط العلامات الكيميائية على الحمض النووي وبروتينات تغليفه التي تعمل كمخفتات للجينات. يصف المؤلفون هذا المشهد باعتباره مشكَّلاً بواسطة "محور طاقة" داخل الخلية: قمم ووديان في مستويات جزيئات أيضية رئيسية مثل أسيتيل-CoA وNAD⁺/NADH وα-كيتوغلوتارات. عندما تنتقل الخلية الجذعية من حالة بدائية إلى حالة أكثر التزامًا، يُعاد توصيل مسارات الكربون المركزية لديها، ويتغير المشهد فوق الجيني معها. بالتالي، فإن تغيُّرات استخدام الخلية للوقود ليست مجرد نتائج لهوية الخلية — بل تُسهم فعليًا في تحديدها.
إنزيمات تحول الغذاء إلى إشارات فوق جينية
الأكسيدوالاختزالات هي إنزيمات تحفز تفاعلات الأكسدة والاختزال وتقع عند مفاصل رئيسية في الأيض. العديد منها يُنتج "الوسائط الأيضية فوق الجينية"، وهي جزيئات تعمل كمادة خام أو كعوامل مساعد لِإنزيمات تضع علامات على الحمض النووي والهيستونات. على سبيل المثال، تنتج الديهيدروجينازات في التحلل السكري ودورة TCA أسيتيل-CoA لأستلة الهيستون، وNAD⁺/NADH وNADPH التي تؤثر على الديهيدروأسيلات، وα-كيتوغلوتارات التي تُشغِّل ديميثيلازات الحمض النووي والهيستون. من خلال التحكم بكمية هذه الوسائط المتاحة، تُحدد الأكسيدوالاختزالات نطاق التغيرات فوق الجينية الممكنة. تعتمد حالات الخلايا الجذعية المختلفة على تركيبات أيضية مختلفة: الخلايا الجذعية متعددة القدرات البدائية تستعين بالسكر والدهون معًا، أما الخلايا الجذعية المتأهبة فتتكأ بشدة على التحلل السكري والجلوتامين، وكثير من الخلايا الجذعية البالغة تفضّل تكسير الأحماض الدهنية والتنفس التأكسدي.
محررون مباشِرون للحمض النووي والـRNA والهيستونات
يتجاوز بعض الأكسيدوالاختزالات دور توفير المكوّنات ليُعيد كتابة العلامات فوق الجينية مباشرة. إنزيمات معتمدة على الحديد وα-كيتوغلوتارات مثل بروتينات TET وديميثيلازات JMJD تزيل مجموعات الميثيل من الحمض النووي والهيستونات، معيدة تشكيل الجينات النشطة. إنزيمات ذات صلة، مثل ALKBH5 وFTO، تمحو علامات الميثيل عن الـRNA، مؤثرة على مدة بقاء الرسائل وكفاءتها في الترجمة. مجموعة أخرى، LSD1 وLSD2، تستخدم عامل فلافين لإزالة ميثيل من ليزينات هيستون محددة. ولأن جميع هذه الإنزيمات تتطلب عوامل أيضية وأكسجينًا، فإن نشاطها حساس للغاية لحالة الطاقة والحالة التأكسدية للخلية. تُظهر المراجعة كيف أن التحولات في α-كيتوغلوتارات والسوكسينات أو وجود مستقلبات طفيرية في السرطان يمكن أن تُحرّك التوازن بين كروماتين مفتوح ومرن وحالات مقفلة ومكبوتة بإحكام.
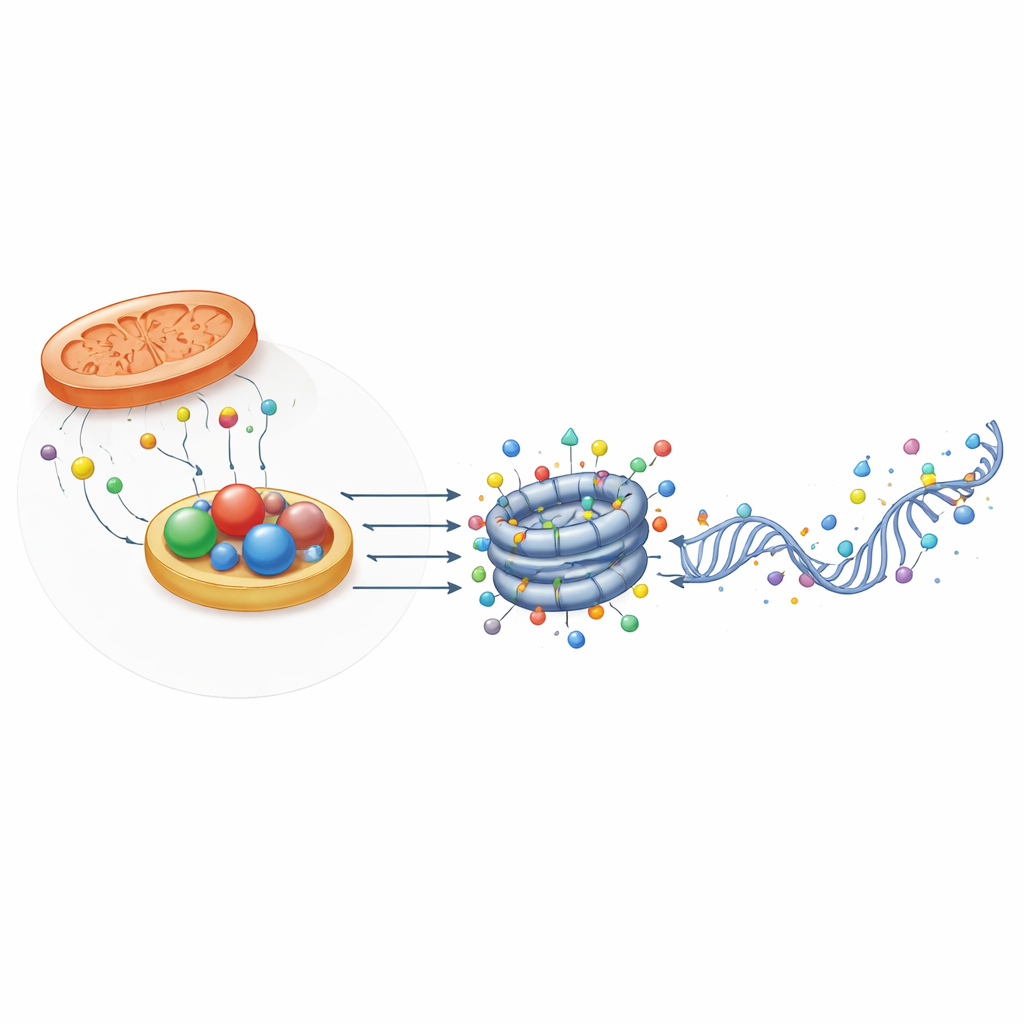
مساعدون بنيويون يحسون حالة الاختزال
من المثير أن ليس كل البروتينات المرتبطة بالأكسيدوالاختزال تعمل كإنزيمات. بعضها، مثل CTBP وNPAC/GLYR1، يحتفظ بثنية بنيوية تُحبس NADH لكنه يمتلك نشاطًا تحفيزيًا ضئيلًا أو معدومًا. بدلًا من ذلك، تُشكّل هذه البروتينات هياكل حمالة متعددة الوحدات تجمع عوامل النسخ ومعدِّلات الكروماتين عند مناطق جينية محددة. تعتمد تجمُّعاتها على ارتباط NAD(H)، مما يعني أنها يمكن أن تعمل كحساسات فيزيائية لحالة الاختزال الخلوي. في خلايا جذعية جنينية للفأر، يساعد CTBP2 في تهيئة جينات التعددية للانطفاء أثناء التمايز عن طريق تجنيد مركبات تزيل مجموعات الأسيتيل والميثيل، بينما يتعاون NPAC/GLYR1 مع LSD2 وبوليميراز RNA II لتنسيق استطالة النسخ والتطعيم البديل. تضيف هذه الأدوار غير الإنزيمية طبقة إضافية لكيفية تأثير الأيض على التحكم الجيني.
لماذا هذا مهم للصحة والمرض
يختتم المؤلفون بأن الأكسيدوالاختزالات تربط بين الأيض وتنظيم الجينات على ثلاثة مستويات: فهي تُنتج الوسائط الأيضية الرئيسية، وتمحو مباشرة العلامات الكيميائية على الحمض النووي والـRNA والهيستونات، وتعمل كحمالات تُعيد تنظيم ألات الكروماتين. معًا، تحوّل هذه الوظائف استخدام الخلية للوقود إلى تعليمات دائمة حول أي الجينات تُعبر، مما يساعد على الحفاظ على الحالة الجذعية أو دفع التمايز. يفسر هذا الإطار لماذا يمكن للطفرات الأيضية أن تعيد برمجة الخلايا نحو حالات شبيهة بالسرطان، ولماذا يغيِّر تعديل المغذيات أو إنزيمات الأيض سلوك الخلايا الجذعية. ومع مواصلة الباحثين فحص هذه الروابط بتفصيل أكبر، تبرز الأكسيدوالاختزالات كأهداف واعدة للعلاجات التجددية واستراتيجيات مضادة للسرطان التي تهدف إلى إعادة تشكيل المشهد فوق الجيني عن طريق إعادة توصيل كيفية تعامل الخلايا مع الطاقة.
الاستشهاد: Lee, HT., Roe, JS. & Youn, HD. Metabolic oxidoreductases: central regulators of the epigenetic landscapes in stemness. Exp Mol Med 58, 1017–1037 (2026). https://doi.org/10.1038/s12276-026-01687-2
الكلمات المفتاحية: تمثيل الخلايا الجذعية, التنظيم فوق الجيني, إنزيمات الأكسيدوالاختزال, إعادة تشكيل الكروماتين, خلايا جذعية سرطانية